Активни састојци: Ацеторпхане
Тиорфик 10 мг грануле за оралну суспензију
Улошци за пакет Тиорфик доступни су за величине паковања:- Тиорфик 10 мг грануле за оралну суспензију
- Тиорфик 30 мг грануле за оралну суспензију
- Тиорфик капсуле од 100 мг
Индикације Зашто се користи Тиорфик? За шта је то?
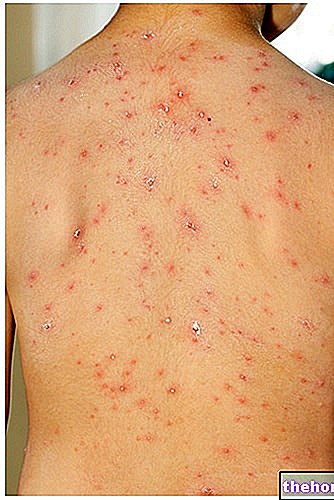
Тиорфик је лек за лечење дијареје.
Тиорфик се користи за симптоматско лечење акутне дијареје код деце старије од три месеца. То мора бити повезано са уносом обилне течности и са уобичајеним мерама исхране, када саме ове мере нису довољно ефикасне за контролу дијареје и када узрочно лечење није могуће.
Рацецадотрил се може давати као комплементаран третман када је могуће узрочно лечење.
Контраиндикације Када се Тиорфик не сме користити
Немојте давати Тиорфик
- Ако је дете алергично (преосетљиво) на рацекадотрил или било који други састојак лека Тиорфик.
- Ако вам је лекар рекао да ваше дете не подноси неке шећере, питајте лекара пре него што свом детету дате Тиорфик.
Мере опреза при употреби Шта треба да знате пре него што узмете лек Тиорфик
Разговарајте са својим лекаром или фармацеутом пре него што свом детету дате Тиорфик.
Реците свом лекару ако:
- Ваша беба има мање од три месеца,
- Пронађите крв или гној у бебиној столици и беба има температуру. Узрок дијареје може бити „бактеријска инфекција коју треба лечити лекар.
- Ваше дете има хроничну дијареју или дијареју узроковану антибиотицима,
- Ваше дете има болест бубрега или оштећену функцију јетре,
- Ваше дете пати од продуженог или неконтролисаног повраћања,
- Ваше дете има дијабетес (погледајте "Важне информације о неким састојцима лека Тиорфик").
Интеракције Који лекови или храна могу да промене учинак Тиорфик -а
Обавестите свог лекара ако ваше дете узима или је недавно узимало било које друге лекове, укључујући и лекове који се добијају без рецепта.
Упозорења Важно је знати да:
Трудноћа, дојење и плодност
Употреба лека Тиорфик се не препоручује ако сте трудни или дојите. Обратите се свом лекару или фармацеуту пре него што узмете било који лек.
Вожња и управљање машинама
Тиорфик нема или има занемарљив утицај на способност управљања возилима и рада на машинама.
Важне информације о неким састојцима лека Тиорфик
Тиорфик садржи приближно 1 г сахарозе по кесици.
Ако вам је лекар рекао да ваша беба не подноси неке шећере, контактирајте га пре него што беби дате Тиорфик.
Код одојчади са дијабетесом, ако је ваш лекар преписао вашој беби више од 5 кесица Тиорфик -а дневно (еквивалентно више од 5 г сахарозе), то треба узети у обзир при израчунавању укупног дневног уноса шећера бебе.
Доза, начин и време примене Како се користи Тиорфик: Дозирање
Тиорфик се испоручује у облику гранула.
Грануле се морају додати храни или растворити у чаши воде или у флашици за бебе, добро промешати и дати одмах.
Препоручена дневна доза зависи од тежине детета: 1,5 мг / кг по дози (једнако 1 или 2 кесице), три пута дневно у редовним интервалима.
Код одојчади тежине мање од 9 кг: једна кесица по дози.
Код одојчади од 9 кг до 13 кг: две кесице по дози.
Увек дајте детету Тиорфик тачно онако како вам је рекао лекар. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
Ваш лекар ће вам рећи колико дуго да наставите лечење Тиорфиком. То треба наставити све док беба не произведе две нормалне столице, најкасније у року од 7 дана.
Да би се надокнадио губитак течности услед дијареје, овај лек треба користити заједно са „одговарајућом надокнадом течности и соли (електролита). Најбољи додатак течности и соли постиже се такозваним раствором за оралну рехидратацију (ако постоји било каква сумња, молимо контактирајте нас). питајте свог лекара или фармацеута).
Предозирање Шта треба учинити ако сте узели превише Тиорфик -а
Ако сте узели више лека Тиорфик него што је требало
Ако је ваше дете узело више лека Тиорфик него што је требало, одмах се обратите лекару или фармацеуту.
Ако сте заборавили да узмете Тиорфик
Немојте давати свом детету двоструку дозу да надокнади заборављену дозу. Наставите са лечењем као и обично.
Нежељени ефекти Који су нежељени ефекти Тиорфик -а
Као и сви други лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих.
Пријављени су следећи неуобичајени нежељени ефекти (утичу на 1 до 10 корисника на 1000): тонзилитис (упала амигдала), осип и еритем (црвенило коже).
Остали нежељени ефекти (чија се учесталост не може проценити из доступних података) су: мултиформни еритем (ружичасте лезије на екстремитетима и унутар уста), упала језика, упала лица, упала усана, упала капака, ангиоедем (поткожна упала у различитим деловима тела), уртикарија , нодосум еритема (упала у облику квржице испод коже), папуларни осип (осип на кожи са малим, тврдим, квргавим лезијама), пруриго (кожне лезије које сврбе), свраб (општи осећај свраба).
Одмах престаните да дајете Тиорфик свом детету и одмах се обратите лекару ако ваше дете покаже симптоме ангиоедема, као што су:
- отечено лице, језик или ждрело
- отежано гутање
- кошница и отежано дисање
Ако неко од нежељених дејстава постане озбиљно или ако приметите било које нежељено дејство које није наведено у овом упутству, обавестите свог лекара или фармацеута.
Истек и задржавање
Чувати ван домашаја и погледа деце.
Немојте користити Тиорфик након истека рока ваљаности наведеног на секундарном паковању иза "ЕКСП". Датум истека се односи на последњи дан у месецу.
Лекове не треба одлагати у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Овај лек не захтева посебне услове складиштења.
Пре употребе прочитајте упутство за употребу.
Шта Тиорфик садржи
Активни састојак је рацекадотрил. Свака кесица садржи 10 мг рацекадотрила.
Остали састојци су:
Сахароза,
Безводни колоидни силицијум диоксид,
Дисперзија полиакрилата 30%,
Арома кајсије
Како Тиорфик изгледа и садржај паковања
Тиорфик је представљен у облику гранула за оралну суспензију садржаних у кесицама.
Свако паковање садржи 10, 16, 20, 30, 50 или 100 кесица (паковање од 100 кесица само за болничку употребу).
Не могу се на тржиште ставити све величине паковања
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ТИОРФИКС 10 МГ ГРАНУЛЕ ЗА УСМЕНУ УСМЕЊУ
02.0 КВАЛИТАТИВНИ И КОЛИЧИНСКИ САСТАВ
Свака кесица садржи 10 мг рацекадотрила.
Свака кесица садржи 966,5 мг сахарозе.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Грануле за оралну суспензију.
Бели прах са карактеристичним мирисом кајсије.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Комплементарно симптоматско лечење акутне дијареје код одојчади (преко 3 месеца) и одојчади, заједно са оралном рехидрацијом и уобичајеним мерама подршке, када саме такве мере нису довољне за контролу клиничког стања и када узрочно лечење није могуће.
Ако је могуће узрочно лечење, рацекадотрил се може дати као комплементаран третман.
04.2 Дозирање и начин примене
ТИОРФИКС 10 мг се примењује орално, заједно са растворима за оралну рехидратацију (видети одељак 4.4).
ТИОРФИКС 10 мг намењен је деци тежине
Препоручена доза се одређује на основу телесне тежине: 1,5 мг / кг по дози (једнако 1 или 2 кесице), три пута дневно у редовним интервалима.
Код одојчади тежине мање од 9 кг: једна кесица од 10 мг 3 пута дневно.
Код одојчади од 9 кг до 13 кг: 2 кесице од 10 мг 3 пута дневно.
Трајање лечења у клиничким испитивањима код деце је било 5 дана. Третман треба наставити све док се не произведу два нормална фекална испуштања. Лечење не би требало да прелази 7 дана. Не препоручује се дуготрајно лечење рацекадотрилом.
Нису доступне клиничке студије за одојчад млађу од 3 месеца.
Посебне популације:
Нису доступне студије код одојчади или деце са оштећењем бубрега или јетре (видети одељак 4.4).
Опрез се препоручује код пацијената са оштећењем јетре или бубрега.
Грануле се могу додати храни, растворити у чаши воде или у флашици за бебе, добро промешати и дати одмах.
04.3 Контраиндикације
Преосетљивост на активне супстанце или било коју помоћну супстанцу наведену у одељку 6.1.
Овај лијек садржи сахарозу. Пацијенти са ретким наследним проблемима интолеранције на фруктозу, малапсорпције глукозе-галактозе или инсуфицијенције сахаразе-изомалтазе не би требало да узимају овај лек.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Примена ТИОРФИКС -а 10 мг не мења уобичајене режиме рехидратације. Неопходно је да дете пије пуно течности.
У случају тешке или продужене дијареје са јаким повраћањем или губитком апетита, треба размотрити интравенозну рехидрацију.
Присуство крваве или гнојне столице и грознице може указивати на присуство инвазивних бактерија одговорних за дијареју или присуство других озбиљних стања. Осим тога, Рацецадотрил није тестиран на дијареју повезану са антибиотицима. Због тога се Рацецадотрил не сме примењивати у овим условима.
Нема довољно студија о лечењу хроничне дијареје са овим производом.
За пацијенте са дијабетесом треба узети у обзир да свака кесица садржи 0,966 г сахарозе.
Ако количина сахарозе (извор глукозе и фруктозе) присутна у дневној дози од 10 мг ТИОРФИКС -а прелази 5 г дневно, то се мора узети у обзир за дневну дозу шећера.
Производ не треба давати одојчади млађој од 3 месеца због одсуства клиничких студија у овој популацији.
Производ не треба давати деци са оштећењем бубрега или јетре, без обзира на степен озбиљности, због недостатка информација о овој популацији пацијената.
Због могуће ниже биорасположивости, производ се не сме давати у случају продуженог или неконтролисаног повраћања.
04.5 Интеракције са другим лековима и други облици интеракција
До сада нису описане никакве интеракције са другим активним састојцима код људи.
Код људи, истовремени третман са рацецадотрилом и лоперамидом или нифуроксазидом не мења кинетику рацекадотрила.
04.6 Трудноћа и дојење
Плодност
Студије плодности спроведене са рацекадотрилом на пацовима Спрагуе-Давлеи не показују утицај на плодност.
Трудноћа
Нема одговарајућих података о употреби рацекадотрила код трудница. Студије на животињама нису показале директне или индиректне штетне ефекте на трудноћу, плодност, ембрионални развој фетуса, пород или постнатални развој. Међутим, због непостојања било каквих специфичних Према доступним клиничким студијама, рацекадотрил се не сме давати трудницама.
Време храњења
Због недостатка информација о лучењу рацекадотрила у мајчино млеко, овај лек се не сме давати женама које доје.
04.7 Утицај на способност управљања возилима и машинама
Није битно.
Рацецадотрил нема или има занемарљив утицај на способност управљања возилима и рада на машинама.
04.8 Нежељени ефекти
Доступни су подаци из клиничких испитивања која су укључивала 860 педијатријских пацијената са акутном дијарејом лечених рацекадотрилом и 441 лечених плацебом.
Доле наведени нежељени ефекти јављали су се чешће код рацекадотрила него код плацеба или су пријављени током постмаркетиншког надзора. Учесталост нежељених ефеката дефинисана је следећом конвенцијом: врло често (≥ 1/10), често (≥ 1/100 до
Инфекције и инфестације
Мање често: тонзилитис.
Поремећаји коже и поткожног ткива
Мање често: осип, еритем.
Непознато: мултиформни еритем, језични едем, едем лица, едем усана, очни едем, ангиоедем, уртикарија, нодосум еритема, папуларни осип, пруриго, пруритус.
04.9 Предозирање
Нису забележени случајеви предозирања. Појединачне дозе веће од 2 г, еквивалентне 20 пута већој терапијској дози, примењене су код одраслих и нису описани никакви штетни ефекти.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: други лекови против дијареје.
АТЦ ознака: А07КСА04.
Рацецадотрил је предлијек који се мора хидролизирати у свој активни метаболит тиорфан, који је инхибитор енцефалиназе, ензима ћелијске мембране пептидазе који се налази у различитим ткивима, посебно у епителу танког цријева. Овај ензим доприноси пробави пептида. разградња ендогених пептида, попут енкефалина Рацецадотрил штити енкефалине од ензимске разградње продужавањем њиховог деловања на нивоу енцефалинергичких синапси у танком цреву и смањењем хиперсекреције.
Рацецадотрил је чисти цревни антисекреторни активни састојак. Изазива смањење цревне хиперсекреције воде и електролита изазвано токсином колере или инфламаторним стањем, и нема утицаја на базалну секреторну активност. Рацецадотрил има брзу антидијарејску активност, не мењајући време проласка кроз црева..
У два клиничка испитивања на деци, рацекадотрил је смањио фекалну тежину за 40%, односно 46%, у првих 48 сати. Уочено је и значајно смањење трајања дијареје и потреба за рехидратацијом.
Мета-анализа (9 рандомизованих клиничких испитивања рацекадотрила у односу на плацебо, поред оралног рехидратационог раствора) прикупила је податке о појединачним пацијентима од 1384 дечака и девојчица са акутном дијарејом различите тежине и који су третирани као стационарни или амбулантни. Просечна старост је била 12 месеци (интерквартилни распон: 6 до 39 месеци). Укупно 714 пацијената било је млађе од 1 године, а 670 пацијената је имало 1 годину или више. Пацијенти између студија кретали су се од 7,4 кг до 12,2 кг. Просечно трајање дијареје након укључивања износило је 2,81 дан за плацебо групу и 1,75 дана за групу са рацекадотрилом. Удео хоспитализованих пацијената био је већи у групама са рацекадотрилима у поређењу са плацебом [ХР (однос опасности): 2,04; 95% ЦИ: 1,85 до 2,32; п 1 година) (ХР: 2,16; 95% ЦИ: 1,83 до 2,57; стр
Рацецадотрил не изазива дистензију абдомена. Током свог клиничког развоја, рацекадотрил је проузроковао настанак секундарне опстипације у проценту пацијената упоредив са оним који се примећује при давању плацеба.У случају оралне примене, активност се врши искључиво на периферном нивоу, без ефеката на централни нервни систем .
Рандомизована унакрсна студија показала је да капсуле од 100 мг рацекадотрила у терапијској дози (1 капсула) или у над-терапијској дози (4 капсуле) нису изазвале продужење КТ / КТц интервала код 56 здравих добровољаца (за разлику од моксифлоксацина, који се користи као контрола).
05.2 Фармакокинетичка својства
Апсорпција
Рацецадотрил се брзо апсорбује након оралне примене.
Дистрибуција
У плазми, након оралне дозе рацекадотрила означеног са Ц-14, измерена изложеност радио-угљенику била је за много степена веће него у крвним ћелијама и 3 пута већа него у пуној крви. Због тога се лек није везао за крвне ћелије на значајном нивоу. Дистрибуција радиокарбона у друга телесна ткива била је умерена, на шта указује средњи привидни волумен дистрибуције у плазми од 66,4 кг.
Деведесет процената активног метаболита рацекадотрила (тиорфан = (РС) -Н -(1 -оксо -2 -(меркаптометил) -3 -фенилпропил) глицин) се везује за протеине плазме, углавном за албумин.
Трајање и опсег дејства рацекадотрила зависе од дозе. Вршна инхибиција енцефалиназе у плазми постиже се за приближно 2 сата и одговара 90% инхибицији са дозом од 1,5 мг / кг.Трајање инхибиције енцефалиназе у плазми је приближно 8 сати.
Метаболизам
Полуживот рацекадотрила, израчунат као инхибиција енцефалиназе у плазми, је приближно 3 сата.
Рацецадотрил се брзо хидролизује у тиорфан (РС) -Н -(1 -окси -2 -(меркаптометил) -3 -фенилпропил) глицин, активни метаболит, заузврат се претвара у неактивне метаболите идентификоване као С -метилтхиорфан сулфоксид, тиорфан С -метил , 2 -метаносулфинилметил пропионске киселине и 2 -метилсулфанилметил пропионске киселине, сви настали са системском изложеношћу матичном леку већом од 10%.
Други мањи метаболити су такође откривени и квантификовани у урину и измету.
Подаци ин витро указују да рацекадотрил / тиорфан и четири главна неактивна метаболита не инхибирају главне изоформе ензима ЦИП 3А4, 2Д6, 2Ц9, 1А2 и 2Ц19 на клинички релевантним нивоима.
Подаци ин витро указују да рацекадотрил / тиорфан и четири главна неактивна метаболита не индукују изоформе ензима ЦИП (породица 3А, 2А6, 2Б6, 2Ц9 / 2Ц19, породица 1А, 2Е1) и УГТ коњуговане ензиме на клинички релевантним нивоима.
У педијатријској популацији, фармакокинетички резултати су слични онима у одраслој популацији, са Цмак достигнутим 2 сата и 30 минута након дозирања. Не долази до акумулације након вишеструких доза датих сваких 8 сати током 7 дана.
Излучивање
Рацецадотрил се елиминише у облику активних и неактивних метаболита. Излучивање се одвија углавном путем бубрега (81,4%) и, у знатно мањој мери, фекалним путем (приближно 8%). Плућни пут није значајан (мање од 1%дозе).
05.3 Предклинички подаци о безбедности
Четворонедељне студије хроничне токсичности на мајмунима и псима, прилагођене трајању лечења код људи, не указују на ефекте при дозама до 1250 мг / кг / дан и 200 мг / кг, што одговара сигурносним границама од 625 и 62 (у односу на човеку). Рацецадотрил није био имунотоксичан код мишева третираних рацекадотрилом до 1 месеца. Дужа (1 година) изложеност код мајмуна показала је генерализоване инфекције и смањење одговора антитела вакцинацијом у дози од 500 мг / кг / дан и без инфекције / имуносупресије у дози од 120 мг / кг / дан. Слично, неки параметри инфекције / имунитета варирали су код пса који је лечен са 200 мг / кг / дан током 26 недеља. Клиничка важност није позната, видети одељак 4.8.
У стандардним тестовима нису пронађени мутагени или кластогени ефекти рацекадотрила ин витро И ин виво.
Нису рађени тестови канцерогености са рацекадотрилом јер је лек намењен за краткотрајно лечење.
Токсичност по репродукцију и развој (студије о плодности и раном ембрионалном развоју, пренаталном и постнаталном развоју укључујући функцију мајке, ембрионално-фетални развој) нису откриле специфичне ефекте за рацекадотрил.
Студија токсичности на младим пацовима није показала значајне ефекте рацекадотрила до дозе од 160 мг / кг / дан, што је 35 пута више од уобичајеног педијатријског режима (тј. 4,5 мг / кг / дан).
Упркос незрелости бубрежне функције код одојчади млађе од 1 године, не очекују се већи нивои изложености код ових особа.
Остали претклинички ефекти (нпр. Тешка анемија, вероватно апластична, повећана диуреза, кетонурија, дијареја) забележени су само у случајевима изложености за коју се сматра да премашује максимално очекивано излагање људима. Клиничка важност није позната.
Друге безбедносне фармаколошке студије нису откриле штетне ефекте рацекадотрила на централни нервни систем, кардиоваскуларне и респираторне функције.
Код животиња, рацекадотрил је изазвао повећање ефеката бутилскополамина на цревни транзит и на антиконвулзивне ефекте фенитоина.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Сахароза
Безводни колоидни силицијум диоксид
Дисперзија полиакрилата 30%
Арома кајсије.
06.2 Некомпатибилност
Није битно.
06.3 Период важења
2 године.
06.4 Посебне мере предострожности при складиштењу
Овај лек не захтева посебне услове складиштења.
06.5 Природа непосредног паковања и садржај паковања
Торбе од папира / алуминијума / полиетилена топлотно запечаћене.
Паковања од 10, 16, 20, 30, 50 и 100 кесица (100 кесица само за болничку употребу).
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Нема посебних упутстава.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
БИОПРОЈЕТ ЕУРОПЕ ЛТД
29 Еарлсфорт тераса,
2, Даблин
Иреланд
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
АИЦ н. 037518115 / М "Грануле од 10 мг за оралну суспензију" 10 кесица у папиру / Ал / ПЕ - рано детињство
АИЦ н. 037518127 / М "Грануле од 10 мг за оралну суспензију" 16 папирних / Ал / ПЕ кесица - рано детињство 20
АИЦ н. 037518139 / М "Грануле од 10 мг за оралну суспензију" 20 папирних / Ал / ПЕ кесица - рано детињство 30
АИЦ н. 037518141 / М "10 мг грануле за оралну суспензију" 30 кесица у папиру / Ал / ПЕ - рано детињство 50
АИЦ н. 037518154 / М "10 мг грануле за оралну суспензију" 50 кесица у папиру / Ал / ПЕ - рано детињство
АИЦ н. 037518166 / М "10 мг грануле за оралну суспензију" 100 кесица у папиру / Ал / ПЕ - рано детињство
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
/
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
08/03/2013