Активни састојци: лакозамид
Вимпат 50 мг филмом обложене таблете
Вимпат 100 мг филмом обложене таблете
Вимпат 150 мг филмом обложене таблете
Вимпат 200 мг филмом обложене таблете
Улошци за паковање Вимпат доступни су за величине паковања: - Вимпат 50 мг филм таблете, Вимпат 100 мг филм таблете, Вимпат 150 мг филм таблете, Вимпат 200 мг филм таблете
- Вимпат 10 мг / мл сируп
- Вимпат 10 мг / мл раствор за инфузију
Индикације Зашто се користи Вимпат? За шта је то?
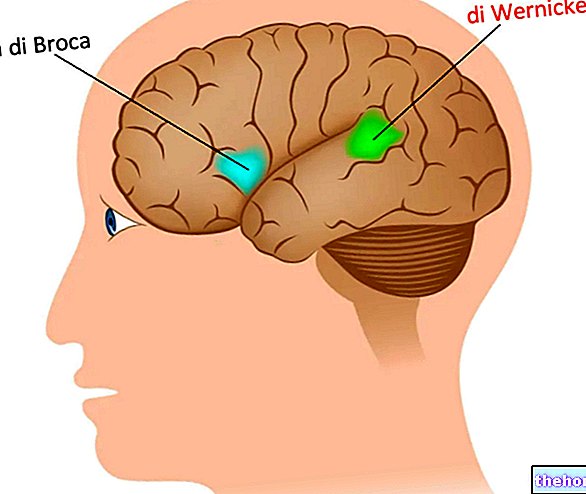
Лакозамид (Вимпат) се користи за лечење одређеног облика епилепсије (види доле) код пацијената старијих од 16 година. Вимпат се користи као додатак другим антиепилептичким лековима. Епилепсија је стање у којем се пацијенти понављају (грчеви). Вимпат се користи за онај облик епилепсије у којем нападаји у почетку захваћају само једну страну мозга, али се касније могу проширити на већа подручја с обје стране. (делимични напади са или без секундарне генерализације) Ваш лекар вам је преписао Вимпат да бисте смањили број напада.
Контраиндикације Када се Вимпат не сме користити
Немојте узимати Вимпат
- ако сте алергични на лакозамид или неки други састојак овог лека (наведен у одељку 6). Ако нисте сигурни да ли сте алергични, обратите се свом лекару
- ако патите од одређене врсте поремећаја срчаног ритма (АВ блок другог или трећег степена)
Мере опреза при употреби Шта треба да знате пре него што узмете лек Вимпат
Мали број пацијената који се лече антиепилептичким лековима, као што је лакозамид, имао је мисли о повређивању или самоубиству. Ако имате такве мисли, одмах се обратите лекару.
Разговарајте са својим лекаром пре него што узмете Вимпат ако имате стање које је повезано са ослабљеном електричном проводљивошћу кроз срце (АВ блок, атријална фибрилација и атријално треперење) или тешка срчана обољења као што су срчана инсуфицијенција или срчани удар. Симптоми АВ блока су успорен или неправилан пулс, осећај вртоглавице и несвестица. У случају атријалне фибрилације и треперења атрија, можете доживети симптоме као што су лупање срца, убрзан или неправилан пулс и отежано дисање.
Вимпат може изазвати вртоглавицу, што може повећати ризик од случајних повреда или пада. Зато будите опрезни док се не навикнете на могуће нежељене ефекте које овај лек може изазвати.
Деца и адолесценти
Вимпат се не препоручује деци и адолесцентима млађим од 16 година. Безбедност и ефикасност у овој старосној групи још нису познати.
Интеракције Који лекови или храна могу променити дејство лека Вимпат
Други лекови и Вимпат
Реците свом лекару или фармацеуту ако узимате, недавно сте узимали или бисте могли да узмете било који други лек. Ово је посебно важно ако узимате лекове за лечење срчаних обољења или ако узимате било које лекове који могу изазвати абнормалности ЕКГ -а (електрокардиограм) који се називају продужење ПР интервала, укључујући карбамазепин, ламотригин, прегабалин (лекови који се користе за лечење срчаних обољења) . епилепсија) и лекове који се користе за лечење неких облика неправилног рада срца или срчане инсуфицијенције. Ако нисте сигурни да ли неки лекови које узимате могу имати овакав ефекат, обратите се лекару. Лекови као што су флуконазол, итраконазол, кетоконазол (лекови који се користе за лечење гљивичне инфекције), ритонавир (лек који се користи за лечење ХИВ инфекција), кларитромицин, рифампицин (лекови за лечење бактеријских инфекција) и кантарион (лек који се користи за лечење благе анксиозности) могу утицати на то како јетра разграђује лакозамид.
Вимпат са алкохолом
Из сигурносних разлога, немојте узимати Вимпат са алкохолом.
Упозорења Важно је знати да:
Трудноћа и дојење
Ако сте трудни или дојите, мислите да сте трудни или планирате трудноћу, питајте свог лекара или фармацеута за савет пре него што узмете овај лек.
Не препоручује се узимање Вимпата током трудноће, јер ефекти Вимпата на фетус нису познати. Ако сте трудни или планирате трудноћу, одмах обавестите свог лекара који ће одлучити да ли можете узети Вимпат.
Дојење се не препоручује током лечења леком Вимпат, јер није познато да ли Вимпат прелази у мајчино млеко. Ако дојите, одмах обавестите свог лекара који ће одлучити да ли можете узети Вимпат.
Истраживања су показала повећан ризик од урођених мана код беба рођених од жена на антиепилептичкој терапији. С друге стране, ефикасна антиепилептичка терапија не сме се прекидати, јер погоршање болести може бити штетно и за мајку и за фетус.
Вожња и управљање машинама
Вимпат може изазвати вртоглавицу или замагљен вид. То може утицати на способност управљања возилима или рада са алатима или машинама. Не возите и не рукујте машинама док не проверите да ли овај лек утиче на вашу способност обављања ових активности.
Доза, начин и време примене Како се користи Вимпат: Дозирање
Увек узимајте овај лек тачно онако како вам је рекао ваш лекар или фармацеут. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
Дозирање
Узимајте Вимпат два пута дневно, једном ујутру и једном увече, отприлике у исто време сваког дана. Вимпат се користи као дуготрајан третман.
Почетак терапије (прве 4 недеље) Овај пакет (пакет за почетак терапије) је за вас да започнете терапију леком Вимпат. Паковање садржи 4 различита паковања за прве 4 недеље терапије, по једно за сваку недељу. Свако паковање садржи 14 таблета, што одговара 2 таблете дневно током 7 дана. Свако паковање садржи различиту јачину лека Вимпат, што вам омогућава да постепено повећавате дозу. Лечење ћете започети ниском дозом Вимпата, обично 50 мг два пута дневно, и постепено повећавати дозу из недеље у недељу. Доза која се најчешће може узимати сваки дан током прве 4 недеље терапије приказана је у доњој табели. Ваш лекар ће вам рећи да ли морате да користите сва 4 паковања.
Табела: почетак терапије (прве 4 недеље)
Терапија одржавања (након прве 4 недеље)
Након прве 4 недеље лечења, лекар може прилагодити дозу коју ћете наставити да узимате за дуготрајну терапију. Ова доза се назива доза одржавања и зависи од вашег одговора на Вимпат. Код већине пацијената, доза одржавања је између 200 мг и 400 мг дневно.
Ваш лекар може прописати другачију дозу ако имате проблема са бубрезима.
Како узимати Вимпат таблете
Вимпат таблете морате прогутати са довољном количином воде (нпр. Чашом). Вимпат можете узимати са или без хране.
Трајање лечења Вимпатом
Вимпат се користи као дуготрајан третман. Морате наставити да узимате Вимпат док вам лекар не каже да прекинете лечење.
Предозирање Шта учинити ако сте узели превише лека Вимпат
Ако сте узели више лека Вимпат него што је требало
Одмах се обратите лекару ако сте узели више лека Вимпат него што је требало. Можда имате вртоглавицу, мучнину, повраћање, срчани удар или проблеме. Не покушавајте да возите.
Ако сте заборавили да узмете Вимпат
Ако сте заборавили да узмете дозу Вимпата, а прошло је неколико сати након што сте је обично узели, узмите Вимпат чим се сетите. Ако је скоро време за следећу дозу (мање од 6 сати), немојте узимати заборављену таблету Узмите следећу таблету Вимпат у уобичајено време. Немојте узети двоструку дозу да бисте надокнадили заборављену дозу.
Ако престанете да узимате Вимпат
Немојте престати узимати Вимпат без консултације са лекаром јер се симптоми могу вратити или погоршати. Ако ваш лекар одлучи да прекине терапију леком Вимпат, он ће вас упутити како да постепено смањите дозу.
Ако имате додатних питања о употреби овог лека, обратите се свом лекару или фармацеуту.
Нежељени ефекти Који су нежељени ефекти лека Вимпат
Као и сви други лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих.
Врло често: могу се јавити у више од 1 на 10 пацијената
- Вртоглавица, главобоља
- Мучнина
- Двоструки вид (диплопија)
Често: могу се јавити код 1 до 10 на 100 пацијената
- Проблеми у одржавању равнотеже, потешкоће у координацији покрета, проблеми са памћењем, поспаност, дрхтавица, потешкоће у размишљању или проналажењу речи, брзи и неконтролисани покрети очију (нистагмус), трнци (парестезија)
- Замагљен вид
- Осећај "вртења" (вртоглавица)
- Повраћање, затвор, вишак гасова у желуцу или цревима, дијареја
- Свраб
- Падови, контузија
- Умор, отежано ходање, неуобичајен умор и слабост (астенија), осећај пијанства
- Депресија
- Забуна
- Смањени додир или осетљивост, потешкоће у артикулисању речи, поремећај пажње
- Звукови у уху, попут зујања или звиждања
- Варење, сува уста
- Раздражљивост
- Грчење мишића
- Осип
- Потешкоће са спавањем
Мање често: могу се јавити код 1 до 10 на 1000 пацијената
- Смањење откуцаја срца
- Поремећај срчане проводљивости
- Пренаглашен осећај благостања
- Алергијска реакција након узимања лека
- Абнормални тестови функције јетре
- Покушај самоубиства
- Мисли о самоубиству или самоповређивању
- Лупање срца и / или брзо или неправилно пулсирање
- Агресија
- Узнемиреност
- Ненормалне мисли и / или губитак контакта са стварношћу
- Озбиљна алергијска реакција која изазива отицање лица, грла, руку, стопала, глежњева или потколеница
- Уртикарија
- Халуцинације (видети и / или чути ствари које нису стварне)
Није познато: учесталост се не може проценити из доступних података
- Озбиљно смањење броја ћелија одређене класе белих крвних зрнаца (агранулоцитоза)
- Озбиљна кожна реакција која може укључивати симптоме сличне грипу, осип на лицу, опсежан осип са повишеном температуром, повећање нивоа ензима јетре уочених у крвним претрагама и повећање врсте белих крвних зрнаца (еозинофилија) и отечених лимфних чворова
- Опсежан осип са жуљевима и љуштењем коже, нарочито око уста, носа, очију и гениталија (Стевенс-Јохнсонов синдром) и тежи облик који изазива љуштење коже на више од 30% површине тела (токсична епидермална некролиза) .
Пријављивање нежељених ефеката
Ако приметите било које нежељено дејство, обратите се свом лекару или фармацеуту.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нежељена дејства директно путем националног система за пријављивање наведеног у Додатку В. Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока ваљаности наведеног на кутији иза „Рок ваљаности“ и на блистеру после „Рок употребе“.
Овај лек не захтева посебне услове складиштења.
Не бацајте никакве лекове у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Састав и фармацеутски облик
Шта Вимпат садржи
Активни састојак је лакозамид.
Једна таблета Вимпат 50 мг садржи 50 мг лакозамида.
Једна Вимпат таблета од 100 мг садржи 100 мг лакозамида.
Једна таблета Вимпат 150 мг садржи 150 мг лакозамида.
Једна таблета Вимпата 200 мг садржи 200 мг лакозамида.
Остали састојци су:
Језгро таблете: микрокристална целулоза, хидроксипропилцелулоза, хидроксипропилцелулоза (ниско супституисана), колоидни анхидровани силицијум диоксид, кросповидон (полиплаздон фармацеутске класе КСЛ-10), магнезијум стеарат
Премаз: поливинил алкохол, полиетилен гликол, талк, титанијум диоксид (Е171), боје *
* Боје су: таблете од 50 мг: црвени гвожђе -оксид (Е172), црни гвожђе -оксид (Е172), индиго кармин (Е132) 100 мг таблете: жути гвожђе -оксид (Е172) Документ је ставила на располагање АИФА 31. 03. 2015. 144 150 мг таблете: жути гвожђе оксид (Е172), црвени гвожђе оксид (Е172), црни гвожђе оксид (Е172) таблете од 200 мг: индиго кармин (Е132)
Опис изгледа Вимпат и садржај паковања
Вимпат 50 мг филмом обложене таблете су ружичасте, овалне са утиснутим „СП“ на једној страни и „50“ на другој.
Вимпат 100 мг филмом обложене таблете су тамно жуте, овалне са угравираним 'СП' на једној страни и '100' на другој страни.
Вимпат 150 мг филмом обложене таблете су боје лососа, овалне са утиснутим „СП“ на једној страни и „150“ на другој.
Вимпат 200 мг филмом обложене таблете су плаве, овалне са утиснутим „СП“ на једној страни и „200“ на другој.
Пакет за почетак терапије садржи 56 филм таблета, подељених у 4 паковања:
- Паковање са ознаком „Недеља 1“ садржи 14 таблета од 50 мг,
- Паковање са ознаком „2. недеља“ садржи 14 таблета од 100 мг,
- Паковање са ознаком „Недеља 3“ садржи 14 таблета од 150 мг,
- Паковање са ознаком 'Недеља 4' садржи 14 таблета од 200 мг.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ВИМПАТ 50 МГ ТАБЛЕТЕ ОБЛОЖЕНЕ ФИЛМОМ
02.0 КВАЛИТАТИВНИ И КОЛИЧИНСКИ САСТАВ
Свака филмом обложена таблета садржи 50 мг лакозамида.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Филмом обложена таблета.
Ружичасте, овалне, филмом обложене таблете са утиснутим словом "СП" на једној страни и "50" утиснутом на другој страни таблете.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Вимпат је индикован као помоћна терапија у лечењу парцијалних напада са или без секундарне генерализације код одраслих и адолесцената (16-18 година) са епилепсијом.
04.2 Дозирање и начин примене
Дозирање
Лакозамид се мора узимати два пута дневно (обично једном ујутру и једном увече). Препоручена почетна доза је 50 мг два пута дневно, коју треба повећати на почетну терапијску дозу од 100 мг два пута дневно након једне недеље. Третман лакозамидом се такође може започети једнократном учитавајућом дозом од 200 мг, након чега следи приближно 12 сати касније дозом одржавања од 100 мг два пута дневно (200 мг / дан). Оптерећујућа доза се може користити за започињање лечења пацијената у оним ситуацијама у којима лекар утврди да се мора обезбедити брзо постизање равнотежне концентрације лакозамида у плазми и терапеутски ефекат. Ово треба применити под лекарским надзором узимајући у обзир потенцијално повећање инциденце нежељених реакција централног нервног система (видети одељак 4.8). Примена оптерећујуће дозе није проучавана у акутним стањима као што је епилептични статус.
Доза одржавања може се додатно повећати за 50 мг два пута дневно сваке недеље у зависности од клиничког одговора и подношљивости, до максималне препоручене дозе од 400 мг / дан (200 мг два пута дневно). Лакозамид се може узимати са или без хране.
На основу тренутне клиничке праксе, у случају да се мора прекинути употреба лакозамида, препоручује се то поступно (нпр. Смањивање дневне дозе за 200 мг сваке недеље).
Посебне популације
Старији људи (старији од 65 година)
Код старијих пацијената није потребно смањење дозе. Искуство са лакозамидом код старијих пацијената са епилепсијом је ограничено. Код старијих пацијената треба узети у обзир смањење бубрежног клиренса повезаног са узрастом са повећањем нивоа АУЦ (видети следећи одељак "Оштећење бубрега" и одељак 5.2).
Инсуфицијенција бубрега
Није потребно прилагођавање дозе код пацијената са благим и умереним оштећењем бубрега (ЦЛЦР> 30 мл / мин). Код пацијената са благим или умереним оштећењем бубрега, може се размотрити учитавајућа доза од 200 мг, али накнадну титрацију дозе (> 200 мг дневно) треба извршити са опрезом.
Код пацијената са тешком бубрежном инсуфицијенцијом (ЦЛЦР ≤30 мл / мин) и код пацијената са терминалном бубрежном инсуфицијенцијом, препоручује се максимална доза одржавања од 250 мг / дан. Код ових пацијената титрацију дозе треба вршити са опрезом. Ако је назначена учитавајућа доза, треба користити почетну дозу од 100 мг, након које следи режим од 50 мг два пута дневно током прве недеље. Код пацијената којима је потребна хемодијализа, препоручује се додатна доза, до 50% појединачне дозе која се користи за постизање дневне дозе, на крају сваке дијализе. Лечење пацијената са крајњим стадијумом бубрежне инсуфицијенције треба спровести опрезно, јер постоји ограничено клиничко искуство и постоји могућност накупљања метаболита (без познате фармаколошке активности).
Хепатична инсуфицијенција
Није потребно прилагођавање дозе код пацијената са благим до умереним оштећењем јетре.
Титрацију код ових пацијената треба вршити са опрезом, узимајући у обзир "могућу истовремену бубрежну инсуфицијенцију. Може се размотрити оптерећујућа доза од 200 мг, али накнадну титрацију дозе (> 200 мг дневно) треба извршити с опрезом. Фармакокинетика лакозамида нису испитиване код пацијената са тешким оштећењем јетре (видети одељак 5.2).
Педијатријска популација
Безбедност и ефикасност лакозамида код деце млађе од 16 година још нису утврђени. Нема доступних података.
Начин примене
Лацосамиде филмом обложене таблете су за оралну примену. Лакозамид се може узимати са или без хране.
04.3 Контраиндикације
Преосетљивост на активну супстанцу или било коју помоћну супстанцу наведену у одељку 6.1.
Већ постојећи атриовентрикуларни (АВ) блок другог или трећег степена.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Идеје о самоубиству и понашање
Пријављени су случајеви суицидалних мисли и понашања код пацијената који су лечени антиепилептичким лековима према различитим индикацијама. Мета-анализа рандомизираних, плацебом контролираних клиничких испитивања проведена с антиепилептичким лијековима такођер је открила незнатно повећан ризик од суицидалних мисли и понашања. Механизам овог ризика није познат, а доступни подаци не искључују могућност повећаног ризика са лакозамидом. Због тога пацијенте треба пратити ради откривања знакова суицидалних идеја и понашања и размотрити одговарајуће лечење. Пацијенте (и неговатеље) треба саветовати да се консултују са својим лекаром ако се појаве знаци суицидалних мисли или понашања (видети одељак 4.8).
Ритам и срчана проводљивост
Продужење ПР интервала примећено је током клиничких испитивања са лакозамидом.Лакозамид треба давати са опрезом код пацијената са већ постојећим поремећајима срчане проводљивости, као и код субјеката са тешким срчаним обољењима, попут историје инфаркта миокарда или срчане инсуфицијенције. Лакозамид треба примењивати са опрезом, посебно код старијих пацијената који могу имати повећан ризик од срчаних обољења или када се лакозамид користи у комбинацији са производима за које је познато да продужавају ПР интервал.
У постмаркетиншком искуству забележен је АВ блок другог степена или виши. У плацебо контролисаним клиничким испитивањима са лакозамидом код пацијената са епилепсијом, није пријављена фибрилација атрија или треперење; међутим, оба су пријављена у студијама о епилепсији. маркетиншко искуство (видети одељак 4.8).
Пацијенте треба обавестити о симптомима АВ блока другог степена или вишем (нпр. Успорен или неправилан пулс, осећај ошамућености и несвестице) и симптомима атријалне фибрилације и треперења (нпр. Палпитације, убрзан или неправилан пулс, отежано дисање). Пацијенте треба саветовати да се обрате свом лекару ако се јави било који од ових симптома.
Вртоглавица
Лечење лакозамидом је повезано са вртоглавицом, што може повећати ризик од случајних повреда или падова. Пацијенте стога треба саветовати да буду опрезни док не буду упознати са потенцијалним ефектима лека (видети одељак 4.8).
04.5 Интеракције са другим лековима и други облици интеракција
Лакозамид треба давати са опрезом код пацијената који се лече лековима за које се зна да продужавају ПР интервал (нпр. Карбамазепин, ламотригин, прегабалин), као и код пацијената лечених антиаритмицима класе И. Међутим, анализе подгрупа у студијама нису показале израженије продужење ПР интервала код пацијената који примају истовремени третман карбамазепином или ламотригином.
Подаци ин витро
Експериментални подаци указују на низак потенцијал интеракције лакозамида. Студије су спроведене ин витро указују да лакозамид не индукује ЦИП1А2, 2Б6 и 2Ц9 цитокроме или инхибицију ЦИП1А1, 1А2, 2А6, 2Б6, 2Ц8, 2Ц9, 2Д6 и 2Е1 у концентрацијама у плазми које су примећене у клиничким студијама. Спроведена студија ин витро показала да се лакозамид не транспортује П-гликопротеином у цревима. Подаци ин витро показују да су цитокроми ЦИП2Ц9, ЦИП2Ц19 и ЦИП3А4 способни да катализују стварање О-десметил метаболита.
Подаци ин виво
Лакозамид не инхибира нити индукује цитокроме ЦИП2Ц19 и 3А4 на клинички релевантан начин. Лакозамид није утицао на АУЦ мидазолама (метаболише се помоћу цитокрома ЦИП3А4, лакозамид се даје у дози од 200 мг два пута дневно), али је Цмак мидазолама благо повећан (30%). Лакозамид није утицао на фармакокинетику мидазолама. омепразол (метаболише се цитокромима ЦИП2Ц19 и 3А4, лакозамид се примењује у дози од 300 мг два пута дневно). Инхибитор ЦИП2Ц19 омепразол (40 мг једном дневно) није резултирао клинички значајном променом изложености лакозамиду. Због тога је мало вероватно да ће умерени инхибитори ЦИП2Ц19 утицати на системску изложеност лакозамиду на клинички релевантан начин. Препоручује се опрез при истовременој терапији са снажним инхибиторима ЦИП2Ц9 (нпр. Флуконазол) и ЦИП3А4 (нпр. Итраконазол, кетоконазол, ритонавир, кларитромицин), што може довести до повећања системске изложености лакозамиду. Такве интеракције нису успостављене ин виво, али су могући на основу података ин витро.
Снажни индуктори ензима, попут рифампицина или кантариона (Хиперицум перфоратум), могу умерено смањити системску изложеност лакозамиду. Сходно томе, сваки третман овим индукторима ензима треба започети или прекинути с опрезом.
Антиепилептици
У студијама интеракције, лакозамид није значајно утицао на плазма концентрације карбамазепина и валпроичне киселине. Нивои лакозамида у плазми нису промењени карбамазепином и „валпроичном киселином.“ Фармакокинетичка анализа популације показала је да је истовремена терапија другим антиепилептицима за које је познато да су индуктори ензима (карбамазепин, фенитоин и фенобарбитал, у различитим дозама) смањила укупну системску изложеност лакозамиду 25%.
Орална контрацепција
У студији интеракције није пронађена клинички значајна интеракција између лакозамида и оралних контрацептива етинилестрадиола и левоноргестрела. Концентрација прогестерона није утицала на истовремену примену два лека.
Друго
Студије интеракција су показале да лакозамид нема утицаја на фармакокинетику дигоксина. Не постоји клинички значајна интеракција између лакозамида и метформина. Иако нема података о интеракцији лакозамида са алкохолом, фармакодинамички ефекат се не може искључити.
Лакозамид има ниско везивање за протеине плазме (мање од 15%). Сходно томе, сматра се да је мало вероватно присуство клинички значајних интеракција са другим лековима конкуренцијом за места везивања за протеине.
04.6 Трудноћа и дојење
Трудноћа
Ризик повезан са епилепсијом и антиепилептичким лековима уопште
Показано је да је код потомака жена лечених антиепилептичким лековима преваленција малформација два до три пута већа од оне од приближно 3% у општој популацији. У леченој популацији примећен је пораст малформација код жена које су на политерапији; међутим, није било могуће схватити у којој мери су те малформације узроковане лечењем и / или болешћу. Штавише, ефикасну антиепилептичку терапију не треба прекидати, јер погоршање болести може бити штетно и за мајку и за фетус.
Ризик повезан са лакозамидом
Нема одговарајућих података о употреби лакозамида у трудница. Студије на животињама не показују тератогене ефекте на пацовима или зечевима, док су ембриотоксични ефекти примећени на пацовима и зечевима након примене токсичних доза за мајку (видети одељак 5.3). ризик за људе је непознат. Лакозамид се не сме примењивати током трудноће осим ако то није неопходно (ако корист за мајку очигледно премашује потенцијални ризик за фетус). Ако жена планира трудноћу, употребу овог лека треба пажљиво применити поново процењује.
Време храњења
Није познато да ли се лакозамид излучује у мајчино млеко код људи. Студије на животињама су показале да се лакозамид излучује у мајчино млеко. Због предострожности, дојење треба прекинути током терапије лакозамидом.
Плодност
Код пацова, нису примећене никакве нежељене реакције на плодност или репродукцију мушкараца или женки у дозама које су резултирале изложеношћу плазми (АУЦ) до приближно 2 пута већом од АУЦ у плазми човека након примене највеће препоручене дозе за људе (МРХД).
04.7 Утицај на способност управљања возилима и машинама
Лакозамид има "благи до умерен утицај на способност управљања возилима и рада са машинама. Лечење лакозамидом је повезано са вртоглавицом и замагљеним видом. Због тога пацијенти не треба да возе или управљају потенцијално опасним машинама док се не упознају са ефектима лакозамида. на њихову способност обављања ових активности.
04.8 Нежељени ефекти
Сажетак сигурносног профила
На основу мета-анализе плацебо контролисаних клиничких испитивања на 1308 пацијената са парцијалним нападима, 61,9% пацијената рандомизованих у групу лакозамида и 35,2% пацијената рандомизираних у плацебо групу пријавило је најмање једну нежељену реакцију. Најчешће пријављене нежељене реакције након третмана лакозамидом биле су вртоглавица, главобоља, мучнина и диплопија. Интензитет ових реакција је обично био благ до умерен. Неки су зависили од дозе и побољшали су се са смањењем дозе. Учесталост и озбиљност нежељених реакција које утичу на централни нервни систем (ЦНС) и гастроинтестинални (ГИ) тракт обично су се временом смањивале.У свим контролисаним студијама проценат пацијената који су прекинули терапију због нежељених реакција био је 12,2% за пацијенте рандомизиране на у групи лакозамида и 1,6% код пацијената рандомизованих у плацебо групу. Најчешћа нежељена реакција која је довела до прекида терапије била је вртоглавица. Учесталост нежељених реакција централног нервног система, попут вртоглавице, може бити већа након пуњења.
Табела нежељених реакција
У следећој табели су наведене учесталости нежељених реакција пријављених у плацебо контролисаним клиничким испитивањима (са стопом инциденције ≥1% у групи са лакозамидом и које су
> 1% у поређењу са плацебом) и у постмаркетиншком искуству. Учесталости су дефинисане на следећи начин: врло често (≥1 / 10); често (≥1 / 100 до
потенцијално важне нежељене реакције на лекове пријављене у клиничким испитивањима са стопом инциденције која не одговара горе наведеним критеријумима.
нежељене реакције пријављене у постмаркетиншком искуству.
Опис одабраних нежељених реакција
Употреба лакозамида повезана је са дозно зависним продужавањем ПР интервала. Могуће су нежељене реакције (нпр. Атриовентрикуларни блок, синкопа, брадикардија) повезане са овим продужењем. У клиничким студијама код пацијената са епилепсијом, учесталост пријављених атриовентрикуларних (АВ) блокова првог степена је ретка, 0,7%, 0%, 0,5% и 0% у групама лакозамида 200 мг, 400 мг, 600 мг или плацеба, респективно . У овим студијама нису примећене епизоде другог степена или великог АВ блока. Међутим, у постмаркетиншком периоду забележени су случајеви АВ блокаде другог и трећег степена повезани са третманом лакозамидом. Учесталост синкопе у клиничким испитивањима је неуобичајена и не разликује се код пацијената са епилепсијом из групе лакозамида (0,1%) и плацебо група (0,3%). У краткотрајним клиничким испитивањима није забележена атријална фибрилација или лепршање; међутим, обоје је пријављено у отвореним клиничким испитивањима код пацијената са епилепсијом и у искуству након третмана. маркетинг.
Абнормалности у лабораторијским тестовима
Одступања у испитивању функције јетре примећена су у контролисаним клиничким испитивањима са лакозамидом код одраслих пацијената са парцијалним нападима који су истовремено узимали 1 до 3 антиепилептичка лека. Повишење АЛТ до ≥3 к ГГН (горња граница нормале) догодило се код 0,7% (7/935) пацијената лечених Вимпатом и 0% (0/356) пацијената лечених плацебом.
Реакције преосјетљивости на више органа
Пријављене су више реакција преосетљивости органа код пацијената лечених неким антиепилептичким лековима. Ове реакције се јављају на променљив начин, али се обично јављају са грозницом и осипом и могу бити повезане са укључивањем различитих органских система. Ретко су пријављени потенцијални случајеви са лакозамидом; ако се сумња на реакцију преосјетљивости на више органа, лијечење лакозамидом треба прекинути.
Педијатријска популација
Претпоставља се да су учесталост, врста и интензитет нежељених реакција код адолесцената у доби од 16 до 18 година исти као и код одраслих.Безбедност лакозамида код деце млађе од 16 година још није утврђена, нема података.
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика лека. Од здравствених радника се тражи да пријаве све сумње на нежељене реакције путем националног система за пријављивање. У „Анексу В .
04.9 Предозирање
Клинички подаци о предозирању лакозамидом код људи су ограничени.
Симптоми
Клинички симптоми (вртоглавица и мучнина) уочени након уноса од 1200 мг / дан претежно су утицали на централни нервни систем и гастроинтестинални систем и решили су се прилагођавањем дозе. Највећа превелика доза лакозамида пријављена у клиничкој историји износи 12 г, узета заједно са токсичне дозе разних других антиепилептика Субјект, који је прво ушао у кому, касније се потпуно опоравио без трајног оштећења.
Менаџмент
Не постоји специфичан противотров за предозирање лакозамидом. Лечење предозирања треба да укључи опште мере подршке и, ако је потребно, може укључити и хемодијализу (видети одељак 5.2).
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: антиепилептици, други антиепилептици, АТЦ ознака: Н03АКС18
Механизам дејства
Активни састојак, лакозамид (Р-2-ацетамидо-Н-бензил-3-метоксипропионамид) је аминокиселина којој су додане друге функционалне групе.
Прецизан механизам деловања на који лакозамид испољава антиепилептички ефекат на људе још није у потпуности објашњен. ин витро показали су да лакозамид селективно потенцира спору инактивацију натријумских канала са напоном, што резултира стабилизацијом хиперексцитабилних неуронских мембрана.
Фармакодинамички ефекти
Лакозамид је показао заштитно дејство против нападаја у широком спектру животињских модела парцијалних и примарно генерализованих напада и одложио почетак паљења.У предклиничким студијама лакозамид, у комбинацији са леветирацетамом, карбамазепином, фенитоином, валпроатом, ламотригином, топираматом или габапентин, показао је синергистичке или адитивне антиконвулзивне ефекте.
Клиничка ефикасност и безбедност
Ефикасност Вимпата као додатне терапије у препорученим дозама (200 мг / дан, 400 мг / дан) процењивана је у 3 мултицентрична, рандомизована, плацебом контролисана клиничка испитивања са периодом одржавања од 12 недеља, у којима се користила као додатна терапија, Вимпат се такође показао ефикасним у дози од 600 мг / дан.Ефикасност је била слична оној постигнутој са 400 мг / дан, међутим пацијенти су мање подносили дозу због нежељених реакција које утичу на ЦНС и гастроинтестиналног тракта. Због тога се не препоручује доза од 600 мг / дан. Максимална препоручена доза је 400 мг / дан. Ове студије су обухватиле укупно 1308 пацијената са просечном историјом од 23 године са парцијалним нападима, и осмишљене су за процену ефикасности и безбедности лакозамида, у комбинацији са 1-3 антиепилептика, код пацијената са парцијалним нападима са или без секундарних напада генерализација није добро контролисана терапијом. Све у свему, проценат пацијената који су постигли смањење учесталости напада од 50% био је 23%, 34% и 40% за плацебо, лакозамид 200 мг / дан и лакозамид 400 мг / дан.
Нема довољно података о прекиду истовремених антиепилептичких терапија како би се могла користити само лакозамид.
Фармакокинетика и безбедност појединачне интравенозне учитавајуће дозе лакозамида утврђене су у отвореној мултицентричној студији осмишљеној за процену безбедности и подношљивости брзог почетка лакозамида применом појединачне интравенске пуњења (укључујући дозу од 200 мг), након чега следи давање две дневне оралне дозе (еквивалентно интравенозној дози) као додатна терапија код одраслих од 16 до 60 година са парцијалним нападима.
05.2 "Фармакокинетичка својства
Апсорпција
Лакозамид се брзо и потпуно апсорбује након оралне примене. Орална биорасположивост таблета лакозамида је близу 100%. Након оралне примене, концентрација непромењеног лакозамида у плазми брзо расте и достиже Цмак отприлике 0,5 до 4 сата након дозирања.Вимпат таблете и Вимпат орални сируп су биоеквивалентни. Храна не утиче на брзину и степен апсорпције.
Дистрибуција
Волумен дистрибуције је приближно 0,6 Л / кг. Везивање лакозамида за протеине плазме је мање од 15%.
Биотрансформација
95% примењене дозе се излучује урином у облику лека и метаболита. Метаболизам лакозамида није у потпуности окарактерисан.
Главна једињења која се излучују урином су непромењени лакозамид (приближно 40% дозе) и његов О-десметил метаболит (мање од 30%).
Поларна фракција за коју се претпоставља да је дериват серина је пронађена у урину приближно 20%, али је откривена у малим количинама (0-2%) у плазми неких испитаника. У урину су пронађене мале количине додатних метаболита (0,5-2%).
Подаци ин витро показују да су цитокроми ЦИП2Ц9, ЦИП2Ц19 и ЦИП3А4 способни да катализују стварање О-десметил метаболита, међутим нема потврде ин виво главног укљученог изоензима. Није било клинички значајних разлика у "изложености лакозамиду када се упореде његова фармакокинетика код субјеката који су дефинисани као" екстензивни метаболизатори "(са функционалним ЦИП2Ц19) и" лоши метаболизатори "(у одсуству функционалног ЦИП2Ц19). Осим тога, студија интеракције са омепразол (инхибитор ЦИП2Ц19) није показао клинички значајне промене у концентрацији лакозамида у плазми, што указује да је овај пут од мале важности. Плазма концентрација О-десметил-лакозамида је приближно 15% концентрације лакозамида у плазми метаболит нема познату фармаколошку активност.
Елиминација
Главни путеви елиминације лакозамида из системске циркулације су бубрежно излучивање и биотрансформација. Након оралне и интравенозне примене радиоактивно обележеног лакозамида, отприлике 95 % примењене радиоактивности је пронађено у урину, а мање од 0,5 % у фецесу. живот непромењеног лека је приближно 13 сати. Фармакокинетика зависи од дозе и константна је током времена, са малом варијабилношћу унутар и међу пацијентима. Након примене два пута дневно, стање равнотеже се постиже током 3 дана. Концентрација у плазми се повећава са фактором акумулације од приближно 2.
Једна доза пуњења од 200 мг доводи до равнотежних концентрација које се могу упоредити са две оралне дозе од 100 мг дневно.
Фармакокинетика код посебних категорија пацијената
Сек
Клиничке студије показују да пол не утиче значајно на концентрацију лакозамида у плазми.
Инсуфицијенција бубрега
АУЦ лакозамида се повећава за приближно 30% код пацијената са благим и умереним оштећењем бубрега и 60% код пацијената са тешким и терминалним оштећењем бубрега које захтевају хемодијализу, у поређењу са здравим субјектима, док Цмак остаје непромењен. Може ефикасно уклонити лакозамид из плазме . Смањење АУЦ лакозамида је приближно 50% након четворочасовне хемодијализе. Због тога се препоручује додатна доза код пацијената на хемодијализи (видети одељак 4.2). Концентрација метаболита О-деметилованог повећана је неколико пута код пацијената са умереном и тешком бубрежном инсуфицијенцијом. У одсуству хемодијализе, ниво метаболита је повећан и континуирано се повећава током 24-часовног узорковања. Није познато да ли је повећана концентрација у плазми метаболит у завршној фази бубрежне инсуфицијенције могао би довести до нежељених догађаја, али није утврђена фармаколошка активност овог метаболита.
Хепатична инсуфицијенција
Испитаници са умереним оштећењем јетре (Цхилд-Пугх Б) имали су веће концентрације лакозамида у плазми (АУЦнорм се повећао за приближно 50%). Већа изложеност делимично је последица смањене бубрежне функције код испитаника. Сматра се да је смањење бубрежног клиренса код ових пацијената одговорно за повећање АУЦ лакозамида за 20%. Фармакокинетика лакозамида није процењивана код пацијената са тешком оштећење јетре (видети одељак 4.2).
Старији људи (старији од 65 година)
У студији на старијим особама оба пола, која је обухватила 4 пацијента старија од 75 година, АУЦ је повећана за приближно 30% код мушкараца и 50% код жена, у поређењу са младим мушким испитаницима. То је делимично због мање телесне тежине Нормализована разлика у телесној тежини је 26, односно 23%, примећено је и повећање варијабилности изложености лековима. У овој студији, бубрежни клиренс лакозамида био је само незнатно смањен код старијих пацијената.
Сматра се да није потребно опште смањење дозе осим ако није индицирано због оштећења бубрежне функције (видети одељак 4.2).
05.3 Предклинички подаци о безбедности
У студијама токсичности, концентрације лакозамида у плазми су биле сличне или нешто веће од оних које су примећене код пацијената, не остављајући додатну маргину за изложеност људи.
Студија аутора фармакологија безбедности у којима је лакозамид даван интравенозно анестезираним псима показало је пролазно повећање ПР интервала и трајања комплекса КРС, као и смањење крвног притиска највероватније због кардиодепресивног ефекта. Ове пролазне промене су почеле у истом распону концентрација. добијено након примена максималне препоручене дозе.Код анестезираних паса и мајмуна Циномолгус, примећена је успорена атрио-вентрикуларна проводљивост, атрио-вентрикуларни блок и атрио-вентрикуларна дисоцијација у дозама у распону од 15-60 мг / кг, примењене интравенозно.
У студијама токсичности при поновљеним дозама, примећене су благе и реверзибилне промене у јетри код пацова почевши од доза 3 пута веће од клиничке разине изложености. Ове промене су укључивале повећање телесне тежине јетре, хипертрофију хепатоцита, повећање серумских ензима јетре и повећање укупног холестерола и триглицерида. Са изузетком хипертрофије хепатоцита, нису откривене даље хистопатолошке промене.
У студијама о репродуктивној и развојној токсичности код глодара и зечева, једини откривени тератогени ефекти били су повећање броја мртворођених и перинаталних смрти, те благо смањење тјелесне тежине и величине јетре у леглу код пацова. Токсичне дозе за мајку које одговарају системској изложености Слично оном у клиничкој пракси. Будући да није било могуће тестирати веће нивое изложености код животиња због токсичности ових доза за мајку, подаци нису довољни за утврђивање ембриофетотоксичног и тератогеног потенцијала лакозамида.
Студије на пацовима показују да лакозамид и / или његови метаболити лако пролазе кроз плаценту.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Језгро таблета:
Микрокристална целулоза
Хидроксипропилцелулоза
Ниско супституисана хидроксипропилцелулоза
Безводни колоидни силицијум диоксид
Цросповидоне (Полипласдон фармацеутског степена КСЛ-10)
Магнезијум стеарат
Облога таблета:
Поливинил алкохол
Полиетилен гликол 3350
Талц
Титанијум диоксид (Е171)
Црвени оксид гвожђа (Е172), црни гвожђе оксид (Е172), индиго кармин (Е132)
06.2 Некомпатибилност
Није битно.
06.3 Период важења
5 година.
06.4 Посебне мере предострожности при складиштењу
Овај лек не захтева посебне услове складиштења.
06.5 Природа непосредног паковања и садржај паковања
Паковања од 14, 56 и 168 филмом обложених таблета у ПВЦ / ПВДЦ блистеру запечаћеном алуминијумском фолијом.
Паковање од 56 к 1 таблета у ПВЦ / ПВДЦ перфорираном блистеру за појединачну дозу, запечаћеном алуминијумском фолијом.
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Нема посебних упутстава за одлагање.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
УЦБ Пхарма СА
Аллее де ла Рецхерцхе 60
Б-1070 Брисел
Белгија
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
ЕУ / 1/08/470 / 001- А.И.Ц. н. 038919015
ЕУ / 1/08/470 / 002- А.И.Ц. н 038919027
ЕУ / 1/08/470 / 003- А.И.Ц. н 038919039
ЕУ/1/08/470/020
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 29. август 2008
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
Јули 2013