Опште и дефиниција
Епигенетика се бави проучавањем свих оних наследних модификација које доводе до варијација у експресији гена, а да при томе не мењају ДНК секвенцу, па самим тим и не изазивају модификације у секвенци нуклеотида који је сачињавају.

Користећи више технички језик, међутим, можемо потврдити да епигенетика проучава све те модификације и све оне промјене које су у стању да мијењају фенотип појединца, а да при томе не мијењају генотип.
Заслуга "скованог израза" епигенетика "приписује се биологу Цонраду Хал Ваддингтону који га је 1942. године дефинисао као" грану биологије која проучава узрочну интеракцију између гена и њихових производа и доводи до фенотипа ".
Објашњено овим појмовима, епигенетика може изгледати прилично сложена; да бисмо боље разумели концепт, могло би бити корисно отворити мале заграде о томе како настаје ДНК и како се одвија транскрипција гена које садржи.
ДНК и транскрипција гена
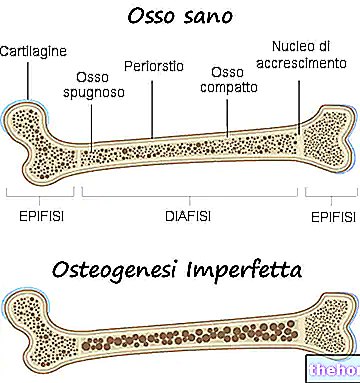
ДНК се налази у језгру ћелије, има структуру двоструке спирале и састоји се од понављајућих јединица, названих нуклеотиди.
Већина ДНК која се налази у нашим ћелијама организована је у одређене подјединице које се називају нуклеозоми.
Нуклеосоми се састоје од централног дела (званог језгро) сачињеног од протеина званих хистони око којих се омотава ДНК.
Скуп ДНК и хистона чини такозвани хроматин.
Транскрипција гена садржаних у ДНК зависи управо од "паковања потоњег" унутар нуклеосома. У ствари, процес транскрипције гена регулишу транскрипциони фактори, посебни протеини који се везују за специфичне регулаторне секвенце присутне на ДНК и који могу активирати или потиснути - у зависности од случаја - специфичне гене.
ДНК са ниским нивоом паковања омогућиће транскрипционим факторима приступ регулаторним секвенцама, док им ДНК са високим нивоом паковања неће омогућити приступ.
Ниво паковања одређују сами хистони и промене које се могу извршити у њиховој хемијској структури.
Прецизније, „ацетилација хистона (тј. Додавање ацетил групе на одређеним местима на аминокиселинама које чине ове протеине) доводи до тога да хроматин претпоставља„ опуштенију “конформацију која омогућава унос транскрипционих фактора, па стога и транскрипцију гена С друге стране, деацетилација уклања ацетилне групе, узрокујући задебљање хроматина и блокирајући тако транскрипцију гена.

Епигенетски сигнали
У светлу до сада реченог, можемо потврдити да, ако епигенетика проучава модификације способне да промене фенотип, али не и генотип појединца, епигенетски сигнал је та модификација која може да промени експресију датог гена , без промене нуклеотидне секвенце.
Сходно томе, можемо потврдити да се ацетилација хистона поменута у претходном пасусу може сматрати епигенетским сигналом; другим речима, то је епигенетска модификација способна да утиче на активност гена (која се може транскрибовати или мање) без промене његову структуру.
Друга врста епигенетске модификације састоји се од реакције метилације, како ДНК, тако и самих хистона.
На пример, метилација (тј. Додавање метил групе) ДНК на месту промотера смањује транскрипцију гена, чија активација је регулисана самим тим месту промотора. У ствари, место промотера је специфична секвенца ДНК која се налази узводно од гена, чији је задатак омогућити почетак транскрипције истих. Додавање метил групе на овом месту стога изазива неку врсту оптерећења које омета транскрипцију гена.
Ипак, други примери тренутно познатих епигенетских модификација су фосфорилација и убиквитинација.
Сви ови процеси који укључују ДНК и хистонске протеине (али не само) су регулисани другим протеинима који се синтетишу након транскрипције других гена, чија се активност, пак, може променити.
У сваком случају, најзанимљивија посебност епигенетске модификације је та што се може догодити као одговор на вањске подражаје из околине који се тичу, управо, околине која нас окружује, нашег начина живота (укључујући исхрану) и нашег здравственог стања.
У извесном смислу, епигенетска модификација се може схватити као адаптивна промена којом управљају ћелије.
Ове промене могу бити физиолошке, као што се дешава у случају неурона који усвајају епигенетске механизме за учење и памћење, али могу бити и патолошке, као што се дешава, на пример, у случају менталних поремећаја или тумора.
Друге важне карактеристике епигенетских модификација су реверзибилност и наследност. У ствари, ове модификације се могу преносити са једне ћелије на другу, мада и даље могу проћи кроз даље промене, увек као одговор на спољне стимулусе.
Коначно, епигенетске модификације могу се десити у различитим фазама живота, а не само на ембрионалном нивоу (када се ћелије разликују) како се некад веровало, већ и када је организам већ развијен.
Терапеутски аспекти
Откриће епигенетике и епигенетских модификација може се широко користити у терапијском пољу за потенцијално лечење различитих врста патологија, укључујући и оне неопластичног типа (тумори).
У ствари, као што је поменуто, епигенетске модификације такође могу бити патолошке природе; стога се у овим случајевима могу дефинисати као праве аномалије.
Истраживачи су стога претпоставили да, ако на ове промене могу утицати спољни надражаји и могу се манифестовати и даље мењати током живота организма, онда је могуће интервенисати на њих помоћу специфичних молекула са циљем да се ситуација врати на нормални услови.од нормалности. То је нешто што се не може учинити (бар још не) када узрок болести лежи у правој генетској мутацији.
Да бисмо боље разумели овај концепт, можемо узети као пример употребу истраживања коју су истраживачи искористили у познавању епигенетике у области антиканцерогених терапија.