Активни састојци: Ритуксимаб
МабТхера 100 мг концентрат за раствор за инфузију
Улошци за пакет Мабтхера доступни су за величине паковања:- МабТхера 100 мг концентрат за раствор за инфузију
- МабТхера 500 мг концентрат за раствор за инфузију
- МабТхера 1400 мг раствор за поткожну ињекцију
Индикације Зашто се користи Мабтхера? За шта је то?
Шта је МабТхера
МабТхера садржи активну супстанцу „ритуксимаб“, врсту протеина звану „моноклонско антитело“ које се веже за површину одређених белих крвних зрнаца, званих лимфоцити Б. Када се ритуксимаб веже за површину ових ћелија, он их убија.
За шта се користи МабТхера
МабТхера се може користити за лечење многих различитих стања код одраслих. Ваш лекар може прописати МабТхеру за лечење:
а) Не-Ходгкинов лимфом
Не-Ходгкинов лимфом је болест лимфног ткива (део имунолошког система) која укључује Б лимфоците, посебну врсту белих крвних зрнаца.
МабТхера се може давати као монотерапија (сама) или са другим лековима који се заједнички називају „хемотерапија“.
Код пацијената чији се третман показао ефикасним, МабТхера се може користити као терапија одржавања 2 године након завршетка почетног лечења.
б) Хронична лимфна леукемија
Хронична лимфоцитна леукемија (ЦЛЛ) је најчешћи облик леукемије одраслих. ЦЛЛ укључује одређени лимфоцит, Б ћелију, која потиче из коштане сржи и сазрева у лимфним чворовима. Пацијенти са ЦЛЛ имају превише абнормалних лимфоцита, који постају они акумулирају се углавном у коштаној сржи и крви.Пролиферација ових абнормалних лимфоцита Б узрок је симптома које можете имати.МабТхера у комбинацији са хемотерапијом уништава ове ћелије које се постепено уклањају из тела биолошким процесима.
ц) Реуматоидни артритис
МабТхера се користи за лечење реуматоидног артритиса.Реуматоидни артритис је болест која погађа зглобове. Б лимфоцити су одговорни за неке од симптома које имате. МабТхера се користи за лечење реуматоидног артритиса код људи који су пробали друге лекове, али су престали да раде, нису радили довољно добро или су изазвали нежељене ефекте. МабТхера се обично узима са другим леком који се зове метотрексат. МабТхера успорава оштећења зглобова изазвана реуматоидним артритисом и повећава способност обављања нормалних дневних активности.
Најбољи одговор на МабТхеру виђен је код оних који су имали позитиван тест крви на реуматоидни фактор (РФ) и / или антициклични цитрулинирани пептид (анти-ЦЦП). Оба теста су обично позитивна код реуматоидног артритиса и помажу у потврђивању дијагнозе.
г) Грануломатоза са полиангиитисом и микроскопским полиангиитисом
МабТхера се користи за индукцију ремисије грануломатозе са полиангиитисом (званично названим Вегенерова болест) или микроскопским полиангиитисом, заједно са глукокортикоидима. Грануломатоза са полиангиитисом и микроскопски полиангиитис су два облика запаљења крвних судова која углавном погађају плућа и бубреге, али могу утицати и на друге органе.Б -лимфоцити су укључени у узрок ових стања.
Контраиндикације Када се Мабтхера не сме користити
Немојте узимати МабТхеру:
- ако сте алергични на ритуксимаб, друге протеине сличне ритуксимабу или било који други састојак овог лека (наведен у одељку 6);
- ако тренутно имате „озбиљну активну инфекцију;
- ако је ваш имунолошки систем слаб;
- ако имате тешку срчану инсуфицијенцију или тешку неконтролисану срчану болест и имате реуматоидни артритис, грануломатозу са полиангиитисом или микроскопски полиангиитис.
Немојте узимати МабТхеру ако се било шта од горе наведеног односи на вас. Ако нисте сигурни, разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што добијете МабТхеру.
Предострожности при употреби Шта треба да знате пре него што узмете лек Мабтхера
Разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што добијете МабТхеру:
- ако сте раније имали инфекцију хепатитисом или је имате сада, јер је у малом броју случајева МабТхера могла изазвати реактивацију хепатитиса Б, што у врло ретким случајевима може бити фатално. Пацијенте са историјом инфекције хепатитисом Б лекар ће помно надгледати ради откривања било каквих знакова ове инфекције;
- ако сте икада имали срчане проблеме (као што су ангина, палпитације или затајење срца) или сте имали проблема са дисањем.
Ако се било шта од горе наведеног односи на вас (или ако нисте сигурни), разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што добијете МабТхеру. Ваш лекар ће можда морати да вам обрати посебну пажњу док узимате МабТхеру.
Ако имате реуматоидни артритис, грануломатозу са полиангиитисом или микроскопски полиангиитис, разговарајте са својим лекаром
- ако мислите да имате инфекцију, чак и благу, попут прехладе.Ћелије на које утиче МабТхера користе се за борбу против инфекција и морате сачекати да се инфекција излечи пре него што узмете МабТхеру.Такође, реците свом лекару ако сте у прошлости имали много инфекција или патите од тешких инфекција;
- ако мислите да су вам потребне вакцинације у блиској будућности, укључујући вакцине потребне за путовање у друге земље. Неке вакцине не треба давати истовремено са МабТхером или у месецима након узимања МабТхере. Ваш лекар ће размотрити да ли можете да се вакцинишете пре него што узмете МабТхеру.
Деца и адолесценти
Разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што дате овај лек ако сте ви или ваше дете млађе од 18 година, јер тренутно нема много информација о употреби лека МабТхера код деце и адолесцената.
Интеракције Који лекови или храна могу променити дејство лека Мабтхера
Обавестите свог лекара, фармацеута или медицинску сестру ако узимате, недавно сте узимали или бисте могли узети било које друге лекове, укључујући лекове без рецепта и лекове на биљној бази, јер МабТхера може утицати на начин на који неки лекови делују и обрнуто.
Посебно реците свом лекару:
- ако узимате лекове за лечење хипертензије. Можда ће бити затражено да престанете са узимањем ових лекова 12 сати пре узимања МабТхере, јер неки људи доживе пад крвног притиска током узимања МабТхере;
- ако сте у прошлости узимали лекове који утичу на имунолошки систем - као што су хемотерапија или имуносупресивни лекови.
Ако се нешто од горе наведеног односи на вас (или ако нисте сигурни), разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што добијете МабТхеру.
Упозорења Важно је знати да:
Трудноћа, дојење и плодност
Обавестите свог лекара или медицинску сестру ако сте трудни, сумњате или планирате трудноћу, јер МабТхера може проћи кроз плаценту и утицати на бебу.
Ако постоји могућност да затрудните, ви и ваш партнер ћете морати да користите ефикасну контрацепцију током терапије МабТхером и у року од 12 месеци од примања последњег третмана МабТхером.
МабТхера може проћи у мајчино млеко, тако да не смете дојити током терапије овим леком, нити 12 месеци након што сте примили последњи третман са МабТхером.
Вожња и управљање машинама
Није познато да ли МабТхера утиче на способност управљања возилима и рада са алатима или машинама.
Дозирање и начин употребе Како користити Мабтхера: Дозирање
Администрација
МабТхеру ће вам дати лекар или медицинска сестра са искуством у употреби овог лека. Они ће вас помно пратити током примене овог лека како би открили све нежељене ефекте.
МабТхера ће се увек давати као кап по кап инфузија у вену (интравенозна инфузија).
Лекови који се дају пре сваке инфузије МабТхере
Пре инфузије МабТхере ћете добити друге лекове (премедикација) како бисте избегли или смањили појаву могућих нежељених ефеката.
Колико и колико често ћете примати терапију
а) Ако се лечите од не-Ходгкиновог лимфома
- Ако вам се даје само МабТхера
МабТхера ће вам се давати једном недељно током 4 недеље. Могући су поновљени курсеви лечења МабТхером.
- Ако вам се МабТхера даје у комбинацији са хемотерапијом
МабТхеру ћете примити истог дана када добијете хемотерапију; њихова администрација се генерално одвија сваке 3 недеље највише 8 пута
- Ако добро реагујете на лечење, МабТхера вам се може дати као терапија одржавања свака 2 до 3 месеца током две године. На основу вашег одговора на лек, ваш лекар може да промени овај режим примене.
б) Ако се лечите од хроничне лимфоцитне леукемије
Ако се лечите МабТхером у комбинацији са хемотерапијом, примаћете инфузије МабТхере првог дана циклуса 1, затим првог дана сваког циклуса укупно 6 циклуса. Сваки циклус траје 28 дана. Хемотерапију треба дати након инфузије МабТхере. Ваш лекар ће одлучити да ли треба да примате истовремену супортивну терапију.
ц) Ако се лечите од реуматоидног артритиса
Сваки циклус лечења састоји се од две одвојене инфузије, које се примењују у размаку од 2 недеље. Могући су поновљени курсеви лечења МабТхером. На основу знакова и симптома ваше болести, ваш лекар ће одлучити када ће вам дати додатне курсеве. То би се могло догодити за неколико месеци.
д) Ако се лечите од грануломатозе са полиангиитисом или микроскопским полиангиитисом
Лечење МабТхером укључује четири одвојене инфузије које се дају у недељним интервалима. Кортикостероиди ће се дати ињекцијом пре почетка терапије леком МабТхера. Ваш лекар може у било које време започети оралну примену кортикостероида ради лечења вашег стања.
Ако имате додатних питања о употреби овог лека, питајте свог лекара, фармацеута или медицинску сестру.
Нежељени ефекти Који су нежељени ефекти лека Мабтхера
Као и сви лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих.
Већина нуспојава су благе или умерене, али у неким случајевима могу бити озбиљне и захтевају лечење. Ретко су неке од ових реакција биле фаталне.
Реакције инфузије
Током или унутар прва 2 сата након прве инфузије, можете развити грозницу, зимицу и тремор. Мање често, неки пацијенти могу имати болове на месту инфузије, стварање пликова, свраб коже, малаксалост, умор, главобољу, отежано дисање, отечени језик или грло, иритацију или цурење из носа, повраћање, осећај топлоте или топлоте. Палпитације, срчани удар или смањење у броју тромбоцита. Ако имате срчану болест или ангину, ове реакције се могу погоршати. Ако осетите било који од ових симптома, одмах реците особи која вам даје инфузију, јер ће брзину инфузије можда требати успорити или прекинути. Можда ће бити потребно додатно лечење, на пример са антихистамином или парацетамолом. Када се ови симптоми повуку или побољшати, инфузија се може наставити. Мање је вероватно да ће се ове реакције јавити након друге инфузије. Ваш лекар може одлучити да прекине лечење леком МабТхера ако су ове реакције озбиљне.
Инфекције
Одмах обавестите свог лекара ако имате било какве знакове инфекције, укључујући:
- грозница, кашаљ, грлобоља, пецкање при мокрењу, осећај слабости или опћенито лоше стање;
- губитак памћења, проблематично размишљање, потешкоће при ходању или губитак вида - то може бити последица веома ретке „озбиљне инфекције која се показала фаталном (прогресивна мултифокална леукоенцефалопатија или ПМЛ).Током лечења леком МабТхера можете лакше развити инфекције.
- То су често прехладе, али било је случајева упале плућа или инфекција уринарног тракта. Ови услови су наведени на "листи под" Остали нежељени ефекти "испод.
Ако се лечите од реуматоидног артритиса, ове информације ћете пронаћи и у картици са упозорењем за пацијенте коју ће вам дати ваш лекар. Важно је да ову картицу упозорења носите са собом и покажете члану породице или било коме иначе се побрини за њу.
Реакције на кожи
Врло ретко се могу јавити озбиљне кожне реакције са стварањем пликова, које могу бити опасне по живот. Црвенило, често повезано са пликовима, може се појавити на кожи или слузници, попут уста, гениталија или капка, а може бити присутна и грозница. Одмах обавестите свог лекара ако приметите неки од ових симптома.
Остали нежељени ефекти
а) Ако се лечите од не-Ходгкиновог лимфома или хроничне лимфоцитне леукемије
Веома чести нежељени ефекти (могу се јавити у више од 1 на 10 особа):
- бактеријске или вирусне инфекције, бронхитис
- низак број белих крвних зрнаца, са или без температуре, или тромбоцита (крвна зрнца)
- мучнина
- подручја ћелавости на власишту, зимица, главобоља
- снижавање имунолошког система - због смањења количине одређених антитела која се називају „имуноглобулини“ (ИгГ) у крви и помажу телу да се заштити од инфекција.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа):
- инфекције крви (сепса), упала плућа, херпес зостер, прехлада, бронхијална инфекција, гљивичне инфекције, инфекције непознатог порекла, синуситис, хепатитис Б
- низак број црвених крвних зрнаца (анемија), низак број свих крвних зрнаца
- алергијске реакције (преосјетљивост)
- висок ниво шећера у крви, губитак тежине, отицање лица и тела, висок ниво „ензима„ ЛДХ “у крви, низак ниво калцијума у крви
- ненормални осећаји на кожи - као што су утрнулост, трнци, трнци, пецкање, осећај растегнуте коже, смањен осећај додира
- осећај немира, тешкоће са заспањем
- изражено црвенило лица и других подручја коже као последица ширења крвних судова
- вртоглавица или анксиозност
- повећано сузење, проблеми са сузним каналима, упала ока (коњунктивитис)
- непрекидно звоњење у ушима, бол у уху
- срчани проблеми - као што су срчани удар, неправилан или убрзан рад срца
- висок или низак крвни притисак (смањење крвног притиска, посебно када стојите)
- контракција мишића у дисајним путевима која изазива пискање (бронхоспазам), упалу, иритацију у плућима, грлу и синусима, отежано дисање, цурење из носа
- повраћање, пролив, бол у стомаку, иритација грла и уста или чиреви, проблеми са гутањем, затвор, лоша пробава
- поремећаји у исхрани: недовољан унос хране резултира губитком тежине
- кошнице, појачано знојење, ноћно знојење
- мишићни проблеми - попут укочености мишића, болова у зглобовима или мишићима, болова у леђима и врату
- општа слабост, немир или умор, дрхтавица, знаци грипа
- отказивање више органа.
Мање чести нежељени ефекти (могу се јавити у до 1 на 100 људи):
- проблеми са згрушавањем, смањена производња црвених крвних зрнаца и повећано уништавање црвених крвних зрнаца (хемолитичка и апластична анемија), отицање или повећање лимфних чворова
- лоше расположење и губитак интереса или задовољства у обављању активности, нервоза
- проблеми повезани са укусом - као што су промене у осећају укуса
- срчани проблеми - као што су успорен рад срца или бол у грудима (ангина)
- астма, недовољна количина кисеоника која стиже до телесних органа
- надутост стомака.
Веома ретки нежељени ефекти (могу се јавити у до 1 на 10.000 људи):
- краткотрајно повећање количине одређених врста антитела (имуноглобулина - ИгМ) у крви, хемијске промене у крви услед разградње умирућих ћелија рака
- оштећење живаца руку и ногу, парализа лица
- отказивање срца
- упала крвних судова, укључујући и оне који изазивају кожне симптоме
- Респираторна инсуфицијенција
- оштећење цревног зида (перфорација)
- тешки кожни проблеми са стварањем пликова, потенцијално фатални. Црвенило, често повезано са пликовима, може се појавити на кожи или слузници, попут уста, гениталија или капака, а може бити присутна и грозница.
- инсуфицијенција бубрега
- озбиљан губитак вида.
Није познато (учесталост појављивања ових нежељених ефеката није позната):
- тренутно смањење белих крвних зрнаца
- смањење броја тромбоцита убрзо након инфузије - реверзибилно стање, али у ретким случајевима опасно по живот
- губитак слуха, губитак других чула.
б) Ако се лечите од реуматоидног артритиса
Веома чести нежељени ефекти (могу се јавити у више од 1 на 10 особа):
- инфекције попут упале плућа (бактеријске)
- бол при уринирању (инфекција уринарног тракта)
- алергијске реакције које ће се вероватно појавити током инфузије, али се могу јавити и до 24 сата након инфузије
- промене крвног притиска, мучнина, осип, грозница, осећај свраба, цурење или зачепљен нос, кихање, дрхтање, убрзан рад срца и умор
- главобоља
- промене у лабораторијским тестовима које захтева лекар. То укључује смањење количине одређених специфичних протеина у крви (имуноглобулини) који помажу у заштити од инфекције.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа):
- инфекције као што је бронхијална упала (бронхитис)
- осећај бола и ситости иза носа, образа и очију (синуситис), бол у абдомену, повраћање и пролив, отежано дисање
- гљивична инфекција стопала (атлетско стопало)
- висок ниво холестерола у крви
- абнормални осећаји на кожи, као што су утрнулост, пецкање, пецкање или печење, ишијас, мигрена, вртоглавица
- губитак косе
- анксиозност, депресија
- пробавне сметње, дијареја, рефлукс киселине, иритација и / или улцерација грла и уста
- бол у стомаку, леђима, мишићима и / или зглобовима.
Мање чести нежељени ефекти (могу се јавити у до 1 на 100 људи):
- задржавање вишка течности у лицу и телу
- упала, иритација и / или напетост у плућима, грлу, кашаљ
- кожне реакције, укључујући копривњачу, свраб, осип
- алергијске реакције укључујући пискање или отежано дисање, отицање лица и језика, колапс.
Веома ретки нежељени ефекти (могу се јавити у до 1 на 10.000 људи):
- комплекс симптома који се јављају у року од неколико недеља након инфузије МабТхере, укључујући реакције алергијског типа попут осипа, свраба, болних зглобова, отечених лимфних жлезда и грознице
- тешке кожне реакције са стварањем пликова који могу бити опасни по живот. Црвенило, често повезано са пликовима, може се појавити на кожи или слузници, попут уста, гениталија или капка, а може бити присутна и грозница.
Остали ретко пријављени нежељени ефекти лечења МабТхером укључују смањење броја белих крвних зрнаца (неутрофила) који се користе за борбу против инфекција. Неке инфекције могу бити озбиљне (погледајте информације о инфекцијама у овом одељку).
ц) Ако се лечите од грануломатозе са полиангиитисом или од микроскопског полиангиитиса
Веома чести нежељени ефекти (могу се јавити у више од 1 на 10 особа):
- инфекције, као што су инфекције плућа, инфекције уринарног тракта (болно мокрење), прехладе и инфекције херпесом
- алергијске реакције које ће се вероватно појавити током инфузије, али се могу јавити и до 24 сата након инфузије
- пролив
- кашаљ или отежано дисање
- крварење из носа
- повећан крвни притисак
- бол у зглобовима или леђима
- трзање или дрхтање мишића
- врти ми се у глави
- дрхтање (дрхтање, често у рукама)
- поремећаји спавања (несаница)
- отицање шака и глежњева.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа):
- лоше варење
- констипација
- кожни осип, укључујући акне или мрље
- испирање или црвенило коже
- запушен нос
- укоченост мишића или болови у мишићима
- бол у мишићима или шакама или стопалима
- низак број црвених крвних зрнаца (анемија)
- низак број тромбоцита у крви повећава се количина калијума у крви
- промене срчаног ритма или откуцаја срца брже од нормалног.
Веома ретки нежељени ефекти (могу се јавити у до 1 на 10.000 људи):
- тешке кожне реакције са стварањем пликова који могу бити опасни по живот. Црвенило, често повезано са пликовима, може се појавити на кожи или слузници, попут уста, гениталија или капака, а може бити присутна и грозница.
- рецидив претходне инфекције хепатитисом Б.
МабТхера такође може изазвати промене у лабораторијским тестовима које захтева ваш лекар.
Ако узимате МабТхеру у комбинацији са другим лековима, неки од нежељених ефеката које доживите могу бити последица других лекова.
Пријављивање нежељених ефеката
Ако добијете било које нежељено дејство, разговарајте са својим лекаром, фармацеутом или медицинском сестром.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нуспојаве директно путем националног система за пријављивање наведених у Додатку В. Нежељена дејства можете помоћи пружити више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока ваљаности наведеног на кутији иза „Рок употребе“. Рок употребе се односи на последњи дан у месецу.
Чувати у фрижидеру (2 ° Ц - 8 ° Ц). Чувајте контејнер у спољном паковању ради заштите од светлости.
Не бацајте никакве лекове у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Шта МабТхера садржи
- Активна супстанца у МабТхери је ритуксимаб. Бочица садржи 100 мг ритуксимаба (10 мг / мл).
- Помоћни састојци су натријум цитрат, полисорбат 80, натријум хлорид, натријум хидроксид, хлороводонична киселина и вода за ињекције.
Како МабТхера изгледа и садржај паковања
МабТхера је бистра и безбојна отопина, испоручује се као концентрат за раствор за инфузију. Бочице од 10 мл су доступне у паковањима од 2 бочице.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
МАБТХЕРА 100 мг концентрат за раствор за инфузију
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ
Сваки мл садржи 10 мг ритуксимаба.
Свака бочица садржи 100 мг ритуксимаба.
Ритуксимаб је генетски модификовано химерно мишје / хумано моноклонско антитело које се састоји од гликозилираног имуноглобулина са константним регионима хуманог ИгГ1 и секвенцама варијабилних регија лаких ланаца и тешких ланаца.
Антитело се производи употребом суспензијске културе ћелија сисара (јајник кинеског хрчка) и пречишћава се помоћу афинске хроматографије и јонске измене, укључујући специфичне поступке инактивације и уклањања вируса.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Концентрат за раствор за инфузију.
Бистра и безбојна течност.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
МабТхера је индицирана код одраслих због следећих индикација:
Не-Ходгкинов лимфом (НХЛ)
МабТхера је индикована за лечење претходно нелечених пацијената са фоликуларним лимфомом стадијума ИИИ-ИВ у комбинацији са хемотерапијом.
МабТхера терапија одржавања је индикована за лечење пацијената са фоликуларним лимфомом који реагују на индукциону терапију.
Монотерапија МабТхером је индикована за лечење пацијената са фоликуларним лимфомом стадијума ИИИ-ИВ који су хеморезистентни или су у другом или накнадном релапсу након хемотерапије.
МабТхера је индикована за лечење пацијената са ЦД20 позитивним дифузним не-Ходгкиновим лимфомом великих Б ћелија у комбинацији са ЦХОП хемотерапијом (циклофосфамид, доксорубицин, винкристин, преднизолон).
Хронична лимфоцитна леукемија (ЦЛЛ)
МабТхера у комбинацији са хемотерапијом је индикована за лечење пацијената са претходно нездрављеном и релапсном / рефракторном хроничном лимфоцитном леукемијом. Доступни су само ограничени подаци о ефикасности и безбедности за пацијенте који су претходно били лечени моноклонским антителима, укључујући МабТхеру, или за пацијенте који су били отпорни на претходни третман МабТхером плус хемотерапијом.
За више информација погледајте одељак 5.1.
Реуматоидни артритис
МабТхера у комбинацији са метотрексатом је индикована за лечење тешког активног реуматоидног артритиса код одраслих пацијената који су показали "неадекватан одговор или" нетолеранцију на друге антиреуматске лекове који мењају болест (ДМАРД), укључујући један или више инхибитора фактора туморске некрозе (ТНФ).
Показало се да МабТхера смањује брзину напредовања оштећења зглобова према рендгенским снимцима и побољшава физичку функцију када се даје у комбинацији са метотрексатом.
Грануломатоза са полиангиитисом и микроскопским полиангиитисом
МабТхера у комбинацији са глукокортикоидима је индицирана за индукцију ремисије код одраслих пацијената са грануломатозом са (Вегенеровим) полиангиитисом (ГПА) и тешким активним микроскопским полиангиитисом (МПА).
04.2 Дозирање и начин примене
МабТхеру треба примењивати под строгим надзором искусног здравственог радника и у окружењу са непосредном доступношћу опреме за реанимацију (видети одељак 4.4).
Пре сваке примене лека МабТхера увек треба узети премедикацију са антипиретичким лековима и антихистаминицима, на пример парацетамолом и дифенхидрамином.
Код пацијената са не-Ходгкиновим лимфомом и хроничном лимфоцитном леукемијом (ЦЛЛ), треба размотрити премедикацију глукокортикоидима ако се МабТхера не даје у комбинацији са хемотерапијом која садржи глукокортикоиде.
Код пацијената са реуматоидним артритисом, премедикација са 100 мг метилпреднизолона интравенозно треба да се заврши 30 минута пре инфузије МабТхере како би се смањила учесталост и озбиљност реакција повезаних са инфузијом (ИРР).
Код пацијената који болују од грануломатозе са полиангиитисом (Вегенер -овим) или микроскопским полиангиитисом, препоручује се интравенозна примена метилпреднизолона у дози од 1000 мг / дан 1 до 3 дана пре прве инфузије МабТхере (последња доза метилпреднизолона може се применити истог дана као прву инфузију лека МабТхера) Након тога треба да уследи орални преднизон у дози од 1 мг / кг / дан (не треба прекорачити 80 мг / дан и сужавање треба учинити што је брже могуће у зависности од клиничког стања) током и након третмана са МабТхером.
Дозирање
& ЕГРАВЕ; Важно је да проверите етикету лека како бисте били сигурни да се одговарајућа формулација (интравенозна или поткожна) даје пацијенту како је прописано.
Не-Ходгкинов лимфом
Фоликуларни не-Ходгкинов лимфом
Терапија удруживања
Препоручена доза МабТхере у комбинацији са хемотерапијом за индукционо лечење претходно нездрављених или рецидивираних / рефракторних пацијената са фоликуларним лимфомом је 375 мг / м2 телесне површине по циклусу, до 8 циклуса.
МабТхеру треба примењивати првог дана сваког циклуса хемотерапије, након и.в. глукокортикоидну компоненту хемотерапије, ако постоји.
Терапија одржавања
• Претходно необрађен фоликуларни лимфом
Препоручена доза МабТхере која се користи као третман одржавања за претходно нелечене пацијенте са фоликуларним лимфомом који су одговорили на индукциони третман је: 375 мг / м2 телесне површине једном у два месеца (почевши од 2 месеца након последње дозе терапије). Индукција) до болести прогресију или за период од највише две године.
• Релаксирани / рефракторни фоликуларни лимфом
Препоручена доза лека МабТхера која се користи као третман одржавања за пацијенте са релапсом / резистентним фоликуларним лимфомом који су одговорили на индукциони третман је 375 мг / м2 телесне површине једном свака 3 месеца (почевши 3 месеца након последње дозе терапије). Индукција) до прогресије болести или најдуже две године.
Монотерапија
• Релаксирани / рефракторни фоликуларни лимфом
Препоручена доза монотерапије МабТхера која се користи као индукцијски третман за одрасле пацијенте са фоликуларним лимфомом стадијума ИИИ-ИВ који су хеморезистентни или су у другом или наредном релапсу након хемотерапије је 375 мг / м2 телесне површине, давана као интравенозна инфузија. једном недељно током четири недеље.
За поновљено лечење монотерапијом МабТхером за пацијенте који су одговорили на претходну терапију монотерапијом МабТхером за рецидив / рефракторни фоликуларни лимфом, препоручена доза је 375 мг / м2 телесне површине, која се примењује као интравенозна инфузија једном недељно током четири недеље (видети одељак 5.1 ).
Дифузни велики Б-ћелијски не-Ходгкинов лимфом
МабТхера се мора користити у комбинацији са ЦХОП хемотерапијом. Препоручена доза је 375 мг / м2 телесне површине, примењена првог дана сваког циклуса хемотерапије током 8 циклуса након интравенозне инфузије глукокортикоидне компоненте ЦХОП -а. Сигурност и ефикасност МабТхере у комбинацији са другим хемотерапијама код дифузних великих Б-ћелија не-Ходгкиновог лимфома још нису утврђене.
Прилагођавање дозе током лечења
Не препоручује се смањење дозе МабТхере. Када се МабТхера даје у комбинацији са хемотерапијом, треба применити стандардно смањење дозе за лекове за хемотерапију.
Хронична лимфоцитна леукемија
За пацијенте са КЛЛ се препоручује профилакса одговарајућом хидратацијом и применом урикостата почевши од 48 сати пре почетка терапије, како би се смањио ризик од синдрома туморске лизе. За пацијенте са ЦЛЛ чији је број лимфоцита> 25 к 109 / Л препоручује се примена преднизона / преднизолона 100 мг интравенозно непосредно пре инфузије МабТхере да би се смањила брзина и тежина акутних инфузионих реакција и / или синдрома ослобађања цитокина.
Препоручена доза МабТхере у комбинацији са хемотерапијом код претходно нелечених и релапсних / рефракторних пацијената је 375 мг / м2 телесне површине дате 0. дана првог циклуса лечења, након чега следи 500 мг / м2 телесне површине дате првог дана сваког следећег циклус за 6 укупних циклуса. Хемотерапију треба дати након инфузије МабТхере.
Реуматоидни артритис
Пацијентима који примају МабТхеру треба дати картон упозорења пацијента при свакој инфузији.
Курс МабТхере се састоји од две интравенозне инфузије од по 1000 мг.Препоручена доза МабТхере је 1000 мг интравенозном инфузијом, након чега следи друга интравенска инфузија од 1000 мг две недеље касније.
Потребу за даљим лечењем треба проценити 24 недеље након претходног циклуса. Поновно лијечење треба извршити у то вријеме ако преостала активност заостале болести остане, у противном поновну терапију треба одгодити док се преостала активност болести поново не појави.
Доступни подаци указују на то да се клинички одговор обично постиже у року од 16 до 24 недеље од почетног курса лечења. Код пацијената који не виде терапијску корист у овом временском периоду, треба пажљиво размотрити да ли да наставе терапију.
Грануломатоза са полиангиитисом и микроскопским полиангиитисом
Пацијентима који се лече МабТхером треба дати картон упозорења пацијента при свакој инфузији.
Препоручена доза МабТхере за индукциону терапију ремисије грануломатозе са полиангиитисом и микроскопским полиангиитисом је 375 мг / м2 телесне површине, која се даје интравенозном инфузијом једном недељно током 4 недеље (4 укупне инфузије).
За пацијенте са грануломатозом са полиангиитисом и микроскопским полиангиитисом, током и после лечења МабТхером, препоручује се профилакса против упале плућа. Пнеумоцистис јировеци, (ПЦП), према потреби.
Посебне популације
Педијатријска популација
Безбедност и ефикасност лека МабТхера код деце и адолесцената млађих од 18 година још нису утврђени. Нема доступних података.
Старији пацијенти
Није потребно прилагођавање дозе код старијих пацијената (старијих од 65 година).
Начин примене
Припремљени раствор МабТхере треба применити интравенозном инфузијом кроз наменску линију. Не треба га давати као интравенозни потисак или болус. Пацијенте треба пажљиво пратити ради појаве синдрома ослобађања цитокина (видети одељак 4.4). Пацијентима који развију тешке реакције, нарочито тешку диспнеју, бронхоспазам или хипоксију, инфузију треба одмах прекинути. Пацијенте са не-Ходгкиновим лимфомом треба затим проценити на присуство синдрома туморске лизе извођењем одговарајућих лабораторијских тестова и на присуство плућне инфилтрације помоћу рендгенског снимка грудног коша. симптоми и нормализација лабораторијских вредности и рендген грудног коша. Тек тада се инфузија може наставити почетном брзином која се смањује за половину него раније. Ако се поново појаве исте озбиљне нежељене реакције, одлуку о прекиду терапије треба пажљиво размотрити од случаја до случаја.
Благе или умерене реакције повезане са инфузијом (ИРР) (видети одељак 4.8) генерално реагују на смањење брзине инфузије. Како се симптоми побољшавају, брзина инфузије се може повећати.
Прва инфузија
Препоручена почетна брзина инфузије је 50 мг / х; након првих 30 минута, може се повећавати у корацима од 50 мг / х сваких 30 минута, до максимално 400 мг / х.
Накнадне инфузије
За све индикације
Накнадне дозе МабТхере могу се примењивати при почетној брзини инфузије од 100 мг / х и повећавати за 100 мг / х у интервалима од 30 минута, до максимално 400 мг / х.
Само за реуматоидни артритис
Алтернативна шема за бржу примену следећих инфузија
Ако са првом или наредним инфузијама које су дате у дози од 1000 мг МабТхере према стандардном распореду инфузије, пацијенти нису доживели озбиљну реакцију повезану са инфузијом, друга и наредне инфузије могу се давати бржим темпом, истом брзином концентрација претходних инфузија (4 мг / мл за запремину од 250 мл).
Инфузију започните брзином од 250 мг / х првих 30 минута, а затим 600 мг / х наредних 90 минута.Ако се бржа инфузија добро подноси, исти распоред инфузије може се користити за давање следећих инфузија.
Бржу инфузију не треба давати пацијентима са клинички значајним кардиоваскуларним обољењима, укључујући аритмије, или који су у прошлости доживели тешке реакције на инфузију ритуксимаба или било коју претходну биолошку терапију.
04.3 Контраиндикације
Контраиндикације за употребу код не-Ходгкиновог лимфома и хроничне лимфоцитне леукемије
Преосетљивост на активну супстанцу, на мишје протеине или на било коју другу помоћну супстанцу наведену у одељку 6.1.
Активне, тешке инфекције (видети одељак 4.4).
Пацијенти у тешком имунолошком стању.
Контраиндикације за употребу код реуматоидног артритиса, код грануломатозе са полиангиитисом и микроскопским полиангиитисом
Преосетљивост на активну супстанцу, на мишје протеине или на било коју другу помоћну супстанцу наведену у одељку 6.1.
Активне, тешке инфекције (видети одељак 4.4).
Пацијенти у тешком имунолошком стању.
Тешка срчана инсуфицијенција (ИВ класа Нев Иорк Хеарт Ассоциатион) или тешка, неконтролисана болест срца (видети одељак 4.4 за друге срчане поремећаје).
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Да би се побољшала следљивост биолошких лекова, назив лека МабТхера треба јасно да се забележи у картону пацијената.
Прогресивна мултифокална леукоенцефалопатија
Свим пацијентима који се лече леком МабТхера за реуматоидни артритис, грануломатозу са полиангиитисом и микроскопски полиангиитис потребно је уз сваку инфузију дати картицу упозорења за пацијента. Картица упозорења садржи важне безбедносне информације за пацијенте у вези са потенцијално великим инфекцијама, укључујући прогресивну мултифокалну леукоенцефалопатију (ПМЛ).
Веома ретки смртни случајеви ПМЛ -а пријављени су након употребе лека МабТхера. Пацијенте треба редовно надгледати ради откривања нових или погоршања неуролошких симптома или због знакова који указују на ПМЛ. дијагноза ПМЛ је искључена. Лекар треба да процени пацијента како би утврдио да ли симптоми указују на неуролошку дисфункцију и, ако је тако, да ли ови симптоми вероватно указују на ПМЛ. Треба потражити неуролошко саветовање ако је клинички индицирано.
Ако сте у недоумици, треба размотрити даљу процену, укључујући тестове као што је МРИ пожељно са контрастом, тестирање цереброспиналне течности (ЦСФ) за процену ДНК вируса ЈЦ и поновљене неуролошке процене.
Лекари треба да буду посебно опрезни на симптоме који указују на ПМЛ, а које пацијент можда неће приметити (на пример, когнитивне, неуролошке или психијатријске симптоме). Пацијента такође треба саветовати да обавести свог партнера или неговатеља о лечењу, јер могу приметити симптоме којих пацијент није свестан.
Ако пацијент развије ПМЛ, примену лека МабТхера мора трајно прекинути.
Након реконституције имунолошког система код имунокомпромитованих пацијената са ПМЛ -ом, примећена је стабилизација или побољшање. Није познато да ли ће рано откривање ПМЛ -а и прекид терапије МабТхером довести до сличне стабилизације или побољшања.
Не-Ходгкинов лимфом и хронична лимфоцитна леукемија
Реакције повезане са инфузијом
МабТхера је повезана са реакцијама повезаним са инфузијом, које су потенцијално повезане са ослобађањем цитокина и / или других хемијских посредника.Синдром ослобађања цитокина може се клинички разликовати од акутних реакција преосетљивости.
Овај скуп реакција, који укључује синдром ослобађања цитокина, синдром лизе тумора и анафилактичке реакције и реакције преосетљивости, описан је у наставку. Ове реакције нису специфично повезане са начином примене МабТхере и могу се посматрати са обе формулације.
Озбиљне и фаталне реакције повезане са инфузијом пријављене су током постмаркетиншке употребе интравенске формулације МабТхера, са почетком у року од 30 минута до 2 сата након почетка прве. ИВ инфузију МабТхере. Ове реакције су окарактерисане плућним догађајима, а у неким случајевима случајеви су укључивали брзу лизу тумора и симптоме синдрома туморске лизе, као и грозницу, зимицу, дрхтавицу, хипотензију, уртикарију, ангиоедем и друге симптоме (видети одељак 4.8).
Синдром тешког ослобађања цитокина карактерише тешка диспнеја, често праћена бронхоспазмом и хипоксијом, као и грозница, зимица, дрхтавица, кошница и ангиоедем. Овај синдром може бити повезан са неким карактеристикама синдрома лизе тумора, као што су хиперурикемија, хиперкалемија, хипокалцемија, хиперфосфатемија, акутна бубрежна инсуфицијенција, повишена концентрација лактат дехидрогеназе (ЛДХ) и може бити повезан са акутном респираторном инсуфицијенцијом и смрћу. Акутна респираторна инсуфицијенција може бити праћена догађајима као што је плућна интерстицијска инфилтрација или плућни едем, видљиви на рендгенском снимку грудног коша. Синдром се често јавља у року од једног до два сата од почетка прве инфузије. Пацијенти са историјом плућне инсуфицијенције или инфилтрације тумора плућа могу имати повећан ризик од лоших исхода и треба их третирати са већим опрезом. Пацијентима код којих се развије тешки синдром ослобађања цитокина треба одмах прекинути инфузију (видети одељак 4.2) и треба им дати агресивно симптоматско лечење. Пошто почетно побољшање клиничких симптома може бити праћено погоршањем, ове пацијенте треба пажљиво пратити све до синдрома лизе тумора и плућна инфилтрација се решава или искључује.
Даљи третман пацијената након потпуног повлачења симптома и знакова ретко је резултирао понављањем тешког синдрома ослобађања цитокина.
Пацијенте са високим туморским оптерећењем или са великим бројем (≥ 25 к 109 / Л) циркулишућих неопластичних ћелија, као што су пацијенти са ХЛЛ, који могу бити у повећаном ризику од посебно тешког синдрома ослобађања цитокина, треба третирати изузетно опрезно. Ове пацијенте треба пажљиво пратити током прве инфузије. Код таквих пацијената треба размислити о употреби смањене брзине инфузије за прву инфузију или подељеној дози током два дана током првог циклуса и сваког наредног циклуса ако је број лимфоцита и даље> 25 к. 109 / л.
Све нежељене реакције повезане са инфузијом (укључујући синдром ослобађања цитокина праћен хипотензијом и бронхоспазмом у 10% пацијената) примећене су код 77% пацијената лечених МабТхером (видети одељак 4.8). Ови симптоми су генерално реверзибилни са прекидом инфузије МабТхере и уз примену антипиретичких лекова, антихистаминика и, повремено, кисеоника, интравенозних физиолошких раствора или лекова за бронходилатацију и, ако је потребно, и глукокортикоида. За тешке реакције видети горе описани синдром ослобађања цитокина.
Анафилактичке и друге реакције преосетљивости су пријављене код пацијената након интравенозне примене протеина. За разлику од синдрома ослобађања цитокина, реакције преосетљивости се обично јављају у року од неколико минута од почетка инфузије. У случају алергијске реакције током примене лека МабТхера, лекови за лечење реакција преосетљивости, нпр. епинефрин (адреналин), антихистаминици и глукокортикоиди треба да буду доступни за тренутну употребу.Клиничке манифестације анафилаксије могу изгледати слично клиничким манифестацијама синдрома ослобађања цитокина (горе описано). Реакције приписане преосетљивости пријављиване су ређе од оних које се приписују ослобађању цитокина.
Додатне реакције пријављене у неким случајевима су инфаркт миокарда, фибрилација атрија, плућни едем и акутна реверзибилна тромбоцитопенија. Током примене лека МабТхера може доћи до хипотензије, па би требало размотрити прекид антихипертензивних лекова 12 сати пре инфузије МабТхере.
Срчани поремећаји
Случајеви ангине пекторис, срчане аритмије, као што су треперење и фибрилација атрија, затајење срца и / или инфаркт миокарда догодили су се код пацијената лечених леком МабТхера. Због тога треба пажљиво пратити пацијенте са историјом срчаних обољења и / или кардиотоксичне хемотерапије.
Хематолошка токсичност
Иако МабТхера сама по себи није мијелосупресивна, треба обратити посебну пажњу приликом разматрања лечења пацијената са аутологним неутрофилима тромбоцита коштане сржи и других ризичних група са вероватно оштећеном функцијом коштане сржи без изазивања мијелотоксичности.
Током терапије леком МабТхера треба редовно вршити комплетну крвну слику, укључујући неутрофиле и тромбоците.
Инфекције
Озбиљне инфекције, укључујући и смртне случајеве, могу се јавити током терапије леком МабТхера (видети одељак 4.8).
МабТхера се не сме користити код пацијената са тешким активним инфекцијама (нпр. Туберкулозом, сепсом и опортунистичким инфекцијама, видети одељак 4.3).
Лекари треба да буду опрезни када разматрају употребу МабТхере код пацијената са историјом понављајућих или хроничних инфекција или са основним стањима која могу додатно предиспонирати пацијенте на озбиљне инфекције (видети одељак 4.8).
Пријављени су случајеви реактивације хепатитиса Б код испитаника који су примали МабТхеру, укључујући извештаје о фулминантном хепатитису са фаталним исходом. Већина ових субјеката је такође примила цитотоксичну хемотерапију. Ограничени подаци из студије спроведене на пацијентима са повратном / рефракторном ХЛЛ указују на то да лечење МабТхером може такође погоршати исход примарне инфекције хепатитисом Б.Скрининг на вирус хепатитиса Б (ХБВ) требало би да се уради код свих пацијената пре почетка лечења МабТхером и требало би да укључи најмање испитивање ХБсАг и ХБцАб. Ови тестови се затим могу надопунити другим одговарајућим маркерима према локалним смерницама. Пацијенте са активном инфекцијом хепатитисом Б не треба лечити МабТхером. Пацијенте са позитивном серологијом хепатитиса Б (и ХБсАг и ХБцАб) треба да прегледа лекар хепатолог пре почетка лечења и треба их пратити и пратити у складу са локалним клиничким стандардима како би се спречила реактивација хепатитиса Б.
Веома ретки случајеви прогресивне мултифокалне леукоенцефалопатије (ПМЛ) забележени су током постмаркетиншке употребе МабТхере у НХЛ и ЦЛЛ (видети одељак 4.8). Већина пацијената је примала МабТхеру у комбинацији са хемотерапијом или као део програма трансплантације хематопоетских матичних ћелија.
Имунизација
Безбедност имунизације живим вирусним вакцинама након терапије МабТхером није проучавана за пацијенте са НХЛ и ЦЛЛ и вакцинација са живим вирусним вакцинама се не препоручује. Пацијенти лечени МабТхером могу примити вакцине против вируса. Међутим, стопа одговора на неживи вирус У не-рандомизованој студији, пацијенти са рецидивом НХЛ ниског степена који су примали МабТхера монотерапију у поређењу са нелеченим здравим контролама добровољаца имали су нижу стопу одговора на вакцинацију са антигенима за повишење тетануса (16% наспрам 81%) и Неоантигени хемоцијанина (КЛХ) Кеихоле Лимпет (4% наспрам 76% када се процени> 2 пута повећање титра антитела). Очекује се да ће ЦЛЛ имати сличне резултате с обзиром на сличности између две болести, међутим то није процењено клиничким студијама . предтерапијска антитела против антигенске плоче (Стрептококус пнеумоние, инфлуенца А, заушњаци, рубеола, водене козице) одржавана је најмање 6 месеци након третмана са МабТхером.
Реакције на кожи
Пријављене су озбиљне кожне реакције, попут токсичне епидермалне некролизе (Лиелл-ов синдром) и Стевенс-Јохнсоновог синдрома, неке са смртним исходом (видети одељак 4.8). У случају таквих догађаја, ако се сумња на везу са МабТхером, лечење треба трајно прекинути. Реуматоидни артритис, грануломатоза са полиангиитисом и микроскопски полиангиитис.
Популације са реуматоидним артритисом које нису биле метотрексат (МТКС)
Употреба МабТхере се не препоручује код пацијената који нису примали МТКС јер није успостављен повољан однос користи и ризика.
Реакције повезане са инфузијом
МабТхера је повезана са реакцијама везаним за инфузију (ИРР), које могу бити повезане са ослобађањем цитокина и / или других хемијских посредника. Пре сваке инфузије лека МабТхера увек треба применити премедикацију са аналгетским / антипиретичким лековима и антихистаминским лековима са реуматоидним артритисом, премедикацију глукокортикоидима увек треба применити пре сваке инфузије МабТхере како би се смањила учесталост и озбиљност ИРР -а (видети одељке 4.2 и 4.8).
Озбиљни случајеви ИРР са фаталним исходом пријављени су код пацијената са реуматоидним артритисом у постмаркетиншком окружењу.
У лечењу реуматоидног артритиса, већина реакција повезаних са инфузијом у клиничким испитивањима била је благог до умереног интензитета. Најчешћи симптоми били су алергијске реакције попут главобоље, свраба, иритације грла, црвенила, осипа, осипа, хипертензије и пирексије. Опћенито, удио пацијената који су доживјели неку реакцију инфузије био је већи након прве инфузије него након друге у било којем циклусу лијечења.Учесталост ИРР -а се смањила у наредним курсевима (видјети дио 4.8). Пријављене реакције су генерално биле реверзибилне са смањењем брзине инфузије или прекидом примене МабТхере и узимањем антипиретика, антихистаминика и, повремено, кисеоника, интравенозне физиолошке отопине или бронходилататора и глукокортикоида, ако је потребно. Пажљиво пратите пацијенте са већ постојећим срчаним обољењима стања и они који су имали претходне кардиопулмоналне нежељене реакције.У зависности од тежине ИРР -а и потребне интервенције, привремено или трајно прекинути примену лека МабТхера. У већини случајева, инфузија се може наставити смањењем брзине на 50% (нпр. Са 100 мг / х на 50 мг / х) када се симптоми потпуно повуку.
Лекови за лечење реакција преосетљивости, нпр. епинефрин (адреналин), антихистаминици и глукокортикоиди, требало би да буду доступни за тренутну употребу, у случају алергијских реакција током примене лека МабТхера.
Нема података о безбедности лека МабТхера код пацијената са умереном срчаном инсуфицијенцијом (НИХА класа ИИИ) или тешком, неконтролисаном болешћу срца. Код пацијената лечених леком МабТхера, уочено је да су већ постојећа стања срчане исхемије, попут ангине пекторис, постала симптоматска, као и фибрилација и треперење атрија. Стога, код пацијената са историјом срчаних обољења, као и код оних који су доживели претходне реакције кардиопулмонални нежељени догађаји, ризик од кардиоваскуларних компликација проузрокованих инфузијским реакцијама треба размотрити пре почетка терапије леком МабТхера, а пацијенте треба пажљиво пратити током примене. Може доћи до хипотензије током инфузије лека МабТхера, па се прекид примене антихипертензивних лекова 12 сати пре МабТхера инфузија.
ИРР код пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом били су слични онима који су примећени у клиничким студијама код пацијената са реуматоидним артритисом (видети одељак 4.8).
Срчани поремећаји
Случајеви ангине пекторис, срчане аритмије, као што су треперење и фибрилација атрија, затајење срца и / или инфаркт миокарда догодили су се код пацијената лечених леком МабТхера. Због тога је потребно пажљиво пратити пацијенте са историјом срчаних обољења (види „Реакције повезане са инфузијом“ горе).
Инфекције
На основу механизма деловања МабТхере и сазнања да Б ћелије играју важну улогу у одржавању нормалног имунолошког одговора, пацијенти имају повећан ризик од инфекција након терапије МабТхером (видети одељак 5.1). Озбиљне инфекције, укључујући фаталне догађаје, могу се јавити током Терапија МабТхером (видети одељак 4.8) МабТхера се не сме давати пацијентима са тешком активном инфекцијом (нпр. Туберкулозом, сепсом и опортунистичким инфекцијама, видети одељак 4.3) или пацијентима са озбиљним имунодефицијенцијом.
(нпр. где су вредности ЦД4 или ЦД8 веома ниске). Лекари треба да буду опрезни када разматрају употребу МабТхере код пацијената са историјом понављајућих или хроничних инфекција или са основним стањима која могу додатно предиспонирати пацијенте на озбиљне инфекције, нпр. Хипогамаглобулинемију (видети одељак 4.8).Препоручује се одређивање нивоа имуноглобулина пре почетка лечења МабТхером.
Пацијенте код којих се јаве знаци и симптоми инфекције након терапије леком МабТхера потребно је одмах прегледати и адекватно лечити. Пре започињања следећег курса лечења МабТхером, пацијенте треба поново проценити на могући ризик од инфекција.
Пријављени су врло ретки случајеви фаталне прогресивне мултифокалне леукоенцефалопатије (ПМЛ) након употребе МабТхере за лечење реуматоидног артритиса и аутоимуних болести, укључујући системски еритематозни лупус (СЛЕ) и васкулитис.
Инфекција хепатитисом Б.
Пријављени су случајеви реактивације хепатитиса Б, укључујући и оне са фаталним исходом, код пацијената са реуматоидним артритисом, грануломатозом са полиангиитисом и микроскопским полиангиитисом који су примали МабТхеру.
Скрининг на вирус хепатитиса Б (ХБВ) треба да се обави код свих пацијената пре почетка терапије леком МабТхера и требало би да укључи најмање испитивање ХБсАг и ХБцАб. Ови тестови се затим могу допунити другим одговарајућим маркерима. Према локалним смерницама. Пацијенти са активним хепатитисом Инфекцију Б не треба лечити леком МабТхера. Пацијенте са позитивном серологијом хепатитиса Б (и ХБсАг и ХБцАб) треба прегледати лекар хепатолог и треба их пратити и пратити у складу са локалним клиничким стандардима како би се спречила реактивација хепатитиса Б.
Неутропенија са касним почетком
Измерите неутрофиле пре сваког курса лека МабТхера и у редовним интервалима до 6 месеци након престанка лечења и у случају знакова или симптома инфекције (видети одељак 4.8).
Реакције на кожи
Пријављене су озбиљне кожне реакције, попут токсичне епидермалне некролизе (Лиелл-ов синдром) и Стевенс-Јохнсоновог синдрома, неке са смртним исходом (видети одељак 4.8). У случају таквих догађаја, ако се сумња на везу са МабТхером, лечење треба трајно прекинути.
Имунизација
Лекари треба да провере статус вакцинације пацијента и да се придржавају тренутних смерница за имунизацију пре терапије МабТхером.Вакцинацију треба завршити најмање 4 недеље пре прве примене МабТхере.
Безбедност имунизације живим вирусним вакцинама након терапије МабТхером није проучавана, па се вакцинација живим вирусним вакцинама не препоручује током терапије МабТхером или током периода исцрпљивања периферних Б ћелија.
Пацијенти који се лече МабТхером могу добити вакцине против живих вируса. Међутим, стопе одговора на вакцине против живих вируса могу се смањити. У рандомизованој студији, пацијенти са реуматоидним артритисом који су лечени МабТхером и метотрексатом имали су сличне стопе одговора као они код пацијената који су примали само метотрексат на повишене антигене тетануса (39% наспрам 42%), снижене стопе на полисахаридну вакцину. Пнеумокок (43% у односу на 82% до најмање 2 серотипа против пнеумококних антитела) и неоантигена КЛХ (47% наспрам 93%), када се дају 6 месеци након МабТхере. Ако су током терапије МабТхером потребне вакцинације против живих вируса, треба их завршити најмање 4 недеље пре почетка следећег курса МабТхере.
У "глобалном искуству поновљених третмана МабТхере у једној години у" окружењу реуматоидног артритиса, проценти пацијената са позитивним титром антитела против С. пнеумониае, грипа, заушњака, рубеоле, богиња и токсина тетануса генерално су биле сличне основним стопама.
Истовремена / узастопна употреба других ДМАРД у лечењу реуматоидног артритиса
Не препоручује се истовремена употреба МабТхере и антиреуматских терапија осим оних наведених у индикацијама и дозирању за реуматоидни артритис.
Постоје ограничени подаци из клиничких испитивања да би се у потпуности проценила безбедност узастопне употребе после МабТхере других ДМАРД (укључујући инхибиторе ТНФ -а и других биолошких лекова) (видети одељак 4.5). Доступни подаци указују на то да је стопа клинички значајних инфекција непромењена када се користе ове терапије користи се код пацијената који су претходно били лечени МабТхером; међутим, пацијенте треба пажљиво пратити због знакова инфекције ако се након терапије МабТхером користе биолошки агенси и / или ДМАРД.
Неоплазме
Имуномодулаторни лекови могу повећати ризик од рака. На основу ограниченог искуства са МабТхером код пацијената са реуматоидним артритисом (видети одељак 4.8), чини се да тренутни подаци не указују на повећан ризик од малигнитета, међутим, тренутно се не може искључити могући ризик од развоја солидних тумора.
04.5 Интеракције са другим лековима и други облици интеракција
Тренутно постоје ограничени подаци о могућим интеракцијама лекова са МабТхером.
Чини се да код пацијената са ЦЛЛ-ом истовремена примена са МабТхером нема утицаја на фармакокинетику флударабина или циклофосфамида. Осим тога, нема очигледног ефекта флударабина и циклофосфамида на фармакокинетику МабТхере.
Истовремена примена са метотрексатом није имала утицаја на фармакокинетику МабТхере код пацијената са реуматоидним артритисом.
Пацијенти код којих су се развила анти-мишја или анти-химерна антитела (ХАМА / ХАЦА) могу имати алергијске реакције или реакције преосетљивости када се лече другим дијагностичким или терапијским моноклонским антителима.
Код пацијената са реуматоидним артритисом, 283 пацијента је накнадно примило биолошку ДМАРД терапију након МабТхере. Код ових пацијената, стопа клинички значајних инфекција током терапије МабТхером била је 6,01 на 100 пацијената-година у поређењу са 4,97 на 100 пацијената-година након биолошког ДМАРД третмана.
04.6 Трудноћа и дојење
Контрацепција код мушкараца и жена
Пошто ритуксимаб има дуго време задржавања код пацијената са исцрпљеним Б-ћелијама, жене у репродуктивном периоду треба да користе ефикасне методе контрацепције током лечења и до 12 месеци након завршетка терапије МабТхером.
Трудноћа
Познато је да ИгГ имуноглобулини пролазе кроз плацентну баријеру.
Ниво Б ћелија код одојчади након излагања мајке МабТхери није процењиван у клиничким испитивањима. Нема одговарајућих и добро контролисаних података из студија на трудницама, међутим пријављено је пролазно исцрпљивање Б-ћелија и лимфоцитопенија код одојчади рођене од мајки изложених МабТхери током трудноће. Слични ефекти су примећени у студијама на животињама (видети одељак 5.3). Из тог разлога, МабТхера се не сме давати трудницама, осим ако могућа корист надмашује потенцијални ризик.
Дојење
Није познато да ли се ритуксимаб излучује у мајчино млеко. Међутим, пошто се мајчински ИгГ излучује у мајчино млеко, а ритуксимаб је откривен у млеку мајмуна у лактацији, жене не би требало да доје током лечења МабТхером и 12 месеци након терапије МабТхером.
Плодност
Студије на животињама нису откриле штетне ефекте ритуксимаба на репродуктивне органе.
04.7 Утицај на способност управљања возилима и машинама
Нису спроведена испитивања утицаја МабТхере на способност управљања возилима и рада са машинама, иако до сада пријављене фармаколошке активности и нежељене реакције указују на то да МабТхера нема или има занемарљив утицај на способност управљања возилима и рада на машинама.
04.8 Нежељени ефекти
Искуство са не-Ходгкиновим лимфомом и хроничном лимфоцитном леукемијом
Сажетак сигурносног профила
Укупни безбедносни профил лека МабТхера код не-Ходгкиновог лимфома и хроничне лимфоцитне леукемије заснован је на подацима пацијената у клиничким испитивањима и постмаркетиншком надзору. Ови пацијенти су лечени МабТхером као монотерапија (као индукциони третман или као постиндукциони третман одржавања) или у комбинацији са хемотерапијом.
Најчешће уочене нежељене реакције на лек (АДР) код пацијената који су примали МабТхеру биле су ИРР које су се јавиле код већине пацијената током прве инфузије. Учесталост симптома повезаних са инфузијом значајно се смањује следећим инфузијама и мања је од 1% након осам доза МабТхере.
Инфективни догађаји (углавном бактеријски и вирусни) догодили су се у приближно 30-55% пацијената са НХЛ лечених у клиничким испитивањима и приближно 30-50% пацијената са ХЛЛ лечених у клиничким испитивањима. Најчешће пријављене или уочене озбиљне нежељене реакције на лекове биле су:
• ИРР (укључујући синдром ослобађања цитокина и синдром лизе тумора), видети одељак 4.4.
• Инфекције, видети одељак 4.4.
• Кардиоваскуларни догађаји, видети одељак 4.4.
Други пријављени озбиљни нежељени ефекти укључују реактивацију хепатитиса Б и ПМЛ (видети одељак 4.4).
Листа нежељених реакција у облику табеле
Учесталости нежељених ефеката пријављених само са МабТхером или у комбинацији са хемотерапијом сажете су у Табели 1. Унутар сваке класе учесталости, нежељени ефекти су наведени према опадајућој озбиљности. Учесталост је дефинисана као врло честа (≥ 1/10), честа ( ≥ 1/100 до
Нуспојаве које су идентификоване само током постмаркетиншког надзора и за које се не може проценити учесталост наведене су под „непознато“.
Табела 1 Нежељени ефекти пријављени у клиничким испитивањима или током постмаркетиншког надзора код пацијената са НХЛ и ЦЛЛ лечених МабТхером као монотерапија / одржавање или у комбинацији са хемотерапијом
Следећи појмови су пријављени као нежељени догађаји током клиничких испитивања; међутим, пријављена је хематолошка токсичност, неутропенична инфекција, инфекција уринарног тракта, сензорни поремећаји, пирексија са сличном или мањом учесталошћу у групама МабТхера у поређењу са контролним групама.
Карактеристични знаци и симптоми реакције повезане са инфузијом пријављени су у више од 50% пацијената у клиничким студијама и примећени су углавном током прве инфузије, обично у прва два сата. Ови симптоми углавном укључују грозницу, зимицу и укоченост. Други симптоми укључују црвенило, ангиоедем, бронхоспазам, повраћање, мучнину, уртикарију / осип, умор, главобољу, иритацију грла, ринитис, пруритус, бол, тахикардију, хипертензију, хипотензију, диспнеју, диспепсију, астенију и симптоме синдрома лизе тумора. Тешка инфузија -реакције повезане (попут бронхоспазма, хипотензије) јављале су се у до 12% случајева. Додатне реакције пријављене у неким случајевима су инфаркт миокарда, фибрилација атрија, плућни едем и акутна реверзибилна тромбоцитопенија. Погоршање већ постојећих срчаних обољења као што су ангина пекторис или конгестивна срчана инсуфицијенција или тешка срчана болест (срчана инсуфицијенција, инфаркт миокарда, атријална фибрилација), плућни едем, отказивање више органа, синдром лизе тумора, синдром ослобађања цитокина, бубрежна инсуфицијенција и респираторна инсуфицијенција квар је пријављен са мањом или непознатом учесталошћу. Учесталост симптома повезаних са инфузијом значајно се смањила са наредним инфузијама и износи
Опис избора нежељених реакција
Инфекције
МабТхера изазива исцрпљивање Б ћелија у приближно 70-80% пацијената, али је овај догађај повезан са смањењем имуноглобулина у серуму само у мањине пацијената.
Локализоване инфекције кандидом, као што је херпес зостер, пријављене су у већој учесталости у групи која је примала МабТхеру у рандомизираним испитивањима. Озбиљне инфекције су пријављене код приближно 4% пацијената лечених монотерапијом МабТхером. Веће стопе свих инфекција, укључујући инфекције 3. или 4. степена, примећене су током двогодишњег одржавања са МабТхером у поређењу са посматрањем. Није било кумулативне токсичности у смислу инфекција пријављених у двогодишњем периоду лечења. Осим тога, друге озбиљне вирусне инфекције, било нове, реактивиране или погоршане, пријављене су током лечења МабТхером, од којих су неке биле фаталне. Већина пацијената је примала МабТхеру у комбинацији са хемотерапијом или као део трансплантације крвотворних матичних ћелија. Примери ових озбиљних вирусних инфекција су инфекције узроковане херпетичким вирусима (цитомегаловирус, Варицелла Зостер вирус и Херпес Симплек), ЈЦ вирусом (прогресивна мултифокална леукоенцефалопатија (ПМЛ)) и вирусним хепатитисом Ц. Случајеви фаталног ПМЛ -а такође су пријављени током клиничких испитивања и догодили су се ти након прогресије болести и поновног лечења. Пријављени су случајеви реактивације хепатитиса Б, од којих се већина јавила код пацијената који су примали МабТхеру у комбинацији са цитотоксичном хемотерапијом. Код пацијената са повратним / рефракторним ЦЛЛ-ом, учесталост инфекције хепатитисом Б степена 3/4 (реактивација и примарна инфекција) била је 2% у Р-ФЦ наспрам 0% у ФЦ. Уочена је прогресија Капосијевог саркома. Код пацијената изложених МабТхери са већ постојећи Капосијев сарком Ови случајеви су се јавили са неодобреним индикацијама и већина пацијената је била ХИВ позитивна.
Хематолошке нежељене реакције
У клиничким испитивањима која су користила МабТхеру као монотерапију примењену током 4 недеље, хематолошке абнормалности су се јавиле код мањине пацијената и биле су генерално благе и реверзибилне. Тешка неутропенија (степен 3/4) пријављена је код 4,2% пацијената, анемија код 1,1% и тромбоцитопенија код 1,7% пацијената. Током двогодишњег одржавања са МабТхером, леукопенија (5% вс 2%, степен 3/4) и неутропенија (10% вс 4%, степен 3/4) пријављено је са већом учесталошћу у поређењу са посматрањем. Учесталост тромбоцитопеније била је ниска (у односу на ЦХОП 79%, Р-ФЦ 23% всХР 12%), неутропенија (Р-ЦВП 24% вс ЦВП 14%; Р-ЦХОП 97% вс ЦХОП 88%, Р-ФЦ 30% вс ХР 19% код претходно нелечене ЦЛЛ), панцитопенија (Р-ФЦ 3% вс ЦФ 1% у претходно нетретираној КЛЛ), опћенито су пријављени са већом учесталошћу у поређењу са само хемотерапијом. Међутим, већа инциденција неутропеније код пацијената лечених МабТхером и хемотерапијом није била повезана са већом учесталошћу инфекција и инфестација у поређењу са пацијентима леченим само хемотерапијом. Претходно нелечене и релапсне / рефракторне ЦЛЛ студије показале су да је у 25% пацијената лечених са Р-ФЦ, неутропенија је била продужена (дефинисана као број неутрофилних гранулоцита мања од 1к109 / л између 24. дана и 42. дана након последње дозе) или се јавила са касним почетком (дефинисана као број неутрофилних гранулоцита мања од 1к109 / л после 42. дана након последње дозе код пацијената који нису имали претходну продужену неутропенију или су се опоравили пре 42. дана) након лечења МабТхером и ЦФ.
Нису забележене разлике у учесталости анемије. Пријављено је неколико случајева касне неутропеније која се догодила више од четири недеље након последње инфузије МабТхере. У ЦЛЛ студији прве линије, пацијенти са стадијом Ц Бинета имали су више нежељених догађаја у групи са Р-ФЦ него у групи са ФЦ (Р-ФЦ 83% вс ХР 71%). У студији релапса / рефракторне ЦЛЛ, тромбоцитопенија степена 3/4 је пријављена код 11% пацијената у РФЦ групи наспрам 9% пацијената у ЦФ групи.
У студијама са МабТхером код пацијената са Валдестромовом макроглобулинемијом, примећено је пролазно повећање нивоа ИгМ у серуму након почетка лечења, што може бити повезано са хипервискозношћу и сродним симптомима. месеци.
Кардиоваскуларне нежељене реакције
У клиничким испитивањима само са МабТхером, кардиоваскуларне реакције су пријављене код 18,8% пацијената са хипотензијом и хипертензијом као најчешће пријављени догађаји. Током инфузије забележени су случајеви аритмија 3. или 4. степена (укључујући вентрикуларну и суправентрикуларну тахикардију) и ангину пекторис. Током терапије одржавања, учесталост срчаних поремећаја степена 3/4 била је упоредива међу леченим пацијентима. Са МабТхером и опсервацијом. пријављени као озбиљни нежељени догађаји (укључујући фибрилацију атрија, инфаркт миокарда, отказ леве коморе, исхемију миокарда) код 3% пацијената лечених МабТхером у поређењу са срчаним аритмијама степена 3 и 4, посебно суправентрикуларним аритмијама, као што су тахикардија и треперење / фибрилација атрија, већи у РЦХОП групи (14 пацијената, 6,9%) у поређењу са ЦХОП групом (3 пацијента, 1,5%). Све ове аритмије су се јавиле у контексту инфузије МабТхере или су биле повезане са предиспонирајућим стањима као што су грозница, инфекција, акутни инфаркт миокарда или већ постојеће респираторне и кардиоваскуларне болести.Није примећена разлика између Р-ЦХОП и ЦХОП група у погледу учесталости других срчаних догађаја степена 3 и 4, укључујући срчану инсуфицијенцију, болест миокарда и манифестације коронарне артеријске болести. или 4 срчана поремећаја била су ниска и у студији прве линије (4% Р-ФЦ, 3% ФЦ) и у релапсно / ватросталној студији (4% Р-ФЦ, 4% ФЦ).
Респираторни систем
Пријављени су случајеви интерстицијске болести плућа, неки са смртним исходом.
Неуролошке патологије
Током периода лечења (фаза индукционе терапије која се састоји од Р-ЦХОП-а до осам циклуса) четири пацијента (2%) лечена Р-ЦХОП-ом, сви са кардиоваскуларним факторима ризика, доживели су цереброваскуларне тромбоемболичне несреће током првог циклуса лечења. Није било разлике између лечених група у погледу учесталости других тромбоемболијских догађаја. Насупрот томе, три пацијента (1,5%) су имала цереброваскуларне догађаје у ЦХОП групи, а сви су се јавили током периода праћења. ЦЛЛ, укупна инциденција поремећаја нервног система 3 или 4 степена била је ниска и у студији прве линије (4% Р-ФЦ, 4% ФЦ) и у студији релапса / ватросталности (3% Р-ФЦ, 3% ФЦ) .
Пријављени су случајеви синдрома постериорне реверзибилне енцефалопатије (ПРЕС) / синдрома постериорне реверзибилне леукоенцефалопатије (РПЛС). Знаци и симптоми укључују поремећаје вида, главобољу, нападе и промене у менталном статусу, са или без придружене хипертензије. Дијагноза ПРЕС / РПЛС захтева потврду са сликање церебралне. Пријављени случајеви су препознали факторе ризика за ПРЕС / РПЛС, укључујући статус истовремене болести пацијента, хипертензију, имуносупресивну терапију и / или хемотерапију.
Гастроинтестинални поремећаји
Уочена је перфорација гастроинтестиналног тракта која је у неким случајевима довела до смрти код пацијената који су примали МабТхеру за лечење не-Ходгкиновог лимфома. У већини ових случајева, МабТхера је давана уз хемотерапију.
Нивои ИгГ
У клиничкој студији која је процењивала МабТхеру у лечењу одржавања код релапса / рефракторног фоликуларног лимфома, средњи ниво ИгГ био је испод доње границе нормале (ЛЛН) (
Мали број спонтаних и литературних случајева повезаних с хипогамаглобулинемијом, у неким случајевима тешким и који захтијевају дуготрајну замјенску терапију имуноглобулином, примијећен је код педијатријских пацијената лијечених МабТхером. Последице дуготрајног исцрпљивања Б ћелија код педијатријских пацијената нису познате.
Поремећаји коже и поткожног ткива
Врло ретко су пријављени случајеви токсичне епидермалне некролизе (Лиелл-ов синдром) и Стевенс-Јохнсоновог синдрома, неки са смртним исходом.
Субпопулације пацијената - МабТхера монотерапија
Старији пацијенти (≥ 65 година):
Учесталост свих нуспојава свих степена и степена 3/4 била је слична код старијих у односу на млађе пацијенте (
Гломазна болест
Постојала је „већа инциденца АДР степена 3/4 код пацијената са гломазном болешћу него код пацијената без гломазне болести (25,6% вс 15,4%). Учесталост свих нуспојава свих степена била је слична у ове две групе.
Ретреатмент
Удео пацијената који су пријавили нежељене реакције током поновљеног лечења са даљим курсевима МабТхере био је сличан уделу пацијената који су пријавили нежељене ефекте током почетне изложености (сви нежељени ефекти свих степена и степена 3/4).
Субпопулације пацијената - Комбинована терапија са МабТхером
Старији пацијенти (≥ 65 година)
Учесталост нежељених догађаја степена 3/4 у крви и лимфном систему била је већа код старијих пацијената у поређењу са млађим пацијентима (
Искуство у реуматоидном артритису
Сажетак сигурносног профила
Укупни безбедносни профил лека МабТхера код реуматоидног артритиса заснован је на подацима пацијената лечених у клиничким испитивањима и на основу постмаркетиншког надзора.
Безбедносни профил лека МабТхера код пацијената са умереним до тешким реуматоидним артритисом сажет је у доле наведеним одељцима. У клиничким студијама, више од 3.100 пацијената је примило најмање један курс лечења и праћено је у периоду од 6 месеци до више од 5 година; приближно 2400 пацијената је примило два или више курсева лечења, а преко 1000 пацијената је прошло 5 или више курсева. Безбедносне информације прикупљене из искуства након стављања лека у промет одражавају очекивани профил нежељених реакција које су већ примећене у клиничким студијама за МабТхеру (видети одељак 4.4).
Пацијенти су примали 2 дозе МабТхере од 1000 мг, одвојене размаком од две недеље, у комбинацији са метотрексатом (10-25 мг / недељно). Инфузије МабТхере примењене су након интравенозне инфузије 100 мг метилпреднизолона; пацијенти су такође примали орални преднизон током 15 дана.
Листа нежељених реакција у облику табеле
Нежељене реакције наведене су у табели 2. Учесталост је дефинисана као врло честе (≥ 1/10), честе (≥1 / 100 до
Најчешће нежељене реакције за које се верује да су настале због узимања лека МабТхера биле су ИРР. Укупна инциденција ИРР у клиничким испитивањима била је 23% са првом инфузијом и смањила се са наредним инфузијама. Озбиљне ИРР нису биле честе (0,5% пацијената) и углавном су се јављале током почетног циклуса. Поред нежељених реакција уочених у клиничким студијама о реуматоидном артритису спроведеним са МабТхером, током постмаркетиншког искуства забележене су прогресивна мултифокална леукоенцефалопатија (ПМЛ) и реакција слична серумској болести.
Табела 2 Преглед нежељених реакција на лекове пријављених у клиничким испитивањима или током постмаркетиншког надзора који су се јавили код пацијената са реуматоидним артритисом који су примали МабТхеру.
Поновљени циклуси
Поновљени курсеви лечења повезани су са сличним профилом нежељених реакција који је примећен након прве изложености. Стопа свих нежељених реакција након прве изложености МабТхери била је највећа током првих 6 месеци, а након тога се смањила. Ово је углавном био случај са ИРР (најчешће током првог третмана), погоршањем реуматоидног артритиса и инфекцијама; све ово је било чешће у првих 6 месеци лечења.
Реакције повезане са инфузијом
У клиничким студијама, најчешће нежељене реакције на лек (АРС) након третмана са МабТхером биле су ИРР (видети Табелу 2). Међу 3189 пацијената лечених МабТхером, 1135 (36%) је имало најмање једну ИРР, а 733/3189 (23%) пацијената је имало ИРР након прве инфузије првог третмана са МабТхером. Учесталост ИРР се смањује са каснијим инфузијама.У клиничким испитивањима мање од 1% (17/3189) пацијената је доживело озбиљну ИРР. У клиничким испитивањима није било заједничких критеријума токсичности (ЦТЦ) степена 4 и није било смртних случајева услед ИРР. Удео догађаја ЦТЦ степена 3 и ИРР -а који су довели до прекида лечења смањивао се током лечења и били су ретки од 3. циклуса надаље. Интравенозна премедикација глукокортикоидима значајно је смањила учесталост и тежину ИРР (видети одељке 4.2 и 4.4). Озбиљни случајеви ИРР са фаталним исходом забележени су у постмаркетиншком окружењу.
У студији која је осмишљена да процени безбедност „брже инфузије МабТхере код пацијената са реуматоидним артритисом, пацијентима са умерено до тешким активним реуматоидним артритисом који нису доживели озбиљну ИРР током или у року од 24 сата након прве проучене инфузије, било је дозвољено да подвргнути 2-сатној интравенској инфузији МабТхере. Пацијенти са историјом тешке инфузионе реакције на биолошку терапију за реуматоидни артритис нису примљени у студију. Учесталост, врсте и озбиљност ИРР -а били су у складу са историјским подацима. Нису примећене озбиљне ИРР -ове.
Опис избора нежељених реакција
Инфекције
Укупна учесталост инфекција била је приближно 94 на 100 пацијената-година у групи МабТхера. Инфекције су биле претежно благе до умерене и укључивале су углавном инфекције горњих дисајних путева и уринарног тракта. Захтевали су ИВ антибиотике било је то око 4 од 100 пацијената-година. Учесталост озбиљних инфекција није показала значајан пораст након поновљених курсева примене МабТхере. У клиничким испитивањима пријављене су инфекције доњих дисајних путева (укључујући пнеумонију), са сличном учесталошћу у групама МабТхера у поређењу са групама МабТхере. Случајеви прогресивне мултифокалне леукоенцефалопатије са фаталним исходом пријављени су након употребе МабТхере за лечење аутоимуних болести. Ово укључује реуматоидни артритис и аутоимуне услове ван индикације, попут системског еритематозног лупуса (СЛЕ) и васкулитиса. Реактивација хепатитиса Б је пријављена код пацијената са не-Ходгкиновим лимфомом који су примали МабТхеру у комбинацији са цитотоксичном хемотерапијом. (Погледајте не-Ходгкинов лимфом .) Реактивација инфекције хепатитисом Б такође је ретко пријављивана код пацијената са РА који су примали МабТхеру (видети одељак 4.4).
Кардиоваскуларне нежељене реакције
Озбиљне срчане реакције забележене су са "учесталошћу од 1,3 на 100 пацијент-година међу онима који су лечени МабТхером и 1,3 на 100 пацијент-година код пацијената лечених плацебом. Удео пацијената са срчаним реакцијама (свим или тешким) није се повећао у различити циклуси.
Неуролошки догађаји
Пријављени су случајеви синдрома постериорне реверзибилне енцефалопатије (ПРЕС) / синдрома постериорне реверзибилне леукоенцефалопатије (РПЛС). Знаци и симптоми укључују поремећаје вида, главобоље, нападе и измењени ментални статус, са или без придружене хипертензије. Дијагноза ПРЕС / РПЛС захтева потврду сликањем мозга. Описани случајеви су имали познате факторе ризика за ПРЕС / РПЛС, укључујући основну болест пацијената, хипертензију, имуносупресивну терапију и / или хемотерапију.
Неутропенија
Након примене лека МабТхера забележени су случајеви неутропеније, од којих је већина била пролазна и благог или умереног интензитета. Неутропенија се може јавити неколико месеци након примене лека МабТхера (видети одељак 4.4).
У плацебо контролисаним клиничким испитивањима, 0,94% (13/382) пацијената лечених МабТхером и 0,27% (2/731) пацијената лечених плацебом развило је тешку неутропенију.
Неутропенични догађаји, укључујући тешку и упорну касну појаву неутропеније, од којих су неки били повезани са смртоносним инфекцијама, ретко су пријављивани у постмаркетиншком искуству.
Поремећаји коже и поткожног ткива
Врло ретко су пријављени случајеви токсичне епидермалне некролизе (Лиелл-ов синдром) и Стевенс-Јохнсоновог синдрома, неки са смртним исходом.
Лабораторијске аномалије
Хипогамаглобулинемија (ИгГ или ИгМ испод доње границе нормале) је примећена код пацијената са реуматоидним артритисом лечених МабТхером. Није било повећања стопе општих или тешких инфекција након ниских нивоа ИгГ или ИгМ (видети одељак 4.4).
Мали број спонтаних и литературних случајева повезаних с хипогамаглобулинемијом, у неким случајевима тешким и који захтијевају дуготрајну замјенску терапију имуноглобулином, примијећен је код педијатријских пацијената лијечених МабТхером. Последице дуготрајног исцрпљивања Б ћелија код педијатријских пацијената нису познате.
Искуство у грануломатози са полиангиитисом и микроскопским полиангиитисом
У клиничкој студији о грануломатози са полиангиитисом и микроскопским полиангиитисом, 99 пацијената је лечено МабТхером (375 мг / м2, једном недељно током 4 недеље) и глукокортикоидима (видети одељак 5.1).
Листа нежељених реакција у облику табеле
Нуспојаве наведене у Табели 3 представљају све нежељене догађаје који су се догодили са инциденцом ≥ 5% у групи МабТхера.
Табела 3. Нежељене реакције на лек које се јављају код ≥ 5% пацијената који су примали МабТхеру и са већом учесталошћу од упоредне групе у шестомесечној кључној клиничкој студији.
Избор нежељених реакција на лекове
Реакције повезане са инфузијом
ИРР у клиничким студијама који се односе на грануломатозу са полиангиитисом и микроскопским полиангиитисом дефинисани су као било који нежељени догађај који се догодио у року од 24 сата од инфузије и сматрани су да је инфузија повезана са безбедносном популацијом. 99 пацијената је лечено МабТхером, а 12% је имало барем један ИРР. Сви ИРР су били степена 1 или 2 према ЦТЦ -у. Најчешћи ИРР укључивао је синдром ослобађања цитокина, налете врућине, иритацију грла и тремор.МабТхера је давана у комбинацији са интравенозним глукокортикоидима који могу смањити учесталост и тежину ових догађаја.
Инфекције
У 99 пацијената лечених леком МабТхера, укупна стопа инфекција била је приближно 237 на 100 пацијената-година (95% ЦИ 197-285) на шестомесечном примарном исходу. Инфекције су биле углавном благе до умерене и састојале су се углавном од инфекција. инфекције тракта, херпес зостера и уринарног тракта. Стопа озбиљних инфекција била је приближно 25 на 100 пацијената-година. Најчешћа озбиљна инфекција у групи која је примала МабТхеру била је пнеумонија са учесталошћу од 4%.
Неоплазме
Учесталост малигних болести код пацијената лечених леком МабТхера у клиничким студијама које се односе на грануломатозу са полиангиитисом и микроскопским полиангиитисом била је 2,00 на 100 пацијената-година на датум завршетка заједничке студије (када је последњи пацијент завршио период праћења).-Горе). На основу стандардизованог односа инциденције, чини се да је инциденција малигних болести слична оној која је раније пријављена код пацијената са васкулитисом повезаним са АНЦА.
Кардиоваскуларне нежељене реакције
Срчани догађаји су се јављали са стопом од приближно 273 на 100 пацијент-година (95 % ЦИ 149-470) у шестомесечној примарној крајњој тачки. Озбиљна учесталост срчаних догађаја била је 2,2 на 100 пацијент-година (95 % ЦИ 3-15) Најчешће пријављени нежељени догађај била је тахикардија (4%) и атријална фибрилација (3%) (видети одељак 4.4).
Неуролошки догађаји
Пријављени су случајеви синдрома постериорне реверзибилне енцефалопатије (ПРЕС) / синдрома постериорне реверзибилне леукоенцефалопатије (РПЛС). Знаци и симптоми укључују поремећаје вида, главобоље, нападе и измењени ментални статус, са или без придружене хипертензије. Дијагноза ПРЕС / РПЛС захтева потврду сликањем мозга. Описани случајеви су имали познате факторе ризика за ПРЕС / РПЛС, укључујући основну болест пацијената, хипертензију, имуносупресивну терапију и / или хемотерапију.
Реактивација хепатитиса Б.
Мали број случајева реактивације хепатитиса Б, неки са смртним исходом, забележен је код пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом лечених МабТхером у постмаркетиншком окружењу.
Хипогамаглобулинемија
Хипогамаглобулинемија (ИгА, ИгГ или ИгМ испод доње границе нормале) примећена је код пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом леченим МабТхером. У шестомесечној, вишецентричној, рандомизираној, двоструко слепој, активно контролисаној студији не инфериорности у групи МабТхера, 27%, 58%и 51%пацијената са нормалним основним нивоом имуноглобулина имало је низак ниво ИгА, ИгГ и ИгМ, респективно, у поређењу са 25%, 50% и 46% групе циклофосфамида. Повећана стопа укупних инфекција или озбиљних инфекција није примећена код пацијената са ниским нивоом ИгА, ИгГ или ИгМ.
Неутропенија
У мултицентричној, рандомизованој, двоструко слепој, активно контролисаној студији неинфериорности контролисане МабТхере за грануломатозу са полиангиитисом и микроскопским полиангиитисом, 24% пацијената у групи МабТхера (појединачни циклус) и 23% пацијената у групи са циклофосфамидом развили су неутропенију ЦТЦ степена 3 или више. Неутропенија није била повезана са примећеним порастом озбиљних инфекција код пацијената лечених МабТхером. Учинак вишеструких курсева лека МабТхера на развој неутропеније код пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом није проучаван у клиничким студијама.
Поремећаји коже и поткожног ткива:
Врло ретко су пријављиване епизоде токсичне епидермалне некролизе (Лиелл-ов синдром) и Стевенс-Јохнсоновог синдрома, од којих су неки са смртним исходом.
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика лека. Здравствени радници се моле да пријаве све сумње на нежељене реакције путем националног система за пријављивање.
04.9 Предозирање
Постоји ограничено искуство из клиничких испитивања на људима са дозама већим од оних одобрених за интравенозну формулацију МабТхере. Највиша интравенозна доза МабТхере тестирана на људима до сада је 5000 мг (2250 мг / м2), у студији повећања дозе у пацијенти са хроничном лимфоцитном леукемијом. Нису идентификовани други знакови безбедности.
Пацијенти који доживе предозирање треба одмах прекинути инфузију и пажљиво их пратити.
Након стављања лека у промет пријављено је пет случајева предозирања МабТхером. Три од ових случајева нису пријавили нежељене догађаје. Два пријављена нежељена догађаја били су симптоми слични грипу са дозом од 1,8 г ритуксимаба и фатална респираторна инсуфицијенција са дозом од 2 г ритуксимаба.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: антинеопластична средства, моноклонска антитела, АТЦ ознака: Л01Кс Ц02.
Ритуксимаб се специфично везује за ЦД20 трансмембрански антиген, не-гликозилирани фосфопротеин, који се налази на лимфоцитима пре-Б и зрелим лимфоцитима Б. Антиген је изражен на више од 95% свих не-Ходгкинових ћелијских лимфома Б (НХЛ).
ЦД20 се налази у нормалним и неопластичним Б ћелијама, али не и у хематопоетским матичним ћелијама, про-Б ћелијама, нормалним плазма ћелијама или другим нормалним ткивима. Антиген се не интернализује након везивања антитела и не дисеминише са ћелијске површине. ЦД20 не циркулише у крви као слободан антиген и стога се не такмичи са везивањем антитела. Фаб домен ритуксимаба везује се за ЦД20 антиген на Б лимфоцитима . и Фц домен могу активирати ефекторске функције имунолошког система са циљем да изазову лизу ћелија Б. Могући механизми ефекта посредоване лизе ћелија укључују комплемент-зависну цитотоксичност (ЦДЦ) кроз везивање за Ц1к и ћелијску цитотоксичност зависну од антитела (АДЦЦ ) посредовани једним или више Фцγ рецептора на површини гранулоцита, макрофага и НК ћелија .. Такође је показано да везивање ритуксимаба за ЦД20 антиген на Б лимфоцитима изазива ћелијску смрт апоптозом.
Број периферних Б ћелија је пао испод нормалног након примене прве дозе МабТхере. Код пацијената лечених од хематолошких карцинома, опоравак Б ћелија почиње у року од 6 месеци од лечења и генерално се враћа на нормалне нивое у року од 12 месеци по завршетку терапије, иако опоравак може бити дужи код неких пацијената (са средњом стопом опоравка од 23 месеца након индукције) терапија). Код пацијената са реуматоидним артритисом, примећено је тренутно исцрпљивање Б ћелија периферне крви након две инфузије од по 1000 мг МабТхере, одвојене размаком од 14 дана. Број периферних Б ћелија почиње да расте од 24. недеље, а знаци опоравка се виде код већине пацијената од 40. недеље, и када се МабТхера даје као монотерапија и када се даје у комбинацији са метотрексатом. Мали проценат пацијената доживео је продужено исцрпљивање периферних Б ћелија 2 године или више након последње дозе МабТхере. Код пацијената са грануломатозом са полиангиитисом или микроскопским полиангиитисом, број Б ћелија периферне крви се смањио на 2, и остао на овом нивоу у већина пацијената до Временска тачка 6 месеци. Већина пацијената (81%) показала је знакове реконституције Б ћелија са бројем> 10 ћелија / μл у року од 12 месеци, достижући 87% пацијената до 18. месеца.
Клиничко искуство у не-Ходгкиновом лимфому и хроничној лимфоцитној леукемији
Фоликуларни лимфом
Монотерапија
Почетни третман, недељно за 4 дозе
У кључној студији, 166 пацијената са повратним или хеморезистентним НХЛ ниског степена или фоликуларних Б-ћелија примило је 375 мг / м2 МабТхере као интравенозну инфузију једном недељно током четири недеље. Проценат укупних одговора (ОРР) у популацији процењен према „намера да се третира анализа (ИТТ) је био 48% (95% ИЗ 41% - 56%) са 6% потпуних одговора (ЦР) и 42% парцијалних одговора (ПР). Просечна пројекција времена до прогресије (ТТП) за пацијенте са одговором била је 13,0 месеци. У анализи подгрупа, ОРР је био већи код пацијената са ИВФ хистолошким подтиповима Б, Ц и Д у поређењу са онима са хистолошким подтипом А ИВФ (58% вс 12%), код пацијената са већим пречником лезије 7 цм (53% вс 38% ) и код пацијената са хемосензитивним релапсом у односу на оне са хеморезистентним релапсом (дефинисано као трајање одговора
ОРР код пацијената који су претходно лечени аутологном трансплантацијом коштане сржи (АБМТ) износио је 78% наспрам 43% код пацијената који претходно нису лечени АБМТ -ом. Старост, пол, степен лимфома, почетна дијагноза, присуство или одсуство гломазне болести, Нормалан или повишен ЛДХ , присуство екстранодалне болести није имало статистички значајан ефекат (Фисхеров егзактни тест) на одговор на МабТхеру. Статистички значајна корелација је идентификована између стопе одговора и захваћености коштане сржи. 40% пацијената са захваћеном коштаном сржи одговорило је наспрам 59% пацијената без захваћености коштане сржи (п = 0,0186). Овај налаз није поткрепљен такозваном анализом „степенасте логистичке регресије“ у којој су као фактори прогностике идентификовани следећи фактори: хистолошки тип, почетна позитивност бцл-2, резистенција на последњу хемотерапију и гломазна болест.
Почетни третман, недељно за 8 доза
У мултицентричној студији са једном руком, 37 пацијената са рецидивом или хеморезистентном, ниско или фоликуларном Б-ћелијском НХЛ-ом примало је МабТхеру 375 мг / м2 као недељну интравенозну инфузију за осам доза. ОРР је био 57% (95% интервал поузданости (ЦИ): 41% - 73%; ЦР 14%, ПР 43%) са средњом пројекцијом ТТП за испитанике од 19,4 месеца (распон од 5,3 до 38,9 месеци).
Почетни третман, гломазна болест, недељно за 4 дозе
У збирци података из 3 студије, 39 пацијената са повратним или хеморезистентним НХЛ-ом, гломазном болешћу (појединачна лезија ≥ 10 цм у пречнику), ниским или фоликуларним Б-ћелијским обољењем, примало је МабТхеру 375 мг / м2 као недељну интравенозну инфузију током четири дозама. ОРР је био 36% (95% ЦИ 21% - 51%; ЦР 3%, ПР 33%) са средњом ТТП за пацијенте са одзивом од 9,6 месеци (распон 4,5 - 26,8 месеци).
Понављање, недељно за 4 дозе
У мултицентричној студији са једном руком, 58 пацијената са повратком или хеморезистентном НХЛ ниског степена или фоликуларних Б-ћелија који су постигли објективни клинички одговор на претходни ток лечења МабТхером, повучено је са 375 мг / м2 МабТхере као недељна интравенозна инфузија за четири дозе. Три од ових пацијената су пре уписа добили два курса МабТхере и тако су добили трећи курс у студији. Два пацијента су повучена два пута у студији. За 60 поновљених третмана у студији, ОРР је био 38% (95% ЦИ 26% - 51%; 10% ЦР, 28% ПР) са средњом пројекцијом ТТП за пацијенте са одзивом од 17,8 месеци (распон 5, 4-26,6) . Ови подаци су бољи од ТТП добијеног након првог курса МабТхере (12,4 месеца).
Почетни третман, у комбинацији са хемотерапијом
У рандомизованом отвореном клиничком испитивању, укупно 322 претходно нелечена пацијента са фоликуларним лимфомом рандомизована су на ЦВП хемотерапију (циклофосфамид 750 мг / м2, винкристин 1,4 мг / м2 до највише 2 мг првог дана и преднизолон 40 мг / м2 / дан у данима 1-5) сваке 3 недеље током 8 циклуса или МабТхера 375 мг / м2 у комбинацији са ЦВП (Р-ЦВП). МабТхера је давана првог дана сваког циклуса лечења. Укупно 321 пацијент (162 Р-ЦВП, 159 ЦВП) је примило терапију и анализирано је на ефикасност. Медијан праћења пацијената био је 53 месеца. Р-ЦВП је резултирао значајном користи у односу на ЦВП за примарну крајњу тачку, односно време до неуспеха лечења (27 месеци наспрам 6,6 месеци, стр.
Разлика између група лечених у укупном преживљавању показала је значајну клиничку разлику (п = 0,029, лог-ранк тест стратификован по центрима): стопа преживљавања од 53 месеца била је 80,9% за пацијенте у Р-групи. ЦВП у поређењу са 71,1% за пацијенти у ЦВП групи.
Резултати три друга рандомизирана испитивања која су користила МабТхеру у комбинацији са хемотерапијским режимима који нису ЦВП (ЦХОП, МЦП, ЦХВП / Интерферон-α) такође су показала значајна побољшања у стопама одговора, параметрима зависним од времена и укупном преживљавању. Најважнији резултати из све четири студије сажети су у Табели 4.
Табела 4 Сажетак кључних налаза из четири рандомизована испитивања фазе ИИИ која је процењивала корист МабТхере са различитим режимима хемотерапије у фоликуларном лимфому.
ЕФС - Опстанак без догађаја
ТТП - Време до прогресије или смрти
ПФС - Прогрессион Фрее Сурвивал
ТТФ - Време до неуспеха лечења
Проценти ОС - стопе преживљавања у време анализе
Терапија одржавања
Претходно необрађен фоликуларни лимфом
У проспективној, отвореној, међународној, мултицентричној студији фазе ИИИ, 1193 пацијената са претходно нездрављеним узнапредовалим фоликуларним лимфомом примило је индукциону терапију са Р-ЦХОП (н = 881), Р-ЦВП (н = 268) или Р-ФЦМ (н = 44), на основу избора истражитеља. Укупно 1078 пацијената је одговорило на индукциону терапију, од којих је 1018 рандомизовано на одржавање МабТхере (н = 505) или посматрање (н = 513). Две групе лечења биле су добро избалансиране с обзиром на основне карактеристике и статус болести. Третман одржавања са МабТхером састојао се од једне инфузије МабТхере примењене у дози од 375 мг / м2 телесне површине свака 2 месеца до прогресије болести или до 2 године.
Након медијана времена посматрања од 25 месеци од рандомизације, терапија одржавања са МабТхером произвела је клинички значајно и статистички значајно побољшање примарне крајње тачке преживљавања процењене од истраживача (ПФС) у поређењу са посматрањем код пацијената са претходно нелеченим фоликуларним лимфомом (табела 5).
Такође је примећена значајна корист од одржавања МабТхером за секундарне крајње тачке преживљавања без догађаја (ЕФС), време до следећег анти-лимфомског третмана (ТНЛТ), време до следеће хемотерапије (ТНЦТ) и укупну стопу одговора (ОРР) (табела 5) . Резултати примарне анализе потврђени су дужим праћењем (средње време посматрања: 48 месеци и 73 месеца), а ажурирани резултати додати су у Табелу 5 ради илустрације поређења између периода праћења од 25, 48 и 73 месеци.
Табела 5 Фаза одржавања: Сажетак резултата ефикасности МабТхере вс. посматрање након 73 месеца просечног времена посматрања (у поређењу са резултатима примарне анализе засноване на средњем времену посматрања од 25 месеци и ажурираном анализом заснованом на средњем времену посматрања од 48 месеци)
* На крају одржавања / посматрања; # п-вредности из хи-квадрат теста.
Главне вредности одговарају средњем времену посматрања од 73 месеца, вредности у курзиву у заградама одговарају 48 месеци просечног времена посматрања, а вредности у заградама одговарају средњем времену посматрања од 25 месеци (примарно анализа).
ПФС: преживљавање без прогресије; ЕФС: преживљавање без догађаја; ОС: општи опстанак; ТНЛТ: време до следећег третмана против лимфома; ТНЦТ: време до следећег хемотерапијског третмана; ОРР: укупна стопа одговора: НР: недостижан у време одрезати клинички; ИЛИ: однос шанси.
Терапија одржавања са МабТхером дала је доследну корист у свим тестираним подгрупама: пол (мушко, женско), старост (= 60 година), ФЛИПИ скор (= 3), индукциона терапија (Р-ЦХОП, Р-ЦВП или Р-ФЦМ) и без обзира на то квалитета одговора на индукциону терапију (ЦР, ЦРу или ПР). Истраживачке анализе користи од одржавања показале су мање изражен ефекат код старијих пацијената (> 70 година старости), међутим величина узорка је била мала.
Релаксирани / ватростални фоликуларни лимфом
У проспективној, отвореној, међународној, мултицентричној студији фазе ИИИ, 465 пацијената са рецидивом / резистентним фоликуларним лимфомом је рандомизовано у првој фази на индукциону терапију са ЦХОП (циклофосфамид, доксорубицин, винкристин и преднизолон; н = 231) о МабТхера плус ЦХОП (Р-ЦХОП, н = 234). Две групе лечења биле су добро избалансиране с обзиром на основне карактеристике и статус болести. Укупно 334 пацијента који су постигли потпуну или делимичну ремисију након индукционе терапије рандомизирано је у другу фазу на терапију одржавања МабТхере (н = 167) или посматрање (н = 167). Третман одржавања са МабТхером састојао се од једне инфузије МабТхере при 375 мг / м2 телесне површине примењене свака 3 месеца до прогресије болести или до две године.
Коначна анализа ефикасности обухватила је све пацијенте рандомизоване у оба дела студије. Након средњег времена посматрања од 31 месеца за пацијенте рандомизоване у фази индукције, Р-ЦХОП је значајно побољшао прогнозу пацијената са лимфомом. Фоликуларни релапс / отпоран у поређењу са ЦХОП (види табелу 6).
Табела 6 Фаза индукције: листа резултата ефикасности ЦХОП-а у поређењу са Р-ЦХОП (средње време посматрања 31 месец).
1) Процена је израчуната са релативним ризиком.
2) Последњи одговор тумора према процени истраживача. "Примарни" статистички тест за "одговор" био је тест тренда ЦР у односу на ПР у односу на неодзив (стр
Кратице: НА, није доступно; ОРР: проценат глобалних одговора; ЦР: потпун одговор; ПР: делимичан одговор.
За пацијенте рандомизиране у фазу одржавања студије, средње време посматрања било је 28 месеци од рандомизације до одржавања. Третман одржавања МабТхером резултирао је клинички релевантним и статистички значајним побољшањем примарне крајње тачке, ПФС (време од рандомизације за одржавање до релапса, прогресије болести или смрти), у поређењу само са посматрањем (стр.
Табела 7 Фаза одржавања: листа резултата ефикасности МабТхере у односу на посматрање (28 месеци просечног времена посматрања).
НР: није достигнуто; а: Примењиво само на пацијенте који постигну ЦР.
Корист од одржавања МабТхером потврђена је у свим анализираним подгрупама без обзира на режим индукције (ЦХОП или Р-ЦХОП) или квалитет одговора на индукциони третман (ЦР или ПР) (табела 7). Третман одржавања са МабТхером значајно је продужио медијану ПФС -а код пацијената који су одговорили на индукциону терапију са ЦХОП (средња вредност ПФС -а 37,5 месеци у односу на 11,6 месеци, стр.
Дифузни велики Б-ћелијски не-Ходгкинов лимфом
У рандомизованој, отвореној студији, укупно 399 претходно нелечених старијих пацијената (старости од 60 до 80 година) са дифузним великим Б-ћелијским лимфомом добило је стандардне курсеве ЦХОП хемотерапије (циклофосфамид 750 мг / м2, доксорубицин 50 мг / м2, винкристин 1,4 мг / м2 до максимално 2 мг дат 1. дана, и преднизолон 40 мг / м2 / дан дат од 1. до 5. дана) сваке 3 недеље током осам циклуса, или МабТхера 375 мг / м2 заједно са ЦХОП (Р -СЕЦКАТИ).
МабТхера је примењена првог дана циклуса лечења.
Коначна анализа података о ефикасности обухватила је све рандомизоване пацијенте (197 ЦХОП, 202 Р-ЦХОП) и представила је просечно трајање праћења од приближно 31 месеца.Две групе лечења биле су добро избалансиране у односу на карактеристике болести и статус на почетку. Коначна анализа је потврдила да је лечење Р-ЦХОП-ом повезано са клинички релевантним и статистички значајним побољшањем у трајању преживљавања без догађаја (примарни параметар ефикасности; догађаји су били смрт, рецидив или прогресија лимфома, или прелазак на нову терапију против лечење лимфома) (п = 0,0001). Каплан-Меиерова процена средњег трајања преживљавања без догађаја била је 35 месеци у групи са Р-ЦХОП наспрам 13 месеци у групи са ЦХОП-ом, што представља смањење ризика за 41%. Након 24 месеца, укупна процена преживљавања била је 68,2% у групи са Р-ЦХОП наспрам 57,4% у групи са ЦХОП. Накнадна анализа укупног трајања преживљавања, изведена са средњим трајањем праћења од 60 месеци, потврдила је корист лечења Р-ЦХОП над ЦХОП (п = 0,0071), што представља смањење ризика за 32%.
Анализом свих секундарних параметара (стопа одговора, преживљавање без прогресије, преживљавање без болести, трајање одговора) потврђена је ефикасност лечења Р-ЦХОП у поређењу са ЦХОП-ом. Стопа потпуног одговора након 8 циклуса била је 76,2% у групи Р-ЦХОП и 62,4% у групи ЦХОП (п = 0,0028). Ризик од прогресије болести смањен је за 46%, а ризик од рецидива за 51%.
У свим подгрупама пацијената (пол, старост, ИПИ прилагођен узрасту, стадијум Анн Арбор, ЕЦОГ, β2-микроглобулин, ЛДХ, албумин, симптоми Б, гломазна болест, екстранодална места, захваћеност коштане сржи), омјери ризика преживљавања без догађаја и укупно преживљавање (РЦХОП у поређењу са ЦХОП) било је мање од 0,83 и 0,95 респективно. Р-ЦХОП је био повезан са побољшаном прогнозом и код пацијената високог и ниског ризика према ИПИ прилагођеној старости.
Клинички лабораторијски подаци
Нису примећени одговори код 67 пацијената који су подвргнути тесту хуманих антитела на миша (ХАМА) .Од 356 пацијената који су подвргнути ХАЦА тесту, 1,1% (4 пацијента) је позитивно.
Хронична лимфоцитна леукемија
У две рандомизоване отворене студије, укупно 817 претходно нелечених пацијената са КЛЛ и 552 пацијента са релапсираним / рефракторним ХЛЛ-ом рандомизовано је на хемотерапију ЦФ (флударабин 25 мг / м2, циклофосфамид 250 мг / м2, дани 1-3) сваки 4 недеље током 6 циклуса или МабТхера у комбинацији са ФЦ (Р-ФЦ). МабТхера је давана у дози од 375 мг / м2 током првог циклуса, један дан пре хемотерапије, и у дози од 500 мг / м2 првог дана сваког следећег циклуса лечења. Пацијенти су искључени из студије релапса / рефракторне ЦЛЛ ако су претходно били лечени моноклонским антителима или су били рефракторни (дефинисани као неуспех да се постигне делимична ремисија током најмање 6 месеци) на флударабин или било који аналог нуклеозида. Укупно 810 пацијената (403 Р-ФЦ, 407 ФЦ) за прву линију испитивања (Табела 8а и Табела 8б) и 552 пацијента (276 Р-ФЦ, 276 ФЦ) за релапс / рефракторну студију (Табела 9), анализирани су на ефикасност.
У студији прве линије, након медијана времена посматрања од 48,1 месеца, медијана ПФС-а била је 55 месеци у Р-ФЦ групи и 33 месеца у ФЦ групи (п
Свеукупна анализа преживљавања показала је значајну корист од лечења РФЦ-ом у поређењу само са хемотерапијом ЦФ (п = 0,0319, лог-ранк тест) (табела 8а). Корист од ПФС-а доследно је примећена у већини подгрупа пацијената анализираних према основном ризику од болести (посебно Бинет АЦ фазе ) (табела 8б).
Табела 8а Лечење прве линије хроничне лимфоцитне леукемије Опис резултата ефикасности МабТхере плус ЦФ вс. Само ХР - просечно време посматрања 48,1 месеца.
Проценат одговора и проценат ЦР анализираних према хи-квадрат тесту. НР: није достигнуто; н.а.: не
примењив.
*: Примењиво само на пацијенте који добију ЦР, нПР, ПР.
**: Примењиво само на пацијенте који постигну ЦР.
Табела 8б Лечење прве линије хроничне лимфоцитне леукемије Однос опасности преживљавања без прогресије болести према Бинетовом стадијуму (ИТТ)-просечно време посматрања 48,1 месеца
ЦИ: Интервал поверења.
У студији релапса / рефракторности, медијан преживљавања без прогресије болести (примарна крајња тачка) било је 30,6 месеци у Р-ФЦ групи и 20,6 месеци у ФЦ групи (п = 0,0002, лог-ранк тест).
Корист од ПФС -а је примећена у скоро свим подгрупама пацијената анализираних према основном ризику од болести. Забележено је благо, али не значајно побољшање укупног преживљавања у групи са Р-ФЦ у поређењу са групом ФЦ.
Табела 9 Лечење релапсирајуће / рефракторне хроничне лимфоцитне леукемије - опис резултата ефикасности МабТхере плус ХР само са ХР (просечно време посматрања 25,3 месеца).
Проценат одговора и проценат ЦР анализираних према хи-квадрат тесту.
*: примењиво само на пацијенте који добију ЦР, нПР, ПР; НР = није достигнуто; н.а. = није применљиво.
**: Примењиво само на пацијенте који постигну ЦР.
Такође, резултати других студија подршке које су користиле МабТхеру у комбинацији са другим режимима хемотерапије (укључујући ЦХОП, ФЦМ, ПЦ, ПЦМ, бендамустин и кладрибин) за лечење претходно нелечених и / или рецидивираних пацијената са ЦЛЛ / рефракторном, показали су „висок проценат глобалних одговора са користима у процентима ПФС, мада са нешто већом токсичношћу (посебно мијелотоксичношћу). Ове студије подржавају употребу МабТхере са било којом хемотерапијом.
Подаци приближно 180 пацијената који су претходно били лечени МабТхером показали су клиничку корист (укључујући ЦР) и подржавају поновно лечење МабТхером.
Педијатријска популација
Европска агенција за лекове одустала је од обавезе достављања резултата студија са МабТхером у свим подскупинама педијатријске популације у фоликуларном лимфому и хроничној лимфоцитној леукемији. Видети одељак 4.2 за информације о педијатријској употреби.
Клиничко искуство у реуматоидном артритису
Ефикасност и безбедност МабТхере у ублажавању симптома и знакова реуматоидног артритиса код пацијената са неадекватним одговором на инхибиторе ТНФ-а доказани су у кључној, рандомизованој, контролисаној, двоструко слепој, мултицентричној студији (Студија 1).
Студија 1 је проценила 517 пацијената са неадекватним одговором или нетолеранцијом на један или више лекова инхибитора ТНФ -а. Пацијенти који испуњавају услове имали су „активни реуматоидни артритис, дијагностикован према критеријумима Америчког колеџа за реуматологију (АЦР)“. МабТхера је давана као 2 и.в. инфузије. одвојене размаком од 15 дана. Пацијенти су примали 2 к 1000 мг интравенске инфузије МабТхере или плацеба у комбинацији са МТКС. Сви пацијенти су истовремено примали 60 мг преднизолона орално 2. до 7. дана и 30 мг 8. до 14. дана након прве инфузије. Примарни крајњи циљ био је удео пацијената који су постигли АЦР20 одговор у 24. недељи. Пацијенти су праћени дуже од 24 недеље ради постизања дугорочних циљева, што је укључивало радиографску процену у 56. и 104. недељи. Током овог периода, "81% пацијената из оригиналне плацебо групе која је примала МабТхеру између 24. и 56. недеље, као део „отворене“ продужене студије протокола.
Студије са МабТхером код пацијената са стадијумом артритиса рано (пацијенти који претходно нису лечени метотрексатом и пацијенти са неадекватним одговором на метотрексат, али још увек нису лечени инхибиторима ТНФ-алфа) постигли су своје примарне циљеве. МабТхера није индикована за ове пацијенте јер су безбедносни подаци о дуготрајном лечењу МабТхером недовољни, посебно у погледу ризика од развоја рака или ПМЛ-а.
Резултати активности болести
МабТхера у комбинацији са метотрексатом значајно је повећала удео пацијената који су постигли побољшање одговора од најмање 20% у односу на пацијенте који су лечени само метотрексатом (табела 10). У свим кључним студијама, корист од лечења била је слична код пацијената без обзира на старост, пол, телесну површину, расу, број претходних третмана или статус болести.
Клинички и статистички значајна побољшања такође су примећена у свим појединачним компонентама одговора на АЦР (број болних и отечених зглобова, укупна процена пацијената и лекара, индекс инвалидитета (ХАК), процена бола и Ц реактивни протеин (мг / дл)).
Табела 10 Резултати клиничког одговора у студији 1 примарне крајње тачке (ИТТ популација).
† Резултат након 24 недеље.
Значајна разлика у односу на плацебо + МТКС ал Временска тачка примарно: *** п ≤ 0,0001.
Пацијенти лечени МабТхером у комбинацији са метотрексатом имали су значајно веће смањење ДАС28 (Оцена активности болести) у поређењу са пацијентима који су лечени само метотрексатом (табела 9). Слично, у свим студијама одговор ЕУЛАР -а (Европска лига против реуматизма) добро до умерено постигло је значајно више пацијената лечених МабТхером и метотрексатом него пацијената лечених само метотрексатом (Табела 10).
Радиолошки одговор
Радиолошки је утврђено оштећење структурних зглобова и изражено као промјена у модификованој укупној оштрини (мТСС) и њеним компонентама, оцјени ерозије и оцјени смањења зглобова.
У студији 1, спроведеној код субјеката са неадекватним одговором или нетолеранцијом на терапије са једним или више ТНФ антагониста који су примали МабТхеру у комбинацији са метотрексатом, пацијенти су имали 56. недељу дана значајно мању радиографску прогресију од оних који су првобитно примали сам метотрексат. Од пацијената који су првобитно лечени само метотрексатом, 81% је примило МабТхеру као терапију спашавања између 16. и 24. недеље или као продужетак студије пре 56. недеље. Осим тога, већи проценат пацијената који су примили „првобитни третман са МабТхером / МТКС није показао прогресију ерозивних лезија током 56 недеља (табела 11).
Табела 11 Радиолошки резултати након 1 године (мИТТ популација)
150 пацијената који су првобитно рандомизирани у студији 1 за плацебо + МТКС примили су најмање један курс РТКС + МТКС
у години.
* стр
Инхибиција брзине прогресије оштећења зглобова такође је дугорочно примећена. Двогодишња радиографска анализа у Студији 1 показала је значајно смањење прогресије структурних оштећења зглобова код пацијената који су примали МабТхеру у комбинацији са метотрексатом у поређењу са онима који су примали само метотрексат и значајно већи проценат пацијената без прогресије оштећења зглобова дуже од 2 године.
Физичка функција и резултати квалитета живота
Значајно смањење индекса инвалидитета (ХАК-ДИ) и астеније (ФАЦИТ-умор) примећено је код пацијената лечених МабТхером у поређењу са пацијентима који су лечени само метотрексатом. Удео пацијената лечених леком МабТхера који су показали клинички важну минималну разлику (МЦИД) у ХАК-ДИ (дефинисаном као смањење индивидуалног укупног скора> 0,22) такође је био већи од оног код пацијената који су примали само метотрексат. (Табела 12) .
Значајно побољшање здравља у смислу квалитета живота показано је значајним побољшањем и резултата физичког здравља (ПХС) и резултата менталног здравља (МХС) СФ-36. Осим тога, значајно већи проценат пацијената постигао МЦИД за ове резултате (Табела 12).
Табела 12 Физичка функција и исходи квалитета живота у 24. недељи у Студији 1.
† Резултати у 24. недељи.
Значајна разлика у односу на плацебо Временска тачка примарно: * стр
МЦИД ХАК-ДИ ≥0,22, МЦИД СФ-36 ПХС> 5,42, МЦИД СФ-36 МХС> 6,33.
Ефикасност код серопозитивних пацијената са аутоантителима (РФ и или анти-ЦЦП)
Реуматоидни фактор (РФ) и / или циклични пептид цитрулинат (анти-ЦЦП) серопозитивни пацијенти који су лечени МабТхером у комбинацији са метотрексатом показали су бољи одговор од пацијената негативних на оба.
Резултати ефикасности код пацијената лечених леком МабТхера анализирани су на основу статуса аутоантитела пре почетка лечења. У 24. недељи, пацијенти који су на почетку били серопозитивни на РФ и / или анти-ЦЦП имали су значајно веће резултате у постизању АЦР20 и 50 одговора од серонегативних пацијената (п = 0,0312 и п = 0,0096) (табела 13). Ови резултати су поновљени у 48. недељи, где је серопозитивност антитела значајно повећала вероватноћу постизања АЦР70. У 48. недељи, серопозитивни пацијенти имају 2-3 пута већу вероватноћу да постигну АЦР одговор од серонегативних пацијената. Серопозитивни су такође имали значајно веће смањење ДАС28 -ЕСР од серонегативних пацијената.
Табела 13 Резиме ефикасности заснован на статусу аутоантитела на почетку.
Значајни нивои су дефинисани као * стр
Дуготрајна ефикасност са поновљеним курсевима терапије
Третман са МабТхером у комбинацији са метотрексатом у више циклуса резултирао је драматичним побољшањем клиничких знакова и симптома реуматоидног артритиса, на шта указују одговори АЦР, ДАС28-ВЕС и ЕУЛАР који су били евидентни у свим испитиваним популацијама. Они су уочени. Значајна побољшања у физичке функције како показује ХАК-ДИ скор и проценат пацијената који су постигли МЦИД за ХАК-ДИ.
Резултати клиничке лабораторије
У клиничким студијама, укупно 392 од 3095 (12,7%) пацијената са реуматоидним артритисом било је позитивно на ХАЦА након третмана са МабТхером. Код већине пацијената почетак ХАЦА није био повезан са клиничким погоршањем или повећаним ризиком од реакција на наредне инфузије. Присуство ХАЦА може бити повезано са погоршањем инфузионих или алергијских реакција након друге инфузије наредних курсева.
Педијатријска популација
Европска агенција за лекове одустала је од обавезе достављања резултата студија са МабТхером у свим подгрупама педијатријске популације са аутоимунским артритисом. Видети одељак 4.2 за информације о педијатријској употреби.
Клиничко искуство у грануломатози са полиангиитисом (Вегенер -овим) и у микроскопском полиангиитису Укупно 197 пацијената старих 15 и више година са активним и тешким полиангиитисом са полиангиитисом (75%) и микроскопским полиангиитисом (24%) било је уписано и лечено у мултицентричном центру, рандомизована, двоструко слепа, активна упоредна студија инфериорности.
Пацијенти су рандомизирани у односу 1: 1 да примају орални циклофосфамид дневно (2 мг / кг / дан) током 3-6 месеци или МабТхеру (375 мг / м2) једном недељно током 4 недеље. Сви пацијенти у групи са циклофосфамидом су примали терапију одржавања азатиоприном током праћења. Пацијенти на обе руке примали су 1000 мг интравенског болусног метилпреднизолона (или друге еквивалентне дозе глукокортикоида) дневно током 1 до 3 дана, након чега је уследила орална примена преднизона (1 мг / кг / дан, не преко 80 мг / дан). Смањење преднизона је завршено у року од 6 месеци од почетка студијског лечења. Примарна мера крајње тачке била је постизање потпуне ремисије након 6 месеци дефинисано као Активност васкулитиса у Бирмингхаму за Вегенерову грануломатозу (БВАС / ВГ) 0, и одсуство терапије глукокортикоидима. Стандардна граница неинфериорности за разлику између третмана била је 20%. Студија је показала не инфериорност МабТхере према циклофосфамиду за потпуну ремисију (ЦР) након 6 месеци (табела 14). Ефикасност је примећена и код новооткривених пацијената и код пацијената са рецидивирајућом болешћу (табела 15).
Табела 14 Проценат пацијената који су постигли потпуну ремисију за 6 месеци (популација намера да се лечи *).
Табела 15 Потпуна ремисија након 6 месеци према статусу болести.
У најгорем случају атрибуција се примењује на пацијенте са подацима који недостају.
Потпуна ремисија са 12 и 18 месеци
У групи МабТхера 48% пацијената постигло је ЦР са 12 месеци, а 39% пацијената са 18 месеци. Код пацијената лечених циклофосфамидом (након чега следи азатиоприн за одржавање потпуне ремисије), 39% пацијената је постигло ЦР са 12 месеци и 33% пацијената са ЦР са 18 месеци. Од 12. до 18. месеца, примећено је 8 рецидива у групи МабТхера у поређењу са 4 у групи са циклофосфамидом.
Повлачење уз МабТхеру
На основу пресуде истраживача, 15 пацијената је добило други курс терапије МабТхером за лечење релапса болести која се догодила између 6 и 18 месеци након првог курса терапије МабТхером. Ограничени подаци из тренутне студије искључују било какве закључке о ефикасности накнадни курсеви МабТхере код пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом.
Континуирана имуносупресивна терапија може бити посебно прикладна за пацијенте са ризиком од рецидива (нпр. Са претходним релапсима и грануломатозом са полиангиитисом у анамнези, или за пацијенте са реконституцијом Б-ћелија поред ПР3-АНЦА током праћења). Када се постигне ремисија са МабТхером, може се размотрити наставак имуносупресивне терапије за спречавање рецидива. Ефикасност и безбедност МабТхере у терапији одржавања нису утврђене.
Лабораторијска испитивања
Укупно 23/99 (23%) пацијената лечених МабТхером у студији било је позитивно на ХАЦА у року од 18 месеци. Ниједан од 99 пацијената лечених МабТхером није био ХАЦА позитиван на скринингу. Клинички значај развоја ХАЦА код пацијената лечених МабТхером није јасан.
05.2 "Фармакокинетичка својства
Не-Ходгкинов лимфом
На основу "популационе фармакокинетичке анализе 298 пацијената са НХЛ -ом који су примили" једнократну или вишекратну инфузију МабТхере као појединачног лека или у комбинацији са ЦХОП терапијом (дозе МабТхере су се користиле у распону од 100 до 500 мг / м2), типичне процене популације за неспецифични клиренс (ЦЛ1), специфични клиренс (ЦЛ2) са вероватним доприносом Б ћелија или туморске масе, и запремина дистрибуције централног одељка (В1) износили су 0,14 л / дан, 0,59 Л / дан и 2,7 Л, респективно. Медијан процењеног терминалног полувремена елиминације МабТхере био је 22 дана (распон: 6,1-52 дана). Основни број ЦД19-позитивних ћелија и пречник мерљивих туморских лезија делимично су допринели варијабилности ЦЛ2 МабТхере, што се види из података из 161 пацијенти који су узимали 375 мг / м2 као интравенозну инфузију током 4 недељне дозе.Пацијенти са већим бројем ћелија позитивних на ЦД19 или већим туморским лезијама имали су већи ЦЛ2. Међутим, велика компонента међуиндивидуалне варијабилности остала је за ЦЛ2 након корекције за ЦД19 -позитиван број ћелија и пречник туморске лезије. В1 је варирао у зависности од површине тела (Површина тела, БСА) и ЦХОП терапију. Ова варијабилност у В1 (27,1% и 19,0%) одређена распоном БСА (1,53 до 2,32 м2) и истовременом ЦХОП терапијом била је релативно мала. Старост, пол и учинак Статус СЗО није имао утицаја на фармакокинетику МабТхере. Ово анализа сугерише да прилагођавање дозе МабТхере са било којом од процењених коваријата вероватно неће резултирати значајним смањењем његове фармакокинетичке варијабилности.
МабТхера, примењена као интравенозна инфузија у дози од 375 мг / м2 у недељним интервалима за 4 дозе до 203 пацијента са НХЛ који нису били на терапији МабТхером, резултирала је средњим Цмак после четврте инфузије од 486 мцг / мл (распон: 77,5 - 996, 6 мцг / мл). Ритуксимаб се могао открити у серуму пацијената 3 - 6 месеци након завршетка последњег третмана.
Након примене МабТхере у дози од 375 мг / м2 као и.в. у недељним интервалима за 8 доза до 37 пацијената са НХЛ, средњи Ц се повећавао са сваком следећом инфузијом, у распону од просека од 243 мцг / мЛ (опсег: 16 - 582 мцг / мЛ) након прве инфузије до 550 мцг / мЛ (опсег : 171 - 1177 мцг / мл) након осме инфузије.
Фармакокинетички профил МабТхере, када се примењује као 6 инфузија од 375 мг / м2 у комбинацији са 6 циклуса ЦХОП хемотерапије, био је сличан оном који је примећен само са МабТхером.
Хронична лимфоцитна леукемија
МабТхера је примењена интравенозном инфузијом са дозом првог циклуса од 375 мг / м2 повећаном на 500 мг / м2 за сваки наредни циклус, за 5 доза, у комбинацији са флударабином и циклофосфамидом код пацијената са КЛЛ. Средња вредност Цмак (Н = 15) након пете инфузије од 500 мг / м2 била је 408 мцг / мл (распон 97-764 мцг / мл), а средњи терминални полуживот био је 32 дана (распон 14-62 дана).
Реуматоидни артритис
Након две интравенозне инфузије МабТхере у дози од 1000 мг, у размаку од две недеље, средњи терминални полуживот је био 20,8 дана (распон 8,58 до 35,9 дана), средњи системски клиренс је био 0,23 Л / дан (распон 0,091 до 0,67 Л / дан) дан), а средњи волумен дистрибуције у стабилном стању био је 4,6 Л (распон 1,7 до 7,51 Л). Популација истих података дала је сличне средње вредности за системски клиренс и полувреме елиминације, од 0,26 л / дан и 20,4 дана, редом. Фармакокинетичке анализе популације откриле су да су БСА и пол најзначајније коваријанте за објашњење интериндивидуалне варијабилности фармакокинетичких параметара. Након прилагођавања на БСА, мушки субјекти су имали већи волумен дистрибуције и бржи клиренс од женских субјеката. Фармакокинетичке разлике повезане са полом нису сматране клинички значајним и није било потребно прилагођавање дозе. Нема фармакокинетичких података за пацијенте са бубрежном или јетреном инсуфицијенцијом.
Фармакокинетика ритуксимаба процењивана је након две интравенозне (и.в.) дозе од 500 мг и 1000 мг 1. и 15. дана у четири студије. У свим овим студијама фармакокинетика ритуксимаба је била пропорционална дози у ограниченом распону дозирања. Средња серумска Цмак ритуксимаба након прве инфузије кретала се од 157 до 171 мцг / мЛ за дозу од 2 к 500 мг и између 298 и 341 мцг / мЛ за дозу од 2 к 1000 мг. Након друге инфузије, средња вредност Цмак била је између 183 и 198 мцг / мЛ за дозу 2 у 500 мг и између 355 и 404 мцг / мл за другу дозу је 1000 Просечни полуживот терминалног излучивања био је између 15 и 16 дана за дозу 2 к 500 мг и између 17 и 21 дан за другу дозу је 1000 мг. Цмак је био између 16 и 19%, већи након друге инфузије у поређењу са првом инфузијом за обе дозе.
Фармакокинетика ритуксимаба оцењивана је након два и.в. 500 мг и 1000 мг након поновне обраде у другом циклусу. Просечна серумска Цмак ритуксимаба након прве инфузије кретала се од 170 до 175 мцг / мЛ за дозу 2 к 500 мг и између 317 до 370 мцг / мЛ за дозу 2 к 1000 мг.Након друге инфузије, средња вредност Цмак била је 207 мцг / мЛ за дозу 2 к 500 мг и између 377 и 386 мцг / мЛ за дозу 2 к 1000 мг. Средњи терминални полувреме елиминације после друге инфузије, после другог циклуса, био је 19 дана за дозу 2 к 500 мг и између 21 и 22 дана за дозу 2 к 1000 мг. Фармакокинетички параметри за ритуксимаб били су упоредиви током два курса лечења.
Фармакокинетички параметри у популацији испитаника са неадекватним одговором на антитела на ТНФ, подвргнути истом режиму дозирања (2 к 1000 мг ив, у размаку од 2 недеље), били су слични са просечном максималном серумском концентрацијом од 369 мцг / мл и „пола живот "просечан терминал од 19,2 дана.
Грануломатоза са полиангиитисом и микроскопским полиангиитисом На основу популационе фармакокинетичке анализе података 97 пацијената са грануломатозом са полиангиитисом и микроскопским полиангиитисом који су примали 375 мг / м2 МабТхере једном недељно током четири недеље, просечни терминални полувреме елиминације процењен је на 23 дана (распон 9 до 49 дана). Средњи клиренс и волумен дистрибуције ритуксимаба били су 0,313 л / дан (распон 0,116 до 0,726 л / дан) и 4,50 л (распон 2,25 до 7,39 л), респективно. Чини се да су фармакокинетички параметри ритуксимаба код ових пацијената слични онима код пацијената са реуматоидним артритисом.
05.3 Предклинички подаци о безбедности
Ритуксимаб је био високо специфичан за ЦД20 антиген на ћелијама Б. Студије токсичности за мајмуне циномолгус нису открили никакве ефекте осим очекиваног фармаколошког исцрпљивања Б ћелија у периферној крви и ткиву лимфних чворова.
Еволуцијске студије токсичности проведене су на мајмунима циномолгус са дозама до 100 мг / кг (третман у данима гестације 20-50) и показали су да нема доказа о феталној токсичности због ритуксимаба. Међутим, примећено је исцрпљивање у лимфоидним органима фетуса зависне од дозе Б ћелија фармакологија, која се одржавала до после рођења и била је повезана са смањењем нивоа ИгГ код погођених новорођенчади.Број Б ћелија се вратио у нормалу код ових животиња у року од 6 месеци од рођења и није умањио реакције имунизације.
Стандардни тестови за испитивање мутагености нису спроведени, јер ови тестови нису релевантни за овај молекул. Дуготрајна истраживања на животињама нису спроведена да би се утврдио канцерогени потенцијал ритуксимаба.
Нису спроведена посебна истраживања која би утврдила ефекте ритуксимаба на плодност. Уопштено у студијама токсичности за мајмунециномолгус нису забележени никакви штетни ефекти на мушке или женске репродуктивне органе.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Натријум цитрат
Полисорбат 80
Натријум хлорид
Натријум хидроксид
Хлороводонична киселина
Вода за ињекције
06.2 Некомпатибилност
Нису примећене некомпатибилности између МабТхере и поливинилхлоридних или полиетиленских кеса или опреме за инфузију.
06.3 Период важења
30 месеци
Раствор МабТхере припремљен за инфузију је физички и хемијски стабилан 24 сата на температури између 2 ° Ц и 8 ° Ц, а затим 12 сати на собној температури.
Са микробиолошког становишта, припремљени раствор за инфузију треба одмах употребити. Ако се не употреби одмах, време складиштења и услови складиштења пре употребе су одговорност корисника и обично се не би прекорачили. 24 сата на температури између 2 ° Ц и 8 ° Ц, осим ако је дошло до разблаживања у контролисаним и валидираним асептичним условима.
06.4 Посебне мере предострожности при складиштењу
Чувати у фрижидеру (2 ° Ц - 8 ° Ц). Чувајте контејнер у спољном паковању ради заштите од светлости.
За услове складиштења након разблаживања лека видети одељак 6.3.
06.5 Природа непосредног паковања и садржај паковања
Прозирне стаклене бочице типа И са чепом од бутил гуме која садржи 100 мг ритуксимаба у 10 мл. Паковања од 2 бочице.
06.6 Упутства за употребу и руковање
МабТхера се испоручује у стерилним бочицама за једнократну употребу које не садрже конзервансе.
Аспирирајте, под стерилним условима, потребну количину МабТхере и разблажите је до израчунате концентрације од 1 до 4 мг / мл ритуксимаба у врећицу за инфузију која садржи стерилни, непирогени раствор натријум хлорида 9 мг / мл (0,9%) за ињекције. ), или 5% Д-глукозе у води. Да бисте мешали раствор, полако преокрените кесу како бисте избегли стварање пене. Мора се водити рачуна да се обезбеди стерилност припремљених раствора. Пошто медицински производ не садржи антимикробне конзервансе или бактериостатике, треба се придржавати асептичних техника. Парентералне лекове пре примене треба визуелно проверити на честице или промену боје.
Неискоришћени лек и отпад добијени из овог лека морају се одложити у складу са локалним прописима.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Роцхе Регистратион Лимитед
6 Фалцон Ваи
Схире Парк
Велвин Гарден Цити
АЛ7 1ТВ
УК
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
ЕУ/1/98/067/001
033315019
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 2. јун 1998
Датум последњег обнављања: 2. јун 2008
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
11.0 ЗА РАДИО ДРОГЕ, ПОТПУНИ ПОДАЦИ О ДОСИМЕТРИЈИ ИНТЕРНОГ ЗРАЧЕЊА
12.0 ЗА РАДИО -ЛИЈЕКОВЕ, ДОДАТНА ДЕТАЉНА УПУТСТВА О ПРИМЕРНОЈ ПРИПРЕМИ И КОНТРОЛИ КВАЛИТЕТА













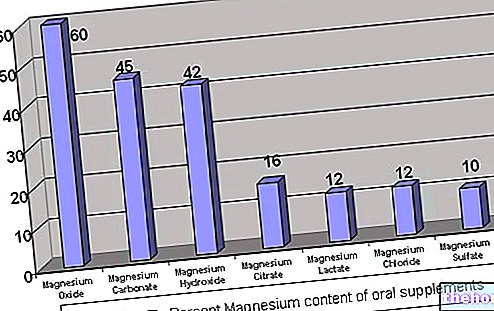





.jpg)