Дефиниција осмозе
Осмоза је спонтани пролаз растварача (који је у биолошким системима обично вода), из раствора у коме су раствори више разблажени до оног у коме су концентрисанији; ово кретање - које се дешава кроз полупропусну мембрану - наставља се све док се не постигне равнотежна ситуација, у којој оба раствора добијају и одржавају исту концентрацију.
Практичан пример

Да бисмо боље разјаснили појам осмозе, замислимо да имамо посуду подељену у два одељка једнаке запремине (А и Б) полупропусном мембраном (то јест, пропустљивом само за растварач - у овом случају воду - а не за растворена супстанца). Одељак А се налази водени раствор у коме је растворена кашика глукозе, док у делу Б имамо водени раствор једнаке запремине у коме су растворене три кашике глукозе (стога је концентрисаније). разлика ствара градијент концентрације глукозе на странама мембране, а пошто овај шећер не може да пређе, равнотежа се постиже проласком воде из одељка А (где је глукоза више разблажена) према одељку Б (где је обилнији) ). Ако више волите, такође се може рећи да вода пролази осмозом из раствора у коме је концентрисанија (А) до оног у коме је мање концентрована (Б).
Након овог тока, ниво воде у Б расте и смањује се у А, стварајући одређену разлику у нивоу између њих. Ова појава престаје када два раствора достигну исту концентрацију, а затим је одржавају константном.
Хипотонична, изотонична и хипертонична раствора
Узимајући два раствора са различитом моларном концентрацијом (различит број честица растворених у њима), раствор са најнижом моларном концентрацијом се дефинише као хипотоничан, а концентрованији је хипертоничан. Два решења су уместо тога изотонична (или еквимоларна) када имају исту концентрацију.
У примеру који је управо направљен, раствор Б је хипертоничан (стога садржи више растворених материја) од другог (дефинисан као хипотоничан); стога се под нормалним условима растварач осмозом креће из хипотоничног у хипертонични раствор. Говорили смо о стандардним условима јер је, играјући се са законима физике, могуће преокренути сам појам осмозе и погодовати преласку растварача из најразблаженије концентрације у најконцентрисанију (реверзна осмоза).
Осмотски притисак и реверзна осмоза
Као што је до сада изражено, нето проток растварача - настао осмозом - наставља се све док два раствора не достигну исту концентрацију.Па, овом кретању се може супротставити, зауставити или чак преокренути притиском притиском на одељак са највећом концентрацијом.

У претходном примеру довољно је поставити клип у одељак Б (за који се сећамо да има већу концентрацију) и притиснути га са одређеном силом надоле, како би се олакшао пролаз воде према А; у овом случају говоримо о обрнутом положају осмоза.
Осмотски притисак је притисак који се тачно супротставља проласку растварача кроз полупропусну мембрану; стога је притисак неопходан за сузбијање осмозе.
За оно што је до сада речено, два изотонична раствора имају исти осмотски притисак; стога треба нагласити да осмотски притисак зависи искључиво од броја честица присутних у раствору, а не од њихове природе.
Осмоза и људско тело
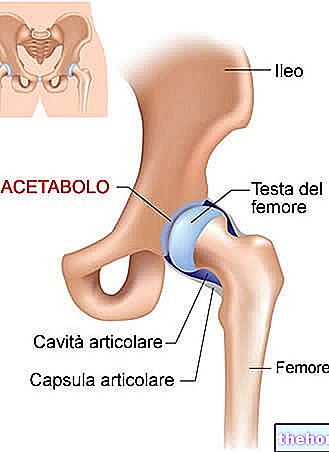
Плазма мембране које окружују ћелије људског тела у ствари су полупропусне мембране које омогућавају директан пролаз, кроз осмозу, малих молекула (попут воде и урее), али не и оних са већом молекулском тежином ( као што су протеини, аминокиселине и шећери). Осмотски баланси у телесним течностима су стога неопходни да би се ћелијама гарантовало оптимално окружење за живот.
Ако узмемо ћелију попут црвеног крвног зрнца и уронимо је у хипотонични раствор, она - осмозом - пролази отицање (узроковано уласком воде), па чак може и да експлодира. Напротив, ако се урони у хипертонични раствор ћелије кроз коју пролази, услед проласка воде ка споља, тешке дехидрације због које долази до набора. На срећу, ћелије у људском организму су уроњене у изотоничне растворе у односу на њихово унутрашње окружење, а постоје различити системи за одржавање ових течности у осмотској равнотежи.
Осмотски притисак и складиштење хране
Размислимо на тренутак о домаћем џему ... шећера се додаје у изобиљу не само ради побољшања укуса, већ и пре свега ради повећања рока трајања. Ипак, шећер је важан елемент за живот многих микроорганизама укључених у разградњу производа. Ову привидну контрадикцију разбија сам концепт осмозе.