Активни састојци: Елтромбопаг
Револаде 12,5 мг филмом обложене таблете
Револаде 25 мг филмом обложене таблете
Револаде 50 мг филмом обложене таблете
Револаде 75 мг филмом обложене таблете
Зашто се користи Револаде? За шта је то?
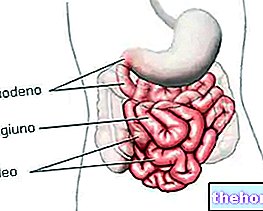
Револаде садржи елтромбопаг, који припада групи лекова који се називају агонисти тромбопоетинских рецептора. Користи се за повећање броја тромбоцита у крви. Тромбоцити су крвне ћелије које служе за смањење или спречавање крварења.
- Револаде се користи за лечење поремећаја згрушавања крви који се назива аутоимуна (идиопатска) тромбоцитопенична пурпура (ИТП) код пацијената (старијих од 1 године) који су већ узимали друге лекове (кортикостероиде или имуноглобулине) који нису били ефикасни.
ИТП је узрокован малим бројем тромбоцита у крви (тромбоцитопенија). Људи са ИТП -ом имају већи ризик од крварења. Симптоми код пацијената са ИТП могу укључивати петехије (мале равне црвене округле мрље на кожи), модрице, епистаксију (крварење из носа), крварење из десни и немогућност контроле крварења услед посекотина или рана.
- Револаде се такође може користити за лечење ниског броја тромбоцита (тромбоцитопеније) код пацијената са вирусом хепатитиса Ц (ХЦВ), ако су имали проблема са нежељеним реакцијама током употребе интерферона. Многи људи са хепатитисом Ц имају низак број тромбоцита. резултат саме болести, али и због неких антивирусних лекова који се користе за лечење. Узимањем Револаде -а може вам бити лакше да завршите цео курс антивирусних лекова (пегинтерферон и рибавирин).
- Револаде се такође може користити за лечење одраслих пацијената са ниским бројем крвних зрнаца узрокованим тешком апластичном анемијом (САА).
Контраиндикације Када се Револаде не сме користити
Немојте узимати Револаде
- ако сте алергични на елтромбопаг или било који други састојак овог лека (шта Револаде садржи).
- Проверите са својим лекаром ако мислите да се ово односи на вас.
Предострожности при употреби Шта треба да знате пре него што узмете лек Револаде
Пре него што узмете Револаде, разговарајте са својим лекаром:
- ако имате проблема са јетром Људи који имају низак број тромбоцита, као и хронично (дуготрајно) узнапредовало обољење јетре изложени су већем ризику од нуспојава, укључујући оштећење јетре и крвне угрушке опасне по живот. Ако ваш лекар сматра да користи од узимања Револаде -а надмашују ризике, бићете помно праћени током лечења.
- ако имате ризик од стварања крвних угрушака у венама или артеријама или ако сте свесни да су крвни угрушци чести у вашој породици.
- Можда сте у повећаном ризику од стварања крвних угрушака:
- ако сте у поодмаклој доби
- ако сте морали дуго да останете у кревету
- ако имате тумор
- ако узимате контрацепцијске пилуле или хормонску надомјесну терапију
- ако сте недавно имали операцију или сте претрпели физичку трауму - ако сте претерано гојазни (гојазни)
- ако сте пушач
- ако имате узнапредовало хронично обољење јетре
- Ако се било шта од наведеног односи на вас, обавестите свог лекара пре почетка лечења. Не бисте требали узимати Револаде осим ако ваш лекар сматра да очекиване користи надмашују ризик од стварања угрушака.
- ако патите од катаракте (замагљивање очног сочива)
- ако имате неки други поремећај крви, као што је мијелодиспластични синдром (МДС). Ваш лекар ће пре него што почнете да узимате Револаде спровести тестове да провери да немате овај поремећај крви. Ако имате МДС и узимате Револаде, ваш МДС се може погоршати.
- Реците свом лекару ако се било шта од овога односи на вас.
Преглед очију
Ваш лекар ће вам препоручити да проверите да ли има катаракте. Ако немате рутинске прегледе ока, ваш лекар ће заказати редован преглед. Такође се може проверити да ли постоји крварење у ретини или око ње (слој ћелија осетљивих на светлост у задњем делу ока).
Биће му потребни редовни испити
Пре него што почнете да узимате Револаде, ваш лекар ће урадити тестове крви како би проверио ваше крвне ћелије, укључујући тромбоците. Ови тестови ће се понављати у интервалима док узимате лек.
Крвни тестови за функцију јетре
Револаде може променити резултате крвних тестова који могу указивати на оштећење јетре - повећање неких јетрених ензима, посебно билирубина и аланин / аспартат трансаминаза. Ако се лечите интерфероном у комбинацији са Револадеом за лечење ниског броја тромбоцита због хепатитиса Ц, неки проблеми са јетром могу се погоршати.
Морате да урадите крвне претраге да бисте проверили функцију јетре пре него што почнете да узимате Револаде и током лечења. Можда ћете морати да престанете да узимате Револаде ако се количина ових ензима превише повећа, или ако се појаве физички знаци оштећења јетре.
- Прочитајте информације "Проблеми са јетром" у одељку 4 ове брошуре
Крвни тестови за број тромбоцита
Ако престанете да узимате Револаде, број тромбоцита ће се вероватно поново смањити у року од неколико дана. Број тромбоцита ће се пратити и лекар ће вас обавестити о одговарајућим мерама предострожности.
Веома висок број тромбоцита може повећати ризик од стварања крвних угрушака, међутим крвни угрушци се такође могу формирати са нормалним или чак ниским бројем тромбоцита. Ваш лекар ће прилагодити дозу Револаде -а како би се осигурало да се број тромбоцита не повећа превише.
Одмах потражите медицинску помоћ ако имате било који од ових знакова крвног угрушка:
- оток, бол или осетљивост у једној нози
- изненадни почетак отежаног дисања, посебно заједно са оштрим болом у грудима или убрзаним дисањем
- бол у стомаку (стомак), отицање абдомена, крв у столици.
Тестови за проверу коштане сржи
Код људи који могу имати проблеме с коштаном сржи, лијекови попут Револадеа могу погоршати тегобе. Знаци промена коштане сржи могу се показати као абнормалности у резултатима крвних претрага. Ваш лекар може да изврши тестове за проверу коштане сржи директно током лечења Револадеом.
Тестови за пробавно крварење
Ако се лечите интерферонским лековима у комбинацији са Револадеом, проверићете да ли има знакова крварења у желуцу или цревима након што престанете да узимате Револаде.
Контрола срца
Ваш лекар ће можда морати да прегледа ваше срце током лечења Револадеом и да вам уради електрокардиограм (ЕКГ).
Деца и адолесценти
Револаде се не препоручује деци млађој од 1 године са ИТП -ом. Такође се не препоручује особама млађим од 18 година са ниским бројем тромбоцита због хепатитиса Ц или тешке апластичне анемије.
Интеракције Који лекови или храна могу променити дејство Револаде -а
Обавестите свог лекара или фармацеута ако узимате, недавно сте узимали или бисте узимали било које друге лекове.
Неки од уобичајених лекова ступају у интеракцију са Револадеом - укључујући лекове и минерале на рецепт и без рецепта. Ови укључују:? антацидни лекови за лечење лоше пробаве, жгаравице или чира на желуцу Када га узимати)
- лекови који се зову статини, за снижавање холестерола
- неки лекови за лечење ХИВ инфекције, као што су лопинавир и / или ритонавир
- циклоспорин који се користи за трансплантацију и имунолошке болести
- минерали попут гвожђа, калцијума, магнезијума, алуминијума, селена и цинка који се могу наћи у витаминима и минералним суплементима (када их узимати)
- лекове као што су метотрексат и топотекан за лечење рака
- Реците свом лекару ако узимате неки од ових лекова. Неки од њих се не могу узети са Револадеом или ће можда бити потребно прилагодити дозу коју узимате или променити време које узимате. Ваш лекар ће прегледати све лекове које узимате и по потреби предложити да их на одговарајући начин замените.
Ризик од крварења је већи ако узимате и лекове за спречавање стварања крвних угрушака. Ваш лекар ће о томе разговарати са вама.
Ако узимате кортикостероиде, даназол и / или азатиоприн, можда ћете морати да узмете нижу дозу или престанете да их узимате док узимате Револаде.
Револуцију уз храну и пиће
Немојте узимати Револаде са пићима или млечним производима и сиром, јер калцијум у млечним производима утиче на апсорпцију лека.
Упозорења Важно је знати да:
Трудноћа и дојење
Немојте користити Револаде ако сте трудни, осим ако вам то није препоручио ваш лекар. Ефекат Револаде током трудноће није познат.
- Реците свом лекару ако сте трудни, мислите да сте можда или планирате трудноћу.
- Користите поуздане методе контрацепције док узимате Револаде да бисте спречили трудноћу
- Ако затрудните док узимате Револаде, обавестите свог лекара.
Немојте дојити док узимате Револаде. Није познато да ли Револаде прелази у мајчино млеко.
- Ако дојите или планирате дојење, обавестите свог лекара.
Вожња и управљање машинама
- Револаде може изазвати вртоглавицу и имати друге нуспојаве које доводе до мање пажње.
- Не управљајте возилима и не рукујте машинама осим ако нисте сигурни да нисте погођени.
Доза, начин и време примене Како се користи Револаде: Дозирање
Увек узимајте овај лек тачно онако како вам је рекао лекар. Ако сте у недоумици, обратите се свом лекару или фармацеуту. Немојте мењати дозу или распоред лека Револаде осим ако вам то не саветује лекар или фармацеут. Док узимате Револаде, лечиће вас лекар са специјалистичким искуством у лечењу вашег стања.
Колико треба узети
За ИТП
Одрасли и деца (од 6 до 17 година) - препоручена почетна доза за ИТП је једна Револаде таблета од 50 мг дневно. Ако сте источноазијског порекла (Кинези, Јапанци, Тајванци, Тајланђани или Корејци), можда ћете морати да почнете са нижом дозом од 25 мг.
Деца (1 до 5 година) - препоручена почетна доза за ИТП је једна таблета Револаде од 25 мг дневно.
За хепатитис Ц.
Одрасли - Препоручена почетна доза за хепатитис Ц је једна таблета Револадеа од 25 мг дневно. Ако сте пореклом из Источне Азије (Кинези, Јапанци, Тајванци, Тајланђани или Корејци), почет ћете са истом дозом од 25 мг.
За САА
Одрасли - препоручена почетна доза за ААС је једна Револаде таблета од 50 мг дневно. Ако сте источноазијског порекла (Кинези, Јапанци, Тајванци, Тајланђани или Корејци), можда ћете морати да почнете са нижом дозом од 25 мг.
За рад Револаде -а може бити потребно 1 до 2 недеље. На основу вашег одговора на Револаде, ваш лекар може препоручити дневну промену дозе.
Како узимати таблете
Таблету прогутајте целу са мало воде.
Када га узети
Уверите се да-
- 4 сата пре узимања Револаде -а
- и 2 сата након узимања Револаде
Не конзумирате ништа од следећег:
- намирнице као што су сир, путер, јогурт или сладолед
- млеко или смоотхие на бази млека, пића која садрже млеко, јогурт или кајмак
- антациди, врста лека за варење и горушицу
- неки витамински и минерални додаци укључујући гвожђе, калцијум, магнезијум, алуминијум, селен и цинк.
Ако се то догоди, лек се неће правилно апсорбовати у тело.
За додатне савете о одговарајућој храни и пићу, питајте свог лекара.
Ако сте заборавили да узмете Револаде
Следећу дозу узмите у уобичајено време. Не узимајте више од једне дозе Револаде -а дневно.
Ако престанете да користите Револаде
Немојте престати узимати Револаде без разговора са лекаром. Ако вам лекар саветује да прекинете лечење, број тромбоцита ће се проверавати сваке недеље током четири недеље.
Ако имате додатних питања о употреби овог лека, обратите се свом лекару или фармацеуту.
Предозирање Шта учинити ако сте узели превише лека Револаде
Одмах се обратите свом лекару или фармацеуту.Ако је могуће, покажите им кутију или овај летак. Сви знаци или симптоми нежељених ефеката ће се проверити и одмах ће се на одговарајући начин третирати.
Нежељени ефекти Који су нежељени ефекти Револаде -а
Као и сви други лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих.
Симптоми на које треба обратити пажњу: Посетите лекара
Људи који узимају Револаде за ИТП или низак број тромбоцита у крви због хепатитиса Ц могли би развити знакове потенцијално озбиљних нуспојава. Важно је да обавестите свог лекара ако развијете ове симптоме.
Већи ризик од стварања крвних угрушака
Неки људи могу имати већи ризик од стварања крвних угрушака, а лијекови попут Револадеа могу погоршати овај проблем. Нагло зачепљење крвног суда крвним угрушком је неуобичајен нежељени ефекат и може се јавити у до 1 на 100 људи.
Одмах се обратите лекару ако приметите знакове и симптоме крвног угрушка, као што су:
- отицање, бол, топлина, црвенило или осетљивост на једној нози
- изненадни почетак отежаног дисања, посебно заједно са оштрим болом у грудима или убрзаним дисањем
- бол у стомаку (стомак), отицање абдомена, крв у столици.
Проблеми са јетром
Револаде може изазвати промене које се показују у крвним тестовима и могу бити знаци оштећења јетре. Проблеми с јетром (повећање ензима пронађених у крвним претрагама) су чести и могу се јавити у до 1 на 10 особа. Остали проблеми с јетром (жуч не тече правилно) су неуобичајени и могу се јавити у до 1 на 10 особа.
Ако имате било који од ових знакова проблема са јетром:
- жутило на кожи или беоњачама (жутица)
- урин необично тамне боје
- Одмах обавестите свог лекара.
Крварење или модрице након престанка лечења
У року од две недеље након престанка узимања Револадеа, број тромбоцита ће се обично смањити на онолико колико је био пре почетка примене Револаде -а. Мањи број тромбоцита може повећати ризик од крварења или модрица. Ваш лекар ће проверавати ваш број тромбоцита најмање 4 недеље након што престанете да узимате Револаде.
- Реците свом лекару ако имате крварење или модрице након што престанете да узимате Револаде.
Неки људи имају крварење у дигестивном систему након престанка узимања пегинтерферона, рибавирина и Револадеа. Симптоми укључују:
- тамне столице, промена боје столице је неуобичајен нежељени ефекат који се може јавити у до 1 на 100 људи)
- крв у столици
- повраћање крви или нешто попут талога кафе
- Одмах обавестите свог лекара ако приметите неки од ових симптома.
Други могући нежељени ефекти код одраслих са ИТП
Уобичајени нежељени ефекти Могу се јавити у до 1 на 10 особа:
- мучнина
- пролив
- катаракта (замагљивање очног сочива)
- суво око
- неуобичајен губитак или проређивање косе
- осип
- сврбеж
- болови у мишићима, грчеви мишића
- бол у леђима
- болови у костима
- пецкање и утрнулост у рукама или стопалима
- тежак менструални циклус
- чиреви у устима.
Уобичајени нежељени ефекти који се могу појавити у тесту крви:
- повећани јетрени ензими
- повећан билирубин (супстанца коју производи јетра)
- повећан ниво неких протеина.
Ретки нежељени ефекти
Ово може утицати на до 1 на 100 људи:
- прекид дотока крви у део срца
- изненадни недостатак даха, посебно када је праћен оштрим болом у грудима и / или убрзаним дисањем које може бити знак крвног угрушка у плућима (погледајте "Већи ризик од стварања крвних угрушака" на почетку одељка 4
- губитак функције дела плућа узрокован зачепљењем плућне артерије
- проблеми са јетром, укључујући жутање очију и коже
- убрзан рад срца, неправилан рад срца, плавичаста промена боје коже
- поремећаји срчаног ритма (продужење КТ интервала)
- запаљење вене
- модрице
- грлобоља и нелагодност при гутању, упала плућа, синуса, крајника, носа и грла
- утицај
- упала плућа
- губитак апетита
- болно отицање зглобова узроковано мокраћном киселином (гихт)
- проблеми са спавањем, депресија, губитак интересовања, промене расположења
- осећај поспаности, проблеми са равнотежом, говором и нервном функцијом, мигрене, дрхтавица
- проблеми са очима, укључујући замагљен и мање јасан вид
- бол у уху, вртоглавица
- проблеми са носом, грлом и синусима, проблеми са дисањем током сна
- проблеми пробавног система, укључујући: повраћање, надутост, честе столице, бол и осјетљивост у трбуху, тровање храном
- ректални карцином
- проблеми са устима укључујући сува или болна уста, осетљивост језика, крварење десни,
- промене на кожи укључујући прекомерно знојење, осип са жуљевима и свраб, црвене мрље, промене у изгледу
- опекотине од сунца
- црвенило или оток око ране
- крварење око катетера (ако постоји)
- осећај страног тела на месту убризгавања
- слабост мишића
- бубрежни проблеми укључујући: упалу бубрега, прекомерно мокрење ноћу, отказивање бубрега, инфекцију уринарног тракта, бела крвна зрнца у урину
- малаксалост, грозница, осећај врућине, бол у грудима
- хладан зној
- упала десни
- инфекција коже.
Ретки нежељени ефекти који се могу појавити у тесту крви:
- смањење броја црвених крвних зрнаца (анемија), белих крвних зрнаца и тромбоцита
- повећан број црвених крвних зрнаца
- промене у морфологији крви
- промене нивоа мокраћне киселине, калцијума и калијума.
Други могући нежељени ефекти код деце са ИТП
Веома чести нежељени ефекти
Ово може утицати на више од 1 на 10 деце:
- бол у грлу, цурење из носа, зачепљеност носа и кијање
- инфекција носа, синуса, грла и горњих дисајних путева, обична прехлада (инфекција горњих дисајних путева)
- пролив.
Уобичајени нежељени ефекти
Ово може утицати на до 1 на 10 деце:
- тешкоће са спавањем (несаница)
- бол у стомаку
- зубобоља
- кашаљ
- бол у носу и грлу
- свраб у носу, цурење или зачепљен нос
- висока температура.
Други могући нежељени ефекти код људи са хепатитисом Ц.
Веома чести нежељени ефекти
Ово може утицати на више од 1 на 10 особа:
- главобоља
- смањен апетит
- несаница
- кашаљ
- мучнина, дијареја
- болови у мишићима, свраб, недостатак енергије, висока температура, неуобичајен губитак косе, осећај слабости, болест слична грипу, отицање у шакама и стопалима, зимица.
Веома чести нежељени ефекти који се могу појавити у тесту крви:
- смањење броја црвених крвних зрнаца (анемија).
Уобичајени нежељени ефекти
Могу се јавити у до 1 на 10 особа:
- инфекције уринарног система
- упала носних пролаза, грла и уста, симптоми слични грипу, сува уста, болови у устима, зубобоља
- губитак тежине
- поремећаји спавања, абнормална поспаност, конфузија, депресија, анксиозност, узнемиреност
- вртоглавица, проблеми са концентрацијом и памћењем
- пецкање или утрнулост у рукама или стопалима
- запаљење у мозгу
- очни проблеми укључујући катаракту (замагљивање очног сочива) суво око, мале жуте наслаге у ретини, жутило беоњача
- крварење у или око ретине (присутно у задњем делу ока)
- осећај вртоглавице, лупање срца, отежано дисање
- кашаљ са слузи
- проблеми са дигестивним системом, укључујући: повраћање, бол у стомаку, лоше варење, затвор, отицање желуца, поремећај укуса, упалу желуца, хемороиде, отечене крвне судове и крварење у једњаку (езофагитис), иритацију црева
- проблеми са јетром, укључујући: крвни угрушак, жутило беоњаче или ока или коже (жутица), рак јетре
- промене на кожи, укључујући: осип, суву кожу, екцем, црвенило коже, свраб, прекомерно знојење, необичан раст коже? болови у зглобовима, леђима, костима, болови у шакама или стопалима, грчеви мишића
- раздражљивост, општи осећај лошег осећаја, болови у грудима и нелагодност
- реакције на месту убризгавања
- поремећаји срчаног ритма (продужење КТ интервала).
Уобичајени нежељени ефекти који се могу појавити у тесту крви:
- повишен шећер у крви (хипергликемија)
- смањење броја белих крвних зрнаца
- смањење протеина у крви
- распад црвених крвних зрнаца (хемолитичка анемија)
- повећан билирубин (супстанца коју производи јетра)
- промене у ензимима који контролишу згрушавање крви.
Ретки нежељени ефекти
Ово може утицати на до 1 на 100 људи:
- бол приликом мокрења.
Ретки нежељени ефекти
Учесталост се не може проценити из доступних података
- промена боје коже
Следећи нежељени ефекти су пријављени у вези са лечењем Револадеом код пацијената са тешком апластичном анемијом (САА).
Веома чести нежељени ефекти
Могу се јавити у до 1 на 10 особа:
- кашаљ
- главобоља
- пискање (диспнеја)
- бол у носу и грлу
- цурење носа
- бол у стомаку
- пролив
- мучнина
- модрице
- бол у зглобовима
- грчење мишића
- бол у рукама, ногама, шакама и стопалима
- вртоглавица
- осећај великог умора
- грозница
- несаница
Веома чести нежељени ефекти који се могу појавити у тесту крви:
- повећани јетрени ензими (трансаминазе). Крвни тестови могу показати абнормалне промене у ћелијама коштане сржи.
Уобичајени нежељени ефекти
Могу се јавити у до 1 на 10 особа:
- анксиозност
- депресија
- Хладно
- општа слабост
- очни проблеми који укључују: замагљен и мање јасан вид, катаракту, вид мрља у оку због несавршене прозирности стакластог тела, суве очи, сврбеж очију, жутило коже или беоњача
- крварење из носа
- крварење десни
- пликови у устима
- проблеми са дигестивним системом који укључују: повраћање, промене апетита (повећање или смањење), бол у стомаку / нелагоду, надути стомак, ветар, промену боје столице
- несвестица
- кожни проблеми који укључују: мале црвене или љубичасте мрље узроковане крварењем на кожи (петехије), осип, свраб, кожне лезије
- бол у леђима
- бол у мишићима
- болови у костима
- слабост
- отицање ткива, обично доњих удова, услед задржавања воде
- абнормално обојен урин
- поремећај снабдевања крви слезином (инфаркт слезине).
Уобичајени нежељени ефекти који се могу појавити у тесту крви:
- повећани ензими због повреде мишића (креатин фосфокиназа)
- накупљање гвожђа у крви
- смањен број белих крвних зрнаца (неутропенија)
- снижен шећер у крви (хипогликемија)
- повећан билирубин (супстанца коју производи јетра)
Ретки нежељени ефекти
Учесталост се не може проценити из доступних података
- промена боје коже
Пријављивање нежељених ефеката
Ако добијете било које нежељено дејство, разговарајте са својим лекаром, фармацеутом или медицинском сестром. Ово укључује све могуће нежељене ефекте који нису наведени у овом упутству. Нежељене ефекте можете пријавити и директно путем националног система за пријављивање. Пријављивањем нежељених ефеката можете помоћи да пружите више информације о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока ваљаности наведеног на кутији и блистеру иза „Рок употребе“.
Овај лек не захтева посебне услове складиштења.
Не бацајте никакве лекове у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Остале информације
Шта Револаде садржи
Активни састојак лека Револаде је елтромбопаг.
12,5 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 12,5 мг елтромбопага.
25 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 25 мг елтромбопага.
50 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалентан 50 мг елтромбопага.
75 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 75 мг елтромбопага.
Помоћни састојци су: хипромелоза, макрогол 400, магнезијум стеарат, манитол (Е421), микрокристална целулоза, повидон, натријум скроб гликолат, титанијум диоксид (Е171).
Револаде 50 мг филмом обложене таблете такође садрже црвени оксид гвожђа (Е172), жути гвожђе оксид (Е172).
Револаде 75 мг филмом обложене таблете такође садрже црвени оксид гвожђа (Е172), жути гвожђе оксид (Е172).
Како Револаде изгледа и садржај паковања
Револаде 12,5 мг филмом обложене таблете су округле, биконвексне, беле, са утиснутим „ГС МЗ1“ и „12,5“ на једној страни.
Револаде 25 мг филмом обложене таблете су округле, биконвексне, беле, са "ГС НКС3" и "25" утиснутим на једној страни.
Револаде 50 мг филмом обложене таблете су округле, биконвексне, смеђе боје, са утиснутим натписима „ГС УФУ“ и „50“ на једној страни.
Револаде 75 мг филмом обложене таблете су округле, биконвексне, розе боје, са утиснутим ознакама "ГС ФФС" и "75" на једној страни.
Испоручују се у алуминијским блистерима у паковању које садржи 14 или 28 филмом обложених таблета и вишеструком паковању које садржи 84 (3 паковања од 28) филмом обложених таблета.
Не продају се све величине паковања у вашој земљи.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
РЕВОЛАДЕ ТАБЛЕТЕ ОБЛОЖЕНЕ ФИЛМОМ
02.0 КВАЛИТАТИВНИ И КОЛИЧИНСКИ САСТАВ
Револаде 12,5 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 12,5 мг елтромбопага.
Револаде 25 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 25 мг елтромбопага.
Револаде 50 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалентан 50 мг елтромбопага.
Револаде 75 мг филмом обложене таблете
Свака филмом обложена таблета садржи елтромбопаг оламин еквивалент 75 мг елтромбопага.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Филмом обложена таблета.
Револаде 12,5 мг филмом обложене таблете
Округла, биконвексна, бела филм таблета (пречника приближно 7,9 мм) са утиснутим натписима "ГС МЗ1" и "12,5" на једној страни.
Револаде 25 мг филмом обложене таблете
Округла, биконвексна, бела филм таблета (приближно 10,3 мм у пречнику) са утиснутим натписима "ГС НКС3" и "25" на једној страни.
Револаде 50 мг филмом обложене таблете
Округла, биконвексна, смеђа филмом обложена таблета (приближно 10,3 мм у пречнику) са утиснутим натписима "ГС УФУ" и "50" на једној страни.
Револаде 75 мг филмом обложене таблете
Округла, биконвексна, ружичаста филм таблета (пречника приближно 10,3 мм) са утиснутим натписима "ГС ФФС" и "75" на једној страни.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Револаде је индициран код пацијената старијих од 1 године са хроничном аутоимуном (идиопатском) тромбоцитопеничном пурпуром (ИТП) који су отпорни на друге третмане (нпр. Кортикостероиде, имуноглобулине) (видети одељке 4.2 и 5.1).
Револаде је индициран код одраслих пацијената са хроничном инфекцијом вирусом хепатитиса Ц (Вирус хепатитиса Ц., ХЦВ) за лечење тромбоцитопеније, када је степен тромбоцитопеније главни фактор који спречава почетак или ограничава способност одржавања оптималне терапије засноване на интерферону (видети одељке 4.4 и 5.1).
Револаде је индикован код одраслих пацијената са тешком стеченом апластичном анемијом (САА), који су отпорни на претходну имуносупресивну терапију или су претходно претходно третирани и не испуњавају услове за трансплантацију хематопоетских матичних ћелија (видети одељак 5.1).
04.2 Дозирање и начин примене
Лечење елтромбопагом треба започети и одржавати под надзором лекара са искуством у лечењу хематолошких болести или у лечењу хроничног хепатитиса Ц и његових компликација.
Дозирање
Потребну дозу елтромбопага треба индивидуализовати на основу броја тромбоцита у пацијента. Циљ лечења елтромбопагом не би требао бити нормализација броја тромбоцита.
Прашак за оралну суспензију може довести до веће изложености елтромбопагу од формулације таблете (видети одељак 5.2). Приликом преласка са формулације таблете на формулу праха за оралну суспензију, број тромбоцита треба пратити недељно 2 недеље.
Хронична аутоимуна (идиопатска) тромбоцитопенија
Најнижу дозу елтромбопага треба користити за постизање и одржавање броја тромбоцита ≥ 50.000 / μл. Прилагођавање дозе је засновано на одговору броја тромбоцита.
Елтромбопаг се не сме користити за нормализацију броја тромбоцита. У клиничким студијама, број тромбоцита се генерално повећао у року од 1-2 недеље након почетка примене елтромбопага, а смањио се у року од 1-2 недеље након престанка.
Одрасли и педијатријска популација старости 6-17 година
Препоручена почетна доза елтромбопага је 50 мг једном дневно. Код пацијената источноазијског порекла (као што су Кинези, Јапанци, Тајванци, Корејци или Тајланђани), лечење елтромбопагом треба започети смањеном дозом од 25 мг једном дневно (видети одељак 5.2).
Педијатријска популација од 1 до 5 година
Препоручена почетна доза елтромбопага је 25 мг једном дневно.
Праћење и модификација дозе
Након почетка терапије елтромбопагом, дозу треба прилагодити како би се постигао и одржао број тромбоцита ≥ 50.000 / μл неопходан за смањење ризика од крварења. Не сме се прекорачити дневна доза од 75 мг.
Хемију крви и параметре функције јетре треба редовно пратити током терапије елтромбопагом, а режим дозирања елтромбопага треба прилагодити на основу броја тромбоцита како је приказано у Табели 1. Током терапије елтромбопагом недељно треба процењивати комплетну крвну слику, укључујући број тромбоцита и периферне брис крви, све док се не постигне стабилан број тромбоцита (≥ 50.000 / μл најмање 4 недеље).
Након тога, месечно треба обавити комплетну крвну слику, укључујући број тромбоцита и брис периферне крви.
Табела 1 Модификације дозе елтромбопага код пацијената са ИТП
* - За пацијенте који узимају елтромбопаг 25 мг једном у два дана, повећајте дозу на 25 мг једном дневно.
? - За пацијенте који узимају елтромбопаг 25 мг једном дневно, треба размотрити дозу од 12,5 мг једном дневно или алтернативно дозу од 25 мг једном у два дана.
Елтромбопаг се може давати као додатак другим ИТП лековима. Режим дозирања истовремених лекова за лечење ИТП -а треба модификовати, како је клинички прикладно, како би се избегло прекомерно повећање броја тромбоцита током терапије елтромбопагом.
Неопходно је сачекати најмање 2 недеље да би се видео ефекат било које промене дозе на одговор тромбоцита пацијента пре разматрања другог прилагођавања дозе.
Стандардна модификација дозе елтромбопага, било надоле или навише, треба да буде 25 мг једном дневно.
Прекид лечења
Лечење елтромбопагом треба прекинути ако се број тромбоцита не повећа на ниво довољан да се избегне клинички важно крварење након четири недеље терапије са 75 мг елтромбопага једном дневно.
Пацијенте треба подвргнути периодичној клиничкој процени, а о наставку лечења треба да одлучи лекар појединачно. Код пацијената који немају спленектомију, ово би требало да укључи процену спленектомије. По прекиду терапије могућа је поновна појава тромбоцитопеније (видети одељак 4.4).
Тромбоцитопенија повезана са хроничним ХЦВ хепатитисом
Када се елтромбопаг примењује у комбинацији са антивирусним лековима, потребно је позвати сажетак карактеристика производа одговарајућих истовремених лекова ради потпуних детаља о релевантним безбедносним информацијама и контраиндикацијама.
У клиничким студијама, број тромбоцита је генерално почео да расте у року од 1 недеље од почетка примене елтромбопага. Циљ лечења елтромбопагом треба да буде постизање минималног броја тромбоцита неопходних за започињање антивирусне терапије, у складу са препорукама у клиничкој пракси. Током антивирусне терапије, циљ лечења треба да буде одржавање броја тромбоцита на нивоу који спречава ризик од компликација крварења, типично око 50 000 - 75 000 / μл. Треба избегавати број тромбоцита> 75 000 / μл Треба користити најмању дозу елтромбопага потребну за постизање циљева .Модификације дозе се заснивају на одговору броја тромбоцита.
Иницијални режим дозирања
Елтромбопаг треба започети у дози од 25 мг једном дневно. Није потребна промена дозе за пацијенте са хроничним ХЦВ хепатитисом источноазијског порекла или за пацијенте са благим оштећењем јетре (видети одељак 5.2).
Праћење и модификација дозе
Дозу елтромбопага треба мењати у корацима од 25 мг сваке 2 недеље како би се постигао циљни број тромбоцита потребан за почетак антивирусне терапије. Број тромбоцита треба проверавати недељно пре почетка антивирусне терапије. Број тромбоцита може пасти на почетку антивирусне терапије, стога треба избегавати тренутне промене у дози елтромбопага (видети Табелу 2).
Током антивирусне терапије, дозу елтромбопага треба прилагодити по потреби како би се избегло смањење дозе пегинтерферона због смањења броја тромбоцита које би могле изложити пацијента ризику од крварења (видети Табелу 2). Број тромбоцита треба пратити недељно током антивирусне терапије док се не постигне стабилан број тромбоцита, обично око 50.000-75.000 / μл. Комплетну крвну слику, укључујући број тромбоцита и брис периферне крви, требало би затим спровести месечно. Треба размотрити смањење дозе од 25 мг од дневне дозе ако број тромбоцита премаши тражени циљ. Препоручљиво је сачекати 2 недеље да би се проценили ефекти овог и свих накнадних прилагођавања дозе.
Не треба прекорачити дозу од 100 мг елтромбопага једном дневно.
Табела 2 Модификације дозе елтромбопага код пацијената са хроничним ХЦВ хепатитисом током антивирусне терапије
* - Код пацијената који узимају 25 мг елтромбопага једном дневно, треба размотрити поновно започињање терапије са 25 мг сваки други дан.
? - Број тромбоцита може се смањити након почетка антивирусне терапије, стога треба избјегавати тренутно смањење дозе елтромбопага.
Прекид лечења
Лечење елтромбопагом треба прекинути ако број тромбоцита потребних за почетак антивирусне терапије није достигнут након 2 недеље терапије од 100 мг.
Осим ако није другачије оправдано, лечење елтромбопагом треба прекинути када се прекине антивирусна терапија. Превелик одговор на број тромбоцита или велике абнормалности у тестовима функције јетре такође захтевају прекид лечења.
Тешка апластична анемија
Иницијални режим дозирања
Лечење елтромбопагом треба започети дозом од 50 мг једном дневно. Код пацијената источноазијског порекла, лечење елтромбопагом треба започети смањеном дозом од 25 мг једном дневно (видети одељак 5.2). Лечење не треба започињати ако пацијенти већ имају цитогенетске абнормалности хромозома 7.
Праћење и модификација дозе
Хематолошки одговор захтева титрацију дозе, обично до 150 мг, а може потрајати и до 16 недеља након почетка терапије елтромбопагом (видети одељак 5.1). Дозу елтромбопага треба мењати у корацима од 50 мг. Сваке 2 недеље како би се постигао циљни тромбоцит број ≥ 50.000 / μл. За пацијенте који узимају 25 мг једном дневно, дозу треба повећати на 50 мг дневно пре следећих корака од 50 мг. Не треба је прекорачити. дозу од 150 мг дневно Треба пратити клиничке хематолошке и хепатичке тестове током терапије елтромбопагом и модификованог режима дозирања елтромбопага на основу броја тромбоцита како је наведено у Табели 3.
Табела 3 Модификације дозе елтромбопага код пацијената са тешком апластичном анемијом
Смањење за пацијенте са трилинеарним одговором (бела крвна зрнца, црвена крвна зрнца и тромбоцити)
За пацијенте који постигну трилинеарни одговор, укључујући независност од трансфузије, који траје најмање 8 недеља: доза елтромбопага се може смањити за 50%.
Ако крвна слика остане стабилна након 8 недеља при смањеној дози, елтромбопаг треба прекинути и пратити крвну слику. Ако би број тромбоцита пао са нивоа хемоглобина на ниво неутрофила на ниво
Прекид
Ако након 16 недеља терапије елтромбопагом није дошло до хематолошког одговора, терапију треба прекинути. Ако се открију нове цитогенетске абнормалности, треба размотрити да ли је одговарајућа даља терапија елтромбопагом (видети одељке 4.4 и 4.8). Прекомерни одговор у броју тромбоцита (као што је приказано у Табели 3) или велике абнормалности теста јетре такође захтевају прекид терапије елтромбопагом (видети одељак 4.8).
Посебне популације
Инсуфицијенција бубрега
Није потребно прилагођавање дозе код пацијената са бубрежном инсуфицијенцијом. Пацијенти са оштећеном бубрежном функцијом треба да користе елтромбопаг са опрезом и под пажљивим надзором, на пример провером серумског креатинина и / или анализом урина (видети одељак 5.2).
Хепатична инсуфицијенција
Елтромбопаг се не сме користити код пацијената са ИТП са инсуфицијенцијом јетре (Цхилд-Пугх скор ≥ 5) осим ако очекивана корист надмашује идентификовани ризик од тромбозе порталне вене (видети одељак 4.4).
Ако се сматра да је употреба елтромбопага неопходна за пацијенте са ИТП-ом са инсуфицијенцијом јетре, почетна доза треба да буде 25 мг једном дневно.Након почетка примене дозе елтромбопага код пацијената са инсуфицијенцијом јетре, интервал од 3 недеље пре повећања дозе.
Није потребно прилагођавање дозе за тромбоцитопеничне пацијенте са хроничним ХЦВ хепатитисом и благом инсуфицијенцијом јетре (Цхилд-Пугх скор ≤ 6). Пацијенти са хроничним ХЦВ хепатитисом и тешком апластичном анемијом са инсуфицијенцијом јетре треба да почну са елтромбопагом у дози од 25 мг једном дневно (видети одељак 5.2). Након почетка терапије елтромбопагом код пацијената са инсуфицијенцијом јетре, потребно је придржавати се размака од 2 недеље пре повећања дозе.
Постоји повећан ризик од нежељених догађаја, укључујући декомпензацију јетре и тромбоемболијске догађаје, код тромбоцитопеничних пацијената са узнапредовалим хроничним обољењем јетре лечених елтромбопагом било у припреми за инвазивне процедуре или код пацијената са хроничним ХЦВ хепатитисом који се лече антивирусном терапијом (видети одељке 4.4 и 4.8).
Старији грађани
Постоје ограничени подаци о употреби елтромбопага код пацијената са ИТП -ом старијим од 65 година и старијим, а нема клиничког искуства код пацијената са ИТП -ом старијим од 85 година. У клиничким испитивањима са елтромбопагом нису клинички уочене никакве укупне разлике. Значајна је безбедност елтромбопага међу испитаници старости најмање 65 година и млађи. Друга пријављена клиничка искуства нису идентификовала разлике у одговорима између старијих и млађих пацијената, али се не може искључити већа осетљивост неких старијих испитаника (видети одељак 5.2).
Постоје ограничени подаци о употреби елтромбопага код пацијената са хроничним хепатитисом изазваним ХЦВ-ом и ААС старијим од 75 година. Треба бити опрезан код ових пацијената (видети одељак 4.4).
Источноазијски пацијенти
Код пацијената источноазијског порекла (као што су Кинези, Јапанци, Тајванци, Корејци или Тајланђани), укључујући и оне са оштећењем јетре, елтромбопаг треба започети у дози од 25 мг једном дневно (видети одељак 5.2).
Треба наставити са праћењем броја тромбоцита код пацијената и следити стандардне критеријуме за даље прилагођавање дозе.
Педијатријска популација
Револаде се не препоручује код деце млађе од 1 године са хроничном ИТП због недостатка података о безбедности и ефикасности. Безбедност и ефикасност елтромбопага код деце и адолесцената (
Начин примене
Орална употреба.
Таблете треба узети најмање два сата пре или четири сата након било ког производа, попут антацида, млечних производа (или других прехрамбених производа који садрже калцијум), или минералних додатака који садрже поливалентне катионе (нпр. Гвожђе, калцијум, магнезијум, алуминијум, селен и цинк ) (види одељке 4.5 и 5.2).
04.3 Контраиндикације
Преосјетљивост на елтромбопаг или било коју помоћну супстанцу наведену у одјељку 6.1.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Постоји повећан ризик од нежељених реакција, укључујући декомпензацију јетре опасну по живот и тромбоемболијске догађаје, код пацијената са хепатитисом изазваним тромбоцитопеничном ХЦВ са узнапредовалом хроничном болешћу јетре, дефинисаном ниским албумином ≤ 35 г / л или моделом за бодовање. Болест јетре (МЕЛД) ≥ 10, када се лечи елтромбопагом у комбинацији са терапијом заснованом на интерферону. Штавише, користи од лечења у погледу пропорције пацијената који су постигли одрживи виролошки одговор (СВР) у поређењу са плацебом биле су скромне код ових пацијената (посебно оних са почетним албумином ≤ 35 г / л) у поређењу са целокупном групом.Лечење елтромбопагом код ових пацијената треба да започну само лекари са искуством у лечењу узнапредовалог хроничног ХЦВ хепатитиса, и само када ризик од тромбоцитопеније или прекид антивирусне терапије захтевају интервенцију. Ако се сматра да је лечење клинички индиковано, потребно је пажљиво праћење ових пацијената.
Комбинација са антивирусним лековима директног дејства
Безбедност и ефикасност нису утврђене у комбинацији са антивирусним лековима директног деловања одобреним за лечење хроничног ХЦВ хепатитиса.
Ризик од хепатотоксичности
Примјена елтромбопага може узроковати абнормалну функцију јетре и озбиљну хепатотоксичност, која може бити опасна по живот. У контролисаним клиничким испитивањима са елтромбопагом код хроничне ИТП, примећено је повишење серумске аланин аминотрансферазе (АЛТ), аспартат аминотрансферазе (АСТ) и билирубина (видети одељак 4.8).
Ове промене су биле углавном благе (1-2. Степен), реверзибилне и нису биле праћене клинички значајним симптомима који би указивали на "ослабљену функцију јетре. У" 3 плацебо контролисане студије код одраслих са хроничном ИТП, 1 пацијент из плацебо групе и 1 пацијент из групе елтромбопага имао је „абнормалност 4. степена у параметрима функције јетре. У две плацебо контролисане студије на педијатријским пацијентима (старости од 1 до 17 година) са хроничном ИТП, вредност АЛТ ≥ 3 пута већа од горње границе нормале ( к ГГН) виђено је у 4,7%, односно 0% у групама елтромбопага и плацеба.
У 2 контролисана клиничка испитивања код пацијената са хроничним ХЦВ хепатитисом, АЛТ или АСТ ≥ 3 пута већа од горње границе нормале (ГНН) пријављена је у 34%, односно у 38% група елтромбопага и плацеба. Већина пацијената који су примали елтромбопаг у комбинацији са терапијом пегинтерфероном / рибавирином доживеће индиректну хипербилирубинемију. Свеукупно, укупни билирубин ≥ 1,5 пута већи од ГЦН пријављен је у 76% и 50% група елтромбопага и плацеба, респективно.
Серумски АЛТ, АСТ и билирубин у серуму треба мерити пре почетка елтромбопага, сваке 2 недеље током фазе прилагођавања дозе, и месечно након постизања стабилне дозе.
Елтромбопаг инхибира УДП глукорозил трансферазу (УГТ) 1А1 и полипептид транспортера органских аниона (ОАТП) 1Б1, што може довести до индиректне хипербилирубинемије. Фракционисање треба извршити ако је билирубин повишен. Одступања у тестовима функције јетре у серуму треба проценити поновним тестирањем у року од 3-5 дана Ако се потврде абнормалности, треба пратити серумске тестове јетре све док се абнормалности не реше, стабилизују или врате на почетну вредност.
Давање елтромбопага треба прекинути ако се повећа ниво АЛТ (≥ 3 пута ГГН код пацијената са нормалном функцијом јетре, или ≥ 3 пута у односу на почетну вредност или> 5 пута у горњој граници горње границе, што је ниже, код пацијената са повећањем трансаминаза пре третмана) и ако су:
- прогресивно, или
- трајати ≥ 4 недеље, или
- праћене су повећањем директног билирубина, или
- праћени су клиничким симптомима оштећења јетре или доказима декомпензације јетре.
Потребан је опрез када се елтромбопаг примењује код пацијената са обољењем јетре. Код пацијената са ИТП и САА треба применити нижу почетну дозу елтромбопага. Потребно је пажљиво праћење када се даје пацијентима са инсуфицијенцијом јетре (видети одељак 4.2).
Отказивање јетре (употреба са интерфероном)
Оштећење јетре код пацијената са хроничним ХЦВ хепатитисом: Потребно је праћење код пацијената са ниским нивоом албумина (≤ 35 г / Л) или са основним МЕЛД скором ≥ 10.
Пацијенти са хроничним ХЦВ хепатитисом и цирозом могу бити изложени ризику од декомпензације јетре када примају терапију алфа интерфероном. У 2 контролисана клиничка испитивања код пацијената са тромбоцитопенијом са хроничним ХЦВ хепатитисом, декомпензација јетре (асцитес, хепатична енцефалопатија, варикозне крварења, спонтани бактеријски перитонитис) пријављена је чешће у краку елтромбопага (11%) него у групи која је примала плацебо (6%). Код пацијената са ниским нивоом албумина (≤ 35 г / Л) или МЕЛД скором ≥ 10 на почетку, постојао је троструко повећан ризик од декомпензације јетре и повећан ризик од фаталних нежељених догађаја у поређењу са онима са обољењем јетре која је узнапредовала. Штавише, користи од лечења у смислу стопе постизања СВР у поређењу са плацебом биле су скромне код ових пацијената (посебно код оних са почетним албумином ≤ 35 г / л) у поређењу са целокупном групом. Елтромбопаг се овим пацијентима треба давати тек након пажљивог разматрања очекиваних користи у односу на ризике. Пацијенте са овим карактеристикама треба пажљиво пратити због знакова и симптома јетрене декомпензације. Треба се позвати на одговарајући сажетак карактеристика производа интерферона за критеријуме прекида. Елтромбопаг треба прекинути ако се због декомпензације јетре прекине антивирусна терапија.
Тромботичке / тромбоемболијске компликације
У контролисаним клиничким испитивањима код тромбоцитопеничних пацијената са хроничним ХЦВ хепатитисом који су примали терапију засновану на интерферону (н = 1439), 38 од 955 (4%) испитаника лечених елтромбопагом и 6 од 484 (1%) испитаника у плацебо групи имало је тромбоемболијске догађаје (ТЕЕ). Извештаји о тромботичним / тромбоемболијским компликацијама укључивали су и венске и артеријске догађаје. Већина ТЕЕ није била озбиљна и решена је до краја студије. Тромбоза порталне вене била је најчешћи ТЕЕ у обе групе лечења (2% код пацијената лечених елтромбопагом у поређењу са знацима и симптомима ТЕЕ.
Ризик од ТЕЕ је повећан код пацијената са хроничном болести јетре (хронична болест јетре, ЦЛД) третиран са 75 мг елтромбопага једном дневно током две недеље у припреми за инвазивне процедуре.
Шест од 143 (4%) одраслих пацијената са ЦЛД који су примали елтромбопаг доживели су ТЕЕ (сви укључују портални венски систем), а два од 145 испитаника (1%) у плацебо групи доживели су ТЕЕ (један који укључује портални венски систем и инфаркт миокарда) . Пет од 6 пацијената лечених елтромбопагом доживело је тромботичке компликације са бројем тромбоцита> 200.000 / микролитра и у року од 30 дана од последње дозе елтромбопага. Елтромбопаг није индикован за лечење тромбоцитопеније код пацијената са хроничном болести јетре у припреми за инвазивне процедуре .
У клиничким испитивањима са елтромбопагом у ИТП -у, примећени су тромбоемболијски догађаји са ниским и нормалним бројем тромбоцита. Треба бити опрезан када се елтромбопаг примењује код пацијената са познатим факторима ризика за тромбоемболију, укључујући, али без ограничења, наследне (нпр. Фактор В Леиден) или стечене (нпр. Недостатак АТИИИ, антифосфолипидни синдром), факторе ризика, старију старост, пацијенте са продуженим периодима имобилизације , малигнитети, контрацептивна или хормонска надомјесна терапија, операције / трауме, гојазност и пушење. Треба пажљиво пратити број тромбоцита и размотрити смањење дозе или прекид терапије елтромбопагом ако број тромбоцита прелази потребне нивое (видети одељак 4.2). Однос користи и ризика треба узети у обзир код пацијената са ризиком од настанка ТЕЕ било које етиологије.
Елтромбопаг се не сме примењивати код пацијената са ИТП са инсуфицијенцијом јетре (Цхилд-Пугх скор ≥ 5) осим ако очекивана корист надмашује идентификовани ризик од тромбозе порталне вене. Када се сматра да је лечење одговарајуће, потребан је опрез при давању елтромбопага пацијентима са инсуфицијенцијом јетре (видети одељке 4.2 и 4.8).
Крварење након престанка узимања елтромбопага
Вероватно ће се поново појавити тромбоцитопенија по прекиду терапије елтромбопагом. Након престанка узимања елтромбопага, број тромбоцита се код већине пацијената враћа на почетну вредност у року од 2 недеље, што повећава ризик од крварења и у неким случајевима може довести до крварења. Овај ризик се повећава ако се лечење елтромбопагом прекине у присуству антикоагуланса и анти тромбоцитни агенси. Препоручује се наставак терапије ИТП -ом у складу са важећим смерницама ако се прекине лечење елтромбопагом. Осим тога, медицинско лечење може укључивати престанак примене антикоагуланса и / или антикоагулантну терапију. број треба да се прати недељно 4 недеље након престанка узимања елтромбопага.
У клиничким испитивањима хроничног ХЦВ хепатитиса, пријављена је већа учесталост желучаног крварења, укључујући тешке и фаталне случајеве, након прекида пегинтерферона, рибавирина и елтромбопага.
Након прекида терапије, пацијенте треба пратити ради откривања било каквих знакова или симптома желучаног крварења.
Формирање ретикулина у коштаној сржи и ризик од фиброзе коштане сржи Елтромбопаг може повећати ризик од развоја или прогресије ретикулинских влакана унутар коштане сржи. Као и код других агониста тромбопоетинских рецептора (ТПО-Р), релевантност ових промена још није утврђена.
Пре почетка елтромбопага, брис периферне крви треба пажљиво испитати како би се утврдио основни ниво ћелијских морфолошких абнормалности. Након идентификације стабилне дозе елтромбопага, месечно треба извршити комплетну крвну слику са диференцијалним бројем белих крвних зрнаца. Ако се примете незреле или диспластичне ћелије, брис периферне крви треба да се испита на нове морфолошке абнормалности (на пример, суза црвена крвна зрнца) (дакриоцити) и нуклеарна, незрела бела крвна зрнца) или погоршање или цитопенија. Ако се код пацијента развију нове или погоршавају морфолошке абнормалности или цитопенија, лечење елтромбопагом треба прекинути и узети у обзир Биопсију коштане сржи, укључујући процену фиброзе.
Напредовање постојећег мијелодиспластичног синдрома (МДС)
Агонисти ТПО-Р су фактори раста који изазивају пролиферацију и диференцијацију тромбопоетских матичних ћелија и производњу тромбоцита. ТПО-Р се претежно експримира на површини ћелија мијелоидне лозе. За агонисте ТПО-Р постоји ризик да могу стимулирати прогресију већ постојећих неопластичних хемопатија, попут мијелодиспластичног синдрома.
У клиничким испитивањима са агонистом ТПО-Р код пацијената са МДС-ом, забележени су случајеви пролазног повећања броја бласт ћелија и забележени су случајеви прогресије болести од МДС-а до акутне мијелоичне леукемије (АМЛ).
Дијагнозу ИТП или САА код одраслих и старијих пацијената треба потврдити искључењем других патологија које представљају тромбоцитопенију, посебно дијагнозу МДС -а треба искључити. Аспирацију и биопсију коштане сржи треба размотрити током болести и лечења, посебно код пацијената старијих од 60 година са системским симптомима или абнормалним знацима, попут повећања периферних бластних ћелија.
Ефикасност и безбедност елтромбопага нису утврђени за употребу у другим тромбоцитопеничним стањима, укључујући тромбоцитопенију изазвану хемотерапијом или МДС.
Елтромбопаг се не сме користити изван клиничких испитивања за лечење тромбоцитопеније због МДС -а или било ког другог узрока тромбоцитопеније осим одобрених индикација.
Цитогенетске абнормалности и прогресија МДС / АМЛ код пацијената са ААС
Познато је да се код пацијената са ААС развијају цитогенетске абнормалности. Није познато да ли елтромбопаг повећава ризик од цитогенетских абнормалности код пацијената са ААС. У клиничком испитивању фазе ИИ у којој је елтромбопаг коришћен у ААС, учесталост нових цитогенетских абнормалности забележена је код 19% пацијената [8/43 (од којих је 5 имало абнормалности хромозома 7)]. Средње време током студије за појаву цитогенетске абнормалности било је 2,9 месеци.
У клиничким испитивањима са елтромбопагом у АСА, 4% пацијената (5/133) је дијагностиковано са МДС -ом. Средње време до постављања дијагнозе од почетка терапије елтромбопагом било је три месеца.
За пацијенте са рефракторном или јако претретираном САА и који су претходно били на имуносупресивној терапији, препоручује се преглед аспирата коштане сржи на цитогенетику пре почетка елтромбопага, на 3 месеца лечења и сваких 6 месеци након тога. У случају откривања нових. Цитогенетских абнормалности, требало би размотрити да ли је прикладно наставити са елтромбопагом.
Очне промене
Катаракта је примећена у токсиколошким студијама елтромбопага код глодара (видети одељак 5.3). У контролисаним клиничким испитивањима на тромбоцитопеничним пацијентима са хроничним ХЦВ хепатитисом који су примали терапију интерфероном (н = 1439), прогресија већ постојеће почетне катаракте или појава нове катаракте пријављена је у 8% групе. Елтромбопаг и у 5% плацебо група. Крварења у ретини, углавном степена 1 или 2, пријављена су код пацијената са хроничним ХЦВ хепатитисом који су примали интерферон, рибавирин и елтромбопаг (2% у групи елтромбопага и 2% у групи која је примала плацебо). Крварења су се јавила на површини ретина (преретинална), испод ретине (субретинална) или унутар ретиналног ткива. Препоручује се рутинско офталмолошко праћење пацијената.
КТ / КТц екстензија
КТц студија на здравим добровољцима у дози од 150 мг елтромбопага дневно није показала клинички значајан ефекат на реполаризацију срца. Продужење КТц интервала пријављено је у клиничким испитивањима са ИТП пацијентима и тромбоцитопеничним пацијентима са хроничним ХЦВ хепатитисом. Клинички значај ових случајева продужења КТц периода није познат.
Губитак одговора на елтромбопаг
Губитак одговора или неуспех у одржавању одговора тромбоцита на лечење елтромбопагом у оквиру препорученог терапијског опсега требало би да покрене потрагу за узрочним факторима, укључујући повећање ретикулина у коштаној сржи.
Педијатријска популација
Горе наведена упозорења и мере предострожности за ИТП примењују се и на педијатријску популацију.
04.5 Интеракције са другим лековима и други облици интеракција
Ефекти елтромбопага на друге лекове
Инхибитори ХМГ ЦоА редуктазе
образовање ин витро показао да елтромбопаг није супстрат полипептида органског анионског транспортера ОАТП1Б1, већ је инхибитор овог транспортера. образовање ин витро такође су показали да је елтромбопаг супстрат и инхибитор протеина отпорности на рак дојке (БЦРП). Примена 39 здравих одраслих испитаника елтромбопага од 75 мг једном дневно током 5 дана са једном дозом од 10 мг росувастатина, супстрата ОАТП1Б1 и БЦРП, повећала је Ц росувастатина у плазми за 103% (интервал поузданости 90% [ЦИ]: 82 %, 126%) и АУЦ0-? 55% (90% ЦИ: 42%, 69%). Такође се очекују интеракције са другим инхибиторима ХМГ-ЦоА редуктазе, укључујући аторвастатин, флувастатин, ловастатин, правастатин и симвастатин. Када се примењује истовремено са елтромбопагом, треба размотрити смањење дозе статина и пажљиво праћење нежељених реакција на статине (видети одељак 5.2).
ОАТП1Б1 и БЦРП подлоге
Истовремену примену елтромбопага и супстрата ОАТП1Б1 (нпр. Метотрексат) и БЦРП (нпр. Топотекан и метотрексат) треба предузети с опрезом (видети одељак 5.2).
Подлоге од цитокрома П450
У студијама које су користиле микрозоме људске јетре, елтромбопаг (до 100 мцМ) није показао инхибицију. ин витро ензима ЦИП450 1А2, 2А6, 2Ц19, 2Д6, 2Е1, 3А4 / 5 и 4А9 / 11 и био је инхибитор ЦИП2Ц8 и ЦИП2Ц9 мерен коришћењем паклитаксела и диклофенака као супстрата сонде. Примена елтромбопага у дози од 75 мг једном дневно током 7 дана на 24 здрава мушкарца није инхибирала нити индуковала метаболизам супстрата сонде за 1А2 (кофеин), 2Ц19 (омепразол), 2Ц9 (флурбипрофен) или 3А4 (мидазолам) код људи. Не очекују се клинички значајне интеракције при истовременој примени супстрата елтромбопага и ЦИП450 (видети одељак 5.2).
Инхибитори ХЦВ протеазе
Није потребна промена дозе када се елтромбопаг примењује истовремено са телапревиром или боцепревиром.
Истовремена примена појединачне дозе елтромбопага 200 мг са 750 мг телапревира сваких 8 сати није променила изложеност телапревира плазми.
Истовремена примена појединачне дозе елтромбопага 200 мг са 800 мг боцепревира сваких 8 сати није променила АУЦ (0-?) Боцепревира у плазми, већ је повећала Ц за 20% и смањила Ц за 32%. Клиничка важност смањење Цмин није утврђено: препоручује се ближе клиничко и лабораторијско праћење за сузбијање ХЦВ -а.
Ефекти других лекова на елтромбопаг
Циклоспорин
Ин витро студије су показале да је елтромбопаг супстрат и инхибитор БЦРП. Примећено је смањење изложености елтромбопагу истовременом применом 200 мг и 600 мг циклоспорина (инхибитор БЦРП) (видети одељак 5.2).Промена дозе елтромбопага током лечења је дозвољена на основу броја тромбоцита код пацијената (видети одељак 4.2). Број тромбоцита треба пратити најмање недељно током 2 до 3 недеље када се елтромбопаг примењује истовремено са циклоспорином. Можда ће бити потребно повећати дозу елтромбопага на основу резултата тромбоцита.
Поливалентни катјони (хелација)
Елтромбопаг хелатира поливалентне катионе као што су гвожђе, калцијум, магнезијум, алуминијум, селен и цинк. Примена појединачне дозе од 75 мг елтромбопага са антацидом који садржи поливалентни катион (1524 мг алуминијум хидроксида и 1425 мг магнезијум карбоната) смањује АУЦ0-? елтромбопаг у плазми до 70% (90% ЦИ: 64%, 76%) и Цмак до 70% (90% ЦИ: 62%, 76%).
Елтромбопаг треба узети најмање 2 сата пре или 4 сата након било ког производа антацидне киселине, млечног производа или минералног додатка који садржи поливалентне катјоне како би се избегло значајно смањење апсорпције елтромбопага услед хелације (видети одељке 4.2 и 5.2).
Интеракција са храном
Примена таблета елтромбопага или прашка за оралну суспензију уз оброк са високим садржајем калцијума (нпр. Оброк који је укључивао млечне производе) значајно је смањио АУЦ0-? и Цмак елтромбопага у плазми. Насупрот томе, примена елтромбопага 2 сата пре или 4 сата након оброка са високим садржајем калцијума или хране са ниским садржајем калцијума [
Лопинавир / ритонавир
Истовремена примена елтромбопага са лопинавиром / ритонавиром може изазвати смањење концентрације елтромбопага. Студија на 40 здравих добровољаца показала је да је истовремена примена појединачне дозе од 100 мг елтромбопага са поновљеном дозом од 400/100 мг лопинавира / ритонавира два пута дневно довела до смањења АУЦ (0-?) Елтромбопага за 17% (90 %ЦИ: 6,6%; 26,6%). Због тога треба бити опрезан када се елтромбопаг примењује истовремено са лопинавиром / ритонавиром. Требало би пажљиво пратити број тромбоцита како би се обезбедило одговарајуће клиничко управљање дозом елтромбопага када се започне или прекине терапија лопинавиром / ритонавиром.
Инхибитори и индуктори ЦИП1А2 и ЦИП2Ц8
Елтромбопаг се метаболише путем више путева укључујући ЦИП1А2, ЦИП2Ц8, УГТ1А1 и УГТ1А3 (видети одељак 5.2). Није вероватно да ће лекови који инхибирају или индукују један ензим значајно утицати на концентрацију елтромбопага у плазми; док лекови који инхибирају или индукују више ензима имају потенцијал да повећају (нпр. Флувоксамин) или смање (нпр. Рифампицин) концентрације елтромбопага.
Инхибитори ХЦВ протеазе
Резултати фармакокинетичке студије интеракције између лекова и лека показују да истовремена примена поновљених доза боцепревира 800 мг сваких 8 сати или телапревира 750 мг сваких 8 сати са једном дозом 200 мг елтромбопага није променила изложеност елтромбопага плазми. клинички значајних нивоа.
Лекови за лечење ИТП -а
Лекови који су се користили у клиничким испитивањима у лечењу ИТП-а у комбинацији са елтромбопагом укључивали су кортикостероиде, даназол и / или азатиоприн, интравенозни имуноглобулин (ИВИГ) и анти-Д имуноглобулин. Треба да се прати број тромбоцита када се елтромбопаг даје у комбинацији са другим лековима за лечење ИТП -а, како би се избегло да број тромбоцита буде изван препорученог опсега (видети одељак 4.2).
04.6 Трудноћа и дојење
Трудноћа
Не постоје или постоји ограничена количина података о употреби елтромбопага у трудница, а испитивања на животињама су показала репродуктивну токсичност (видети одељак 5.3). Потенцијални ризик за људе је непознат.
Револаде се не препоручује током трудноће.
Жене у репродуктивној доби / Контрацепција код мушкараца и жена
Револаде се не препоручује женама у репродуктивном периоду које не користе контрацепцију.
Време храњења
Није познато да ли се елтромбопаг / његови метаболити излучују у мајчино млеко. Студије на животињама су показале да се елтромбопаг вероватно излучује у млеко (видети одељак 5.3); стога се не може искључити ризик за дојенче. Мора се донети одлука да ли да се прекине дојење или да се настави / уздржи од терапије леком Револаде, процењујући корист дојења за бебу и користи терапије за жену.
Плодност
Плодност није била погођена код мужјака и женки пацова при излагању које је било упоредиво са излагањем људима. Међутим, ризик по људе се не може искључити (видети одељак 5.3).
04.7 Утицај на способност управљања возилима и машинама
Елтромбопаг има занемарљив утицај на способност управљања возилима и рада на машинама. Клинички статус пацијента и профил нежељених реакција елтромбопага, укључујући вртоглавицу и недостатак будности, треба имати на уму приликом разматрања способности пацијента да обавља задатке који захтевају просуђивање, моторичке и когнитивне способности.
04.8 Нежељени ефекти
Сажетак сигурносног профила
У 4 контролисана и 2 неконтролисана клиничка испитивања, 530 одраслих пацијената са хроничном ИТП лечено је елтромбопагом%. Просечно трајање изложености елтромбопагу било је 260 дана. Најважније озбиљне нуспојаве биле су хепатотоксичност и тромботични / тромбоемболични догађаји. Најчешће нежељене реакције које су се јавиле код најмање 10% пацијената биле су: главобоља, анемија, смањен апетит, несаница, кашаљ, мучнина, дијареја, алопеција, пруритус, мијалгија, грозница, умор, болести сличне грипу, астенија, зимица и периферни едем.
У 2 контролисана клиничка испитивања, 171 педијатријски пацијент са хроничном ИТП лечен је елтромбопагом. Средње трајање изложености било је 171 дан. Профил нежељених реакција био је упоредив са оним код одраслих са неким додатним нежељеним реакцијама, означеним? У следећој табели.
Најчешће нежељене реакције код педијатријских пацијената старих 1 годину и више са ИТП (≥ 3% и више од плацеба) биле су велике инфекције респираторног тракта, назофарингитис, кашаљ, дијареја, пирексија, ринитис, бол у трбуху, бол у орофарингеалу, ране у зубима, кожни осип, повишен АСТ и ринореја.
У 2 контролисана клиничка испитивања, 955 тромбоцитопеничних пацијената са ХЦВ инфекцијом лечено је елтромбопагом. Средње трајање излагања било је 183 дана. Најважније идентификоване озбиљне нежељене реакције биле су хепатотоксичност и тромботични / тромбоемболијски догађаји. Најчешће нежељене реакције које су се јавиле код најмање 10% пацијената укључивале су: главобољу, анемију, смањен апетит, несаницу, кашаљ , мучнина, дијареја, алопеција, свраб, мијалгија, грозница, умор, болести сличне грипу, астенија, зимица и периферни едем.
Безбедност елтромбопага у тешкој апластичној анемији процењена је у отвореној клиничкој студији са једном руком (Н = 43) у којој је 12 пацијената (28%) лечено> 6 месеци, а 9 пацијената (21%) лечено > 1 година. Најважније озбиљне нуспојаве биле су фебрилна неутропенија и сепса / инфекције. Најчешће нежељене реакције које су се јавиле (код најмање 10% пацијената) укључивале су: главобољу, вртоглавицу, несаницу, кашаљ, недостатак даха, бол у ждрелу, ринореју , мучнина, дијареја, бол у трбуху, повећане трансаминазе, модрице, артралгија, грчеви мишића, болови у удовима, умор, фебрилна неутропенија и пирексија.
Листа нежељених реакција
Нежељене реакције у ИТП студијама за одрасле (Н = 550), педијатријским ИТП студијама (Н = 107) и студијама инфицираним ХЦВ -ом (Н = 955), АОС студијама (Н = 43) и постмаркетиншким извештајима доле су наведене према класи органа и учесталости МедДРА система .
Врло често (≥ 1/10)
Често (≥ 1/100 до
Мање често (≥ 1/1000 до
Ретко (≥ 1/10 000 до
Веома редак (
Није познато (не може се проценити из доступних података)
Становништво клиничког испитивања у ИТП -у
Инфекције и инфестације
Веома честа
Назофарингитис?, инфекције горњих дисајних путева?
заједнички
Ринитис?
необичан
Фарингитис, инфекције уринарног тракта, грип, орални херпес, упала плућа, синуситис, тонзилитис, инфекције респираторног тракта, гингивитис, инфекција коже
Бенигне, малигне и неозначене неоплазме (укључујући цисте и полипе)
необичан
Тумор ректосигмоидног тракта
Поремећаји крви и лимфног система
необичан
Анемија, анизоцитоза, еозинофилија, хемолитичка анемија, леукоцитоза, мијелоцитоза, тромбоцитопенија, повишен хемоглобин, повећан број неутрофила у траци, смањен хемоглобин, присуство мијелоцита, повећан број тромбоцита, смањен број белих крвних зрнаца.
Поремећаји имунолошког система
необичан
Преосетљивост
Поремећаји метаболизма и исхране
необичан
Анорексија, хипокалијемија, смањен апетит, гихт, хипокалцемија, повећана мокраћна киселина у крви
Психијатријски поремећаји
необичан
Поремећаји сна, депресија, апатија, промене расположења, лак плач
Поремећаји нервног система
заједнички
Парестхесиас
необичан
Хипестезија, сомноленција, мигрена, тремор, поремећаји равнотеже, дисестезија, хемипареза, мигрена са ауром, периферна неуропатија, периферна сензорна неуропатија, поремећаји говора, токсична неуропатија, васкуларна главобоља
Поремећаји ока
заједнички
Суво око
необичан
Замагљен вид, замућење леће, астигматизам, кортикална катаракта, бол у очима, повећана лакримација, ретинално крварење, пигментна епителиопатија ретине, смањена оштрина вида, оштећење вида, абнормалности теста видне оштрине, блефаритис и кератокоњунктивитис сицца
Поремећаји уха и лавиринта
необичан
Бол у уху, вртоглавица
Срчане патологије
необичан
Тахикардија, акутни инфаркт миокарда, кардиоваскуларни поремећаји, цијаноза, синусна тахикардија, продужење КТ електрокардиограма
Васкуларне патологије
необичан
Дубока венска тромбоза, емболија, испирање, површински тромбофлебитис, црвенило, хематом
Поремећаји дисања, грудног коша и медијастинума
заједнички
Кашаљ, орофарингеални бол?, Ринореја?
необичан
Плућна емболија, плућни инфаркт, нелагодност у носу, стварање жуљева у орофаринксу, бол у орофаринксу, поремећај синуса, синдром апнеје у сну
Гастроинтестинални поремећаји
заједнички
Мучнина, пролив *, чиреви у устима, зубобоља?
* Врло често код педијатријских пацијената са ИТП
необичан
Сува уста, повраћање, бол у трбуху, глосодинија, крварење у устима, абдоминална напетост, измењена столица, надутост, тровање храном, чести трбушни покрети, хематемеза, нелагодност у устима
Хепатобилиарни поремећаји
заједнички
Аланин аминотрансфераза * повећана, аспартат аминотрансфераза * повећана, хипербилирубинемија, поремећаји функције јетре
необичан
Холестаза, повреда јетре, хепатитис, повреда јетре изазвана лековима
* Повећање аланин аминотрансферазе и аспартат аминотрансферазе може се десити истовремено, мада на нижој фреквенцији.
Поремећаји коже и поткожног ткива
заједнички
Осип, алопеција
необичан Хиперхидроза, генерализовани свраб, уртикарија, дерматоза, петехије, хладно знојење, еритем, меланоза, поремећаји пигментације, промена боје коже, љуштење коже
Поремећаји мишићно -коштаног система и везивног ткива
заједнички
Мијалгија, грчеви мишића, мишићно -коштани бол, болови у костима, болови у леђима
необичан
Слабост мишића
Бубрега и уринарног поремећаји
необичан
Затајење бубрега, леукоцитурија, лупоидни нефритис, ноктурија, протеинурија, повећана уреа у крви, повећан креатинин у крви, повећан однос протеина / креатинина
Болести репродуктивног система и дојке
заједнички
Менорагија
Општи поремећаји и стања на месту примене
заједнички
Пирексија?
необичан
Бол у грудима, осећај врућине, крварење на месту парентералне ињекције, астенија, нервоза, упала рана, малаксалост, пирексија, осећај страног тела
Дијагностички тестови
необичан
Повећан албумин у крви, повећана алкална фосфатаза у крви, повећани укупни протеини, смањени албумини у крви, повећан пХ урина
Повреде, тровања и процедуралне компликације
необичан
Опекотине од сунца
? Додатне нежељене реакције уочене у студијама о педијатријској популацији (од 1 до 17 година)
Популација клиничких испитивања инфицираних ХЦВ -ом (у комбинацији са антивирусном терапијом интерфероном и рибавирином)
Инфекције и инфестације
заједнички
Инфекције уринарног тракта, инфекције горњих дисајних путева, бронхитис, назофарингитис, грип, орални херпес, гастроентеритис, фарингитис.
Бенигне, малигне и неозначене неоплазме (укључујући цисте и полипе)
заједнички
Малигни тумор јетре
Поремећаји крви и лимфног система
Веома честа
Анемија
заједнички лимфоцитопенија, хемолитичка анемија
Поремећаји метаболизма и исхране
Веома честа
Смањен апетит
заједнички
Хипергликемија, абнормални губитак тежине
Психијатријски поремећаји
Веома честа
Несаница
заједнички
Депресија, анксиозност, поремећаји сна, конфузија, узнемиреност
Поремећаји нервног система
Веома честа
Главобоља
заједнички
Вртоглавица, поремећај пажње, дисгеузија, хепатична енцефалопатија, летаргија, поремећаји памћења, парестезије
Поремећаји ока
заједнички
Катаракта, ретинални ексудати, суво око, склерална жутица, ретинално крварење
Поремећаји уха и лавиринта
заједнички
Вртоглавица
Срчане патологије
заједнички
Лупање срца
Поремећаји дисања, грудног коша и медијастинума
Веома честа
Кашаљ
заједнички
Диспнеја, орофарингеални бол, диспнеја при напору, продуктиван кашаљ
Гастроинтестинални поремећаји
Веома честа
Мучнина, дијареја
заједнички
Повраћање, асцитес, бол у стомаку, бол у горњем делу трбуха, диспепсија, сува уста, констипација, надутост стомака, зубобоља, стоматитис, рефлуксна болест једњака, хемороиди, нелагодност у стомаку, гастритис, варикозитет једњака, афтозни стоматитис, варикозитет једњака
Хепатобилиарни поремећаји
заједнички
Хипербилирубинемија, жутица, тромбоза порталне вене, затајење јетре, повреда јетре изазвана лековима
Поремећаји коже и поткожног ткива
Веома честа
Свраб, алопеција
заједнички
Осип, сува кожа, екцем, пруритицни осип, еритем, хиперхидроза, генерализовани свраб, ноћно знојење, кожне лезије
необичан
Промена боје коже, хиперпигментација коже
Поремећаји мишићно -коштаног система и везивног ткива
Веома честа
Миалгиа
заједнички
Артралгија, грчеви мишића, болови у леђима, болови у екстремитетима, мишићно -коштани бол, болови у костима
Бубрега и уринарног поремећаји
необичан
Дизурија
Општи поремећаји и стања на месту примене
Веома честа
Пирексија, умор, болест слична грипу, астенија, зимица, периферни едем
заједнички
Раздражљивост, бол, малаксалост, реакције на месту убризгавања, несрчани бол у грудима, едем, осип на месту убризгавања, нелагодност у грудима, свраб на месту убризгавања
Дијагностички тестови
заједнички
Повећан билирубин у крви, смањена тежина, смањен број белих крвних зрнаца, смањен хемоглобин, смањен број неутрофила, повећан међународни нормализовани однос (ИНР), продужено време делимичног тромбопластина, повећана глукоза у крви, смањење албумина у крви, продужење КТ интервала на електрокардиограму
Становништво клиничке студије у ААС
Поремећаји крви и лимфног система
заједнички
Неутропенија, инфаркт слезине
Поремећаји метаболизма и исхране
заједнички
Преоптерећење гвожђем, губитак апетита, хипогликемија, повећан апетит
Психијатријски поремећаји
Веома честа
Несаница
заједнички
Анксиозност, депресија
Поремећаји нервног система
Веома честа
Главобоља, вртоглавица
заједнички
Синкопа
Поремећаји ока
заједнички
Суво око, сврбеж ока, катаракта, очна жутица, замагљен вид, оштећење вида, плута
Поремећаји дисања, грудног коша и медијастинума
Веома честа
Кашаљ, диспнеја, бол у орофаринксу, ринореја
заједнички
Епистакса
Гастроинтестинални поремећаји
Веома честа
Бол у стомаку, дијареја, мучнина
заједнички
Гингивално крварење, жуљеви слузнице усне дупље, орални бол, повраћање, нелагодност у стомаку, бол у трбуху, констипација, надутост стомака, дисфагија, промењена боја столице, отечени језик, поремећаји покретљивости црева, надутост
Хепатобилиарни поремећаји
Веома честа
Повећане трансаминазе
заједнички
Повећан билирубин у крви (хипербилирубинемија), жутица
Није познато
Оштећење јетре изазвано лековима *
* Забележени су случајеви повреде јетре изазване лековима код пацијената са ИТП-ом и ХЦВ-ом
Поремећаји коже и поткожног ткива
Веома честа
Модрице
заједнички
Петехије, осип, свраб, осип, кожне лезије, макуларни осип
необичан
Промена боје коже, хиперпигментација коже
Поремећаји мишићно -коштаног система и везивног ткива
Веома честа
Артралгија, грчеви мишића, болови у екстремитетима
заједнички
Бол у леђима, мијалгија, бол у костима
Бубрега и уринарног поремећаји
заједнички
Хроматурија
Општи поремећаји и стања на месту примене
Веома честа
Умор, фебрилна неутропенија, пирексија
заједнички
Астенија, периферни едем, зимица, малаксалост
Дијагностички тестови
заједнички
Повећана креатинин фосфокиназа у крви
Опис одабраних нежељених реакција
Тромботични / тромбоемболијски догађаји (ТЕЕ)
У 3 контролисана и 2 неконтролисана клиничка испитивања, међу одраслим пацијентима са хроничном ИТП који су примали елтромбопаг (н = 446), 17 испитаника доживело је укупно 19 тромбоемболијских догађаја, који су укључивали (по опадајућој учесталости) дубоку венску тромбозу (н = 6) , плућна емболија (н = 6), акутни инфаркт миокарда (н = 2), церебрални инфаркт (н = 2), емболија (н = 1) (видети одељак 4.4).
У студији контролисаној плацебом (н = 288, безбедносна популација), након 2 недеље лечења у припреми за инвазивне процедуре, 6 од 143 (4%) одраслих пацијената са хроничном болести јетре који су примали елтромбопаг доживели су 7 ТЕЕ порталног венског система а 2 од 145 испитаника (1%) у плацебо групи имало је 3 ТЕЕ. Пет од 6 пацијената лечених елтромбопагом имало је ТЕЕ са бројем тромбоцита> 200.000 / μл.
Нису идентификовани специфични фактори ризика код оних испитаника који су доживели ТЕЕ, осим броја тромбоцита ≥ 200.000 / микролитра (видети одељак 4.4).
У контролисаним студијама на тромбоцитопеничним ХЦВ-инфицираним пацијентима (н = 1439), 38 од 955 (4%) испитаника лечених елтромбопагом имало је ТЕЕ, а 6 од 484 испитаника (1%) у плацебо групи имало је ТЕЕ. Тромбоза порталне вене била је најчешћи ТЕЕ у обе групе лечења (2% код пацијената лечених елтромбопагом наспрам
Отказивање јетре (употреба са интерфероном)
Пацијенти са хроничним ХЦВ хепатитисом са цирозом могу бити изложени ризику од декомпензације јетре када примају терапију алфа интерфероном. У 2 контролисана клиничка испитивања код пацијената са тромбоцитопенијом са ХЦВ инфекцијом, декомпензација јетре (асцитес, хепатична енцефалопатија, варикозно крварење, спонтани бактеријски перитонитис) пријављена је чешће у краку елтромбопага (11%) него у групи која је примала плацебо (6%). Код пацијената са ниским нивоом албумина (≤ 35 г / Л) или МЕЛД скором ≥ 10 на почетку, постојао је три пута већи ризик од декомпензације јетре и повећан ризик од фаталног нежељеног догађаја у поређењу са онима са мањом болешћу јетре. Елтромбопаг се таквим пацијентима треба давати тек након пажљивог разматрања очекиваних користи у односу на ризике. Пацијенте са овим карактеристикама треба пажљиво пратити због знакова и симптома јетрене декомпензације (видети одељак 4.4).
Тромбоцитопенија након прекида лечења
У 3 клиничка испитивања контролисана ИТП-ом, пролазно смањење броја тромбоцита испод почетних нивоа након прекида лечења примећено је у 8% групе елтромбопага и 8% плацебо групе (видети одељак 4.4).
Повећан ретикулин у коштаној сржи
У оквиру програма ниједан пацијент није имао доказе о клинички значајним абнормалностима коштане сржи или клиничким знацима који указују на дисфункцију коштане сржи. Код малог броја пацијената са ИТП, лечење елтромбопагом је прекинуто због ретикулина коштане сржи (видети одељак 4.4).
Цитогенетске аномалије
У отвореној клиничкој студији са једном руком у ААС, пацијенти су подвргнути аспирацијама коштане сржи ради процене цитогенетских абнормалности. Нова цитогенетска абнормалност пријављена је код осам (19%) пацијената, укључујући 5 пацијената код којих је пронађена промена хромозома 7. У две текуће студије (ЕЛТ116826 и ЕЛТ116643), цитогенетске абнормалности су откривене у 4/28 (14%) и 4/62 (6%) испитаника.
Хематолошке неоплазме
Код три (7%) пацијената у једнократној, отвореној клиничкој студији ААС, МДС је дијагностикован након лечења елтромбопагом, у две текуће студије (ЕЛТ116826 и ЕЛТ116643), МДС или АМЛ су дијагностиковани код 1/28 (4 %) и 1/62 (2%) испитаника у свакој студији.
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након одобрења лека је важно, јер омогућава континуирано праћење односа користи и ризика лека. Здравствени радници се моле да пријаве сваку сумњу на нежељену реакцију преко Италијанске агенције за лекове. , веб страница: ввв.агензиафармацо.гов.ит/ит/респонсабили.
04.9 Предозирање
У случају предозирања, број тромбоцита може прекомерно порасти и довести до тромботичних / тромбоемболијских компликација. У случају предозирања, треба размислити о оралној примени препарата који садржи катјоне метала, попут препарата калцијума, алуминијума или магнезијума, за хелат елтромбопага и на тај начин ограничити његову апсорпцију. Треба пажљиво пратити број тромбоцита. Лечење елтромбопагом треба поново започети у складу са дозама и препорукама за примену (видети одељак 4.2).
У клиничким испитивањима било је извештаја о предозирању у којем је субјект прогутао 5000 мг елтромбопага. Пријављене нежељене реакције укључивале су благи осип, пролазну брадикардију, повишење АЛТ и АСТ и умор. Јетрени ензими измерени између 2. и 18. дана након узимања имали су врхунац АСТ на 1,6 пута л "ГНН, и АЛТ на 3,9 пута л" ГНН, а укупни билирубин на 2,4 пута л. "ГГН. Број тромбоцита износио је 672.000 / μл 18. дана након узимања, а максимални број тромбоцита је био 929.000 / μл.
Будући да се елтромбопаг не излучује значајно бубрезима и да је јако везан за протеине плазме, не очекује се да ће хемодијализа бити ефикасна метода за повећање елиминације елтромбопага.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: антихеморагији, други системски хемостати.
АТЦ ознака: Б02БКС 05.
Механизам дејства
Тромбопоетин (ТПО) је главни цитокин укључен у регулацију мегакарипоезе и производњу тромбоцита, и ендогени је лигант за рецептор ТПО (ТПО-Р). Елтромбопаг ступа у интеракцију са трансмембранским доменом хуманог ТПО-Р и иницира каскаду сигнала сличну, али не идентичну оној ендогеног ТПО, изазивајући пролиферацију и диференцијацију од ћелија прогенитора коштане сржи.
Клиничка ефикасност и безбедност
Студије хроничне аутоимуне (идиопатске) тромбоцитопеније (ИТП)
Две фазе ИИИ, рандомизоване, двоструко слепе, плацебом контролисане студије, РАИСЕ (ТРА102537) и ТРА100773Б и две отворене студије, РЕПЕАТ (ТРА108057) и ЕКСТЕНД (ТРА105325) процењивале су безбедност и ефикасност елтромбопага код одраслих пацијената који су претходно лечени хронични ИТП.
Све у свему, елтромбопаг је даван 277 пацијената са ИТП најмање 6 месеци и 202 пацијента најмање 1 годину.
Двоструко слепе плацебо контролисане студије
РАИСЕ: 197 пацијената са ИТП -ом рандомизовано је у односу 2: 1 на елтромбопаг (н = 135) и плацебо (н = 62), а рандомизација је стратификована спленектомијом, основном употребом за ТПИ и основним бројем тромбоцита. Доза елтромбопага је била прилагођено током периода од 6 месеци лечења на основу индивидуалног броја тромбоцита. Сви пацијенти су почели са узимањем елтромбопага у дози од 50 мг. 29. дан до краја лечења, од 15. дана 28% пацијената лечених елтромбопагом одржавано је на ≤ 25 мг и 29 до 53% примио 75 мг.
Осим тога, пацијенти би могли постепено смањивати истовремене ИТП лекове и примати третмане спасавања према локалним смерницама за лечење. Више од половине свих пацијената у свакој терапијској групи имало је ≥ 3 претходне терапије ИТП, а 36% је имало претходну спленектомију.
Средњи почетни број тромбоцита је био 16.000 / μл за обе групе лечења, а у групи са елтромбопагом је остао изнад 50.000 / μл при свим посетама током терапије, почевши од 15. дана; међутим, средњи број тромбоцита у плацебо групи је остао
Одговор на број тромбоцита између 50.000-400.000 / μл у одсуству третмана спашавања постигнут је значајно већим бројем пацијената у групи елтромбопага током шестомесечног периода лечења, п
Табела 4: Резултати секундарне ефикасности из студије РАИСЕ
модел логистичке регресије прилагођен случајним варијаблама стратификације
б 21 од 63 (33%) пацијената лечених елтромбопагом који су узимали основни лек за ИТП трајно је прекинуо све основне лекове за ИТП.
На почетку, више од 70% пацијената са ИТП-ом у свакој терапијској групи пријавило је крварење било које врсте (СЗО степен 1-4), а више од 20% је пријавило клинички значајно крварење (степен 2-4 СЗО). Удео пацијената лечених елтромбопагом са крварењем било које врсте (1-4. Степен) и клинички значајним крварењем (2-4. Степен) смањио се од почетне вредности за приближно 50% од 15. дана до краја лечења током периода од 6 месеци лечења .
ТРА100773Б: Л "крајња тачка примарна ефикасност била је пропорција одговори, дефинисани као пацијенти са ИТП -ом који су имали повећан број тромбоцита на ≥ 50.000 / μл на дан 43. са почетне вредности од 200.000 / μл одговори, узети су у обзир они који су прекинули из било ког другог разлога неодговарајући без обзира на број тромбоцита. Укупно 114 пацијената са претходно леченим хроничним ИТП -ом рандомизовано је 2: 1 у елтромбопаг (н = 76) и плацебо (н = 38).
Табела 5: Резултати ефикасности из студије ТРА100773Б
а - Модел логистичке регресије прилагођен за варијабле рандомизиране стратификације
И у РАИСЕ -у и у ТРА100773Б, одговор на елтромбопаг у поређењу са плацебом био је сличан без обзира на ИТП лек који се користи, спленектомију и основни број тромбоцита (≤ 15.000 / μл,> 15.000 / μл) при рандомизацији.
У студијама РАИСЕ и ТРА100773Б у подгрупи пацијената са ИТП -ом са основним бројем тромбоцита ≤ 15.000 / μл није постигнут потребан ниво (> 50.000 / μл) средњег броја тромбоцита, иако је у обе студије 43% ових пацијената лечених елтромбопагом одговорило је на крају шестонедељног периода лечења. Осим тога, у студији РАИСЕ, 42% пацијената са почетним бројем тромбоцита ≤ 15.000 / μл лечених елтромбопагом одговорило је на крају шестомесечног периода лечења. Четрдесет два до 60% пацијената лечених елтромбопагом у студији РАИСЕ примало је 75 мг од 29. дана до краја лечења.
Отворена студија, поновљена доза (3 курса од 6 недеља лечења, промењена са 4 недеље без лечења) показала је да епизодична употреба са више курсева елтромбопага није резултирала смањењем одговора.
Елтромбопаг је даван 302 пацијента са ИТП-ом у отвореној континуираној студији ЕКСТЕНД (ТРА105325), 218 завршених 1 годину, 180 завршених 2 година, 107 завршених 3 година, 75 завршених 4 године, 34 завршених 6 година и 18 завршених 6 година. Средњи број тромбоцита на почетку је био 19.000 / μл пре примене елтромбопага. Средњи број тромбоцита у 1, 2, 3, 4, 5, 6 и 7 година студије био је 85.000 / микролитра, 85.000 / микролитара, 105.000 / микролитара, 64.000 / микролитара, 75.000 / микролитара, 119.000 / микролитара и 76.000 / микролитра микролитара, респективно.
Нису спроведена клиничка испитивања која упоређују елтромбопаг са другим терапеутским могућностима (нпр. Спленектомија). Пре почетка лечења треба размотрити дугорочну безбедност елтромбопага.
Педијатријска популација (старости 1-17 година)
Сигурност и ефикасност елтромбопага код педијатријских испитаника процењивана је у две студије. ТРА115450 (ПЕТИТ2): Примарни крајњи циљ био је дуготрајан одговор, дефинисан као удео испитаника лечених елтромбопагом, у поређењу са плацебом, који су постигли број тромбоцита ≥50.000 / мцл током најмање 6 од 8 недеља (у одсуству спасилачке терапије), између 5. и 5. недеље 12 током рандомизованог двоструко слепог периода. Субјекти код којих је дијагностикован хронични ИТП најмање 1 годину и који су били рефракторни или су се вратили на најмање једну претходну терапију ИТП-а или из неког разлога нису могли да наставе друге третмане ИТП-а и имали су број тромбоцита
Свеукупно, значајно већи проценат испитаника у групи елтромбопага (40%) постигао је примарну крајњу тачку (однос квота: 18,0 [95% ЦИ: 2,3, 140,9] п
Табела 6: Стопе одрживог одговора тромбоцита према кохортној доби у педијатријских субјеката са хроничном ИТП
Статистички је мање испитаника који су примали елтромбопаг захтевало спасавање током рандомизираног периода од испитаника који су примали плацебо (19% [12/63] наспрам 24% [7/29], п = 0,032).
На почетку, 71% испитаника у групи која је примала елтромбопаг и 69% у плацебо групи пријавило је крварење (оцене СЗО 1-4). У 12. недељи, удео испитаника лечених елтромбопагом који су пријавили крварење преполовљен је у односу на почетну вредност (36%). Поређења ради, у 12. недељи 55% испитаника који су примали плацебо није пријавило крварење.
Испитаницима је било дозвољено да смање или прекину позадинску ИТП терапију само током отворене фазе студије, а 53% (8/15) испитаника је успело да смањи (н = 1) или прекине (н = 7) основну терапију за ИТП, углавном кортикостероиди, без потребе за терапијом спасавања.
ТРА108062 (ПЕТИТ): Примарни крајњи циљ био је проценат испитаника који су постигли број тромбоцита ≥50.000 / мцл најмање једном између 1. и 6. недеље рандомизованог периода. Субјекти су били рефракторни или су се вратили на најмање једну претходну ИТП терапију и са тромбоцитима
Свеукупно, значајно већи проценат испитаника у групи елтромбопага (62%) постигао је примарну крајњу тачку (однос квота: 4,3 [95% ЦИ: 1,4, 13,3] п = 0,011).
Одрживи одговор је примећен код 50% почетних испитаника након 20 од 24 недеље у студији ПЕТИТ 2 и 15 од 24 недеље у студији ПЕТИТ.
Студије тромбоцитопеније повезане са хроничним ХЦВ хепатитисом
Ефикасност и безбедност елтромбопага у лечењу тромбоцитопеније код пацијената инфицираних ХЦВ процењивани су у две рандомизоване, двоструко слепе, плацебом контролисане студије ЕНАБЛЕ 1 је користио пегинтерферон алфа-2а плус рибавирин за антивирусно лечење и ЕНАБЛЕ 2 је користио пегинтерферон алфа- 2б плус рибавирин. Пацијенти нису примали антивирусне лекове директног дејства. У обе студије, укључени су пацијенти са прегледом броја тромбоцита (
Основне карактеристике болести биле су сличне у обе студије и биле су у складу са популацијом пацијената заражених ХЦВ-ом са компензованом цирозом. Већина пацијената је имала ХЦВ генотип 1 (64%) и имала је премошћујућу фиброзу / цирозу. Тридесет један проценат пацијената је претходно био лечен терапијама за ХЦВ инфекцију, углавном пегилованим интерфероном плус рибавирином. Средњи број тромбоцита на почетку је био 59.500 / μл у обе групе лечења: 0,8%, 28% и 72% регрутованих пацијената имало је тромбоците рачуна
Студије су се састојале од две фазе - антивирусне фазе предтретмана и фазе антивирусног лечења. У фази антивирусног третмана, субјекти су примали отворени елтромбопаг да повећају број тромбоцита на ≥ 90,000 / мцл за ЕНАБЛЕ 1 и ≥ 100,000 / мцл за ЕНАБЛЕ 2. Средње време до постизања циљаног броја тромбоцита од ≥ 90,000 / мцл (ЕНАБЛЕ 1 ) или ≥ 100,000 / мцл (ЕНАБЛЕ 2) било је 2 недеље.
Л "крајња тачка примарна ефикасност у обе студије била је одрживи виролошки одговор (непрекидан виролошки одговор, СВР), дефинисан као проценат пацијената са ХЦВ инфекцијом са неоткривеном ХЦВ РНК 24 недеље након завршетка планираног периода лечења.
У обе студије заражене ХЦВ-ом, значајно већи проценат пацијената лечених елтромбопагом (н = 201, 21%) постигао је СВР у поређењу са онима који су лечени плацебом (н = 65, 13%) (видети Табелу 7). Побољшање у проценту пацијената који су постигли СВР било је доследно у свим подгрупама у свим рандомизованим стратумима (основни број тромбоцита (вс.> 50.000), вирусно оптерећење (вс. ≥ 800.000 ИУ / мЛ) и генотип (2/3 вс. 1/4/6).
Табела 7: Виролошки одговор пацијената са ХЦВ инфекцијом у ЕНАБЛЕ 1 и ЕНАБЛЕ 2
елтромбопаг који се даје у комбинацији са пегинтерфероном алфа-2а (180 μг једном недељно током 48 недеља за генотипове 1/4/6; 24 недеље за генотипове 2/3) плус рибавирин (од 800
1200 мг дневно у 2 подељене дозе, орално)
б Елтромбопаг који се примењује у комбинацији са пегинтерфероном алфа-2б (1,5 мцг/кг једном недељно 48 недеља за генотип 1/4/6; 24 недеље за генотип 2/3) плус рибавирин (800 до 1400 мг орално у 2 подељене дозе)
ц Циљани број тромбоцита је био ≥ 90.000 / мцл за ЕНАБЛЕ 1 и ≥ 100,000 / мцл за ЕНАБЛЕ 2. За ЕНАБЛЕ 1, 682 пацијената је рандомизовано у фазу антивирусног лечења; међутим 2 испитаника су затим повукла пристанак пре него што су примили антивирусну терапију.
д вредност п у односу на плацебо
а 64% испитаника који су учествовали у студијама ЕНАБЛЕ 1 и ЕНАБЛЕ 2 имали су генотип 1
ф Пост-хоц анализе
Друга секундарна запажања из студија укључивала су следеће: Значајно мање пацијената лечених елтромбопагом прерано је прекинуло антивирусну терапију у поређењу са онима који су лечени плацебом (45% вс. 60%, п = наспрам 27%). Лечење елтромбопагом је одложило и смањило број смањења дозе пегинтерферона.
Тешка апластична анемија
Елтромбопаг је проучаван у једној руци, са једним центром, отвореном клиничком студијом на 43 пацијента са тешком апластичном анемијом са рефракторном тромбоцитопенијом након најмање једне претходне имуносупресивне терапије (СТИ) и са бројем тромбоцита ≤ 30.000 / μл.
За већину испитаника, 33 (77%), сматрало се да имају „примарну рефракторну болест“, дефинисану као „одсуство адекватног првог одговора на имуносупресивну терапију у било којој линији. Преосталих 10 испитаника имало је одговор тромбоцита. претходних 10 терапија. Свих 10 примљених прошло је најмање 2 претходна режима имуносупресивне терапије, а 50% је примило најмање 3 претходна режима имуносупресивне терапије. Пацијенти са дијагнозом анемије
Фанцони, инфекција која не реагује на одговарајућу терапију, клон ПНХ у неутрофилима величине ≥ 50%, искључени су из студије.
На почетку, средњи број тромбоцита је био 20.000 / μл, хемоглобин је био 8.4 г / дЛ, апсолутни број неутрофила је био 0.58 к 109 / л, а апсолутни број ретикулоцита је био 24.3 к109 / 1. Осамдесет шест посто пацијената зависило је од еритроцита трансфузије, а 91% је зависило од трансфузије тромбоцита.Већина пацијената (84%) је претходно примила најмање 2 имуносупресивне терапије. Три пацијента су имала цитогенетске абнормалности на почетку.
Примарни крајњи циљ био је хематолошки одговор процењен након 12 недеља лечења елтромбопагом.Хематолошки одговор је дефинисан као постизање једног или више следећих критеријума: 1) повећање броја тромбоцита на 20.000 / μл изнад почетне вредности или број тромбоцита стабилан са независношћу од трансфузије за најмање 8 недеља; 2) повећање хемоглобина> 1,5 г / дл или смањење трансфузије ≥ 4 јединице црвених крвних зрнаца (РБЦ) током 8 узастопних недеља; 3) повећање апсолутног броја неутрофила (АНЦ) за 100% или повећање АНЦ> 0,5 к 109 / Л.
Стопа хематолошког одговора била је 40% (17/43 пацијената; 95% ЦИ 25, 56), а већина одговора била је ограничена на једну линију (13 / 17,76%), док су забележена 3 одговора. -линеарни одговор у 12. недељи. Елтромбопаг је прекинут након 16 недеља ако није примећен хематолошки одговор или независност од трансфузије. Испитаници су наставили терапију у продуженој фази студије. Укупно 14 пацијената је учествовало у продуженој фази студије. Девет од ових пацијената постигло је мулти-линеарни одговор, 4 од 9 је наставило лечење, а 5 је постепено опадало са лечењем елтромбопагом и одржавањем одговора (праћење). Медијана: 20,6 месеци, распон: 5,7 до 22,5 месеци) Преосталих 5 пацијената је прекинуло лечење, три због рецидива уоченог током посете продужетка у трећем месецу.
Током лечења елтромбопагом 59% (23/39) је постало независно од трансфузије тромбоцита (28 дана без трансфузије тромбоцита), а 27% (10/37) је постало независно од трансфузије еритроцита (56 дана без трансфузије еритроцита). Најдужи период без трансфузије тромбоцита за особе које нису одговориле био је 27 дана (средња вредност). Најдужи период без трансфузије тромбоцита за испитанике био је 29 дана (средња вредност). Најдужи период без трансфузије еритроцита за испитанике био је 266 дана (средња вредност).
Преко 50% испитаника који су на почетку били зависни од трансфузије имало је> 80% смањење потребе за трансфузијом тромбоцита и еритроцита од почетне вредности.
Прелиминарни резултати супортивне студије (Студија ЕЛТ116826), која је у току, не насумична, фаза ИИ, једнокрака, отворена студија на ватросталним субјектима са ААС, показали су доследне резултате. Подаци су ограничени на 21 од 60 предвиђених пацијената, а хематолошки одговор је примећен код 52% пацијената након 6 месеци. Мулти-линеарни одговори пријављени су код 45% пацијената.
05.2 Фармакокинетичка својства
Фармакокинетика
Подаци концентрације елтромбопага у плазми - време прикупљено код 88 пацијената са ИТП у ТРА100773А и ТРА100773Б комбиновано је са подацима о 111 здравих одраслих испитаника у популационој фармакокинетичкој анализи. Приказане су процене АУЦ (0-?) И Цмак елтромбопага у плазми код пацијената са ИТП (Табела 8).
Табела 8: Геометријска средина (95% интервал поузданости) фармакокинетичких параметара плазме елтромбопага у равнотежном стању код одраслих са ИТП
а-Процене АУЦ (0-?) и Цмак засноване на пост-хоц популационим фармакокинетичким вредностима.
Подаци о концентрацијама елтромбопага у плазми током времена прикупљени у 590 испитаника инфицираних ХЦВ -ом укључених у студије ИИИ фазе ТПЛ103922 / ЕНАБЛЕ 1 и ТПЛ108390 / ЕНАБЛЕ 2 комбиновани су са подацима пацијената са ХЦВ -ом укључених у студију ИИ фазе ТПЛ102357 и здравих одраслих испитаника у популационе фармакокинетичке анализе. Процене Цмак и АУЦ плазме елтромбопага у плазми (0-?) У пацијената инфицираних ХЦВ-ом укључених у испитивање фазе 3 наведене су за сваку дозу у Табели 9.
Табела 9 Геометријска средина (95% ЦИ) ало стабилно стање фармакокинетички параметри плазме елтромбопага у пацијената са хроничном ХЦВ инфекцијом
Подаци представљени као геометријска средина (95% ЦИ).
АУЦ (0-?) И Цмак на основу процена пост-хоц популацијска фармакокинетика при највећој дози у подацима сваког пацијента.
Апсорпција и биорасположивост
Елтромбопаг се апсорбује са највећом концентрацијом која се јавља 2 до 6 сати након оралне примене. Истовремена примена елтромбопага са антацидима и другим производима који садрже поливалентне катионе, попут млечних производа и минералних суплемената, значајно смањује изложеност елтромбопагу (видети одељак 4.2).. У студији релативне биорасположивости код одраслих, прах елтромбопага за оралну суспензију постигао је 22% већу АУЦ у плазми (0-?) У поређењу са формулацијом таблете. Апсолутна орална биорасположивост елтромбопага након људске примене није утврђена. На основу излучивања урином и метаболита излучених фецесом, процењено је да је орална апсорпција супстанци повезаних са лековима након примене појединачне дозе раствора од 75 мг елтромбопага процењена на најмање 52%.
Дистрибуција
Елтромбопаг се у великој мери везује за протеине хумане плазме (> 99,9%), претежно за албумин. Елтромбопаг је БЦРП супстрат, али није П-гликопротеин или ОАТП1Б1 супстрат.
Биотрансформација
Елтромбопаг се примарно метаболише цепањем, оксидацијом и коњугацијом са глукуронском киселином, глутатионом или цистеином. У радиоактивно обележеној студији на људима, елтромбопаг чини приближно 64% АУЦ0-? плазма концентрација радиоактивно обележеног угља. Такође су пронађени мањи метаболити услед глукуронидације и оксидације. образовање ин витро сугеришу да су ЦИП1А2 и ЦИП2Ц8 одговорни за оксидативни метаболизам елтромбопага. Уридин дифосфоглукуронил трансферазе УГТ1А1 и УГТ1А3 одговорне су за глукуронидацију, а бактерије из доњег гастроинтестиналног тракта могу бити одговорне за цепање.
Елиминација
Након апсорпције, елтромбопаг се интензивно метаболише. Претежни начин излучивања елтромбопага је путем измета (59%), а 31% дозе се налази у урину у облику метаболита. Непромењено једињење (елтромбопаг) се не открива у урину. Непромењени елтромбопаг излучен фецесом представља приближно 20% дозе. Полувреме елиминације елтромбопага из плазме је приближно 21-32 сата.
Фармакокинетичке интеракције
На основу студије спроведене на људима са радиоактивно обележеним елтромбопагом, глукуронидација игра мању улогу у метаболизму елтромбопага. Студије на микросомима људске јетре су идентификовале УГТ1А1 и УГТ1А3 као ензиме одговорне за глукуронидацију елтромбопага. Елтромбопаг је инхибитор неколико ензима УГТ. ин витро. Не очекују се клинички значајне интеракције лекова које укључују глукуронидацију због ограниченог доприноса појединачних ензима УГТ у глукуронидацији елтромбопага и потенцијалних истовремених лекова.
Отприлике 21% дозе елтромбопага могло би бити подвргнуто оксидативном метаболизму. Студије на микросомима јетре код људи идентификовале су ЦИП1А2 и ЦИП2Ц8 као ензиме одговорне за оксидацију елтромбопага. Елтромбопаг не инхибира или индукује ензиме ЦИП на основу података ин витро и ин виво (види одељак 4.5)
образовање ин витро показао је да је елтромбопаг инхибитор транспортера ОАТП1Б1 и да је инхибитор транспортера БЦРП и елтромбопага у студији клиничке интеракције повећава изложеност ОАТП1Б1 и БЦРП супстрата росувастатина (видети одељак 4.5). У клиничким студијама са елтромбопагом он је имао препоручено је смањење дозе статина за 50%. Истовремена примена 200 мг циклоспорина (инхибитора БЦРП) смањила је Цмак и АУЦинф елтромбопага за 25% и 18% респективно. Истовремена примена 600 мг циклоспорина смањила је Цмак и АУЦинф елтромбопага за 39% и 24%, респективно.
Елтромбопаг хелатира поливалентне катионе као што су гвожђе, калцијум, магнезијум, алуминијум, селен и цинк (видети одељке 4.2 и 4.5).
Примена појединачне дозе елтромбопага од 50 мг у таблетама са стандардним висококалоричним оброком, доручак са високим садржајем масти који је укључивао млечне производе, смањила је средњу АУЦ0-> елтромбопага у плазми за 59%, а Цмак у просеку за 65%.
Примена појединачне дозе од 25 мг елтромбопага у праху за оралну суспензију уз оброк са високим садржајем калцијума, умерене масти и калорија смањила је средњу АУЦ0-? Елтромбопага у плазми за 75% и средњу Цмак за 79%. Ово смањење изложености је ублажено када једна доза од 25 мг елтромбопага у праху за оралну суспензију давана је 2 сата пре оброка са високим садржајем калцијума (средња АУЦ0-? Смањена за 20% и средња Цмак од 14%).
Храна са ниским садржајем калцијума (воће, посна шунка, говедина и воћни сокови без додатка калцијума, магнезијума или гвожђа), сојино млеко без додавања и пшеница немају значајан утицај на изложеност елтромбопага плазми, без обзира на садржај калорија и масти (видети одељке 4.2 и 4.5).
Посебне популације пацијената
Инсуфицијенција бубрега
Фармакокинетика елтромбопага је проучавана након примене елтромбопага код одраслих особа са бубрежном инсуфицијенцијом. Након примене појединачне дозе од 50 мг, АУЦ0-? Елтромбопага била је 32% до 36% нижа код испитаника са благим до умереним оштећењем бубрега, а 60% нижа код испитаника са тешким оштећењем бубрега у поређењу са здравим добровољцима. варијабилност и значајно преклапање у изложености између пацијената са бубрежном инсуфицијенцијом и здравих добровољаца. Нису мерене слободне (активне) концентрације елтромбопага за овај лек који се везује за протеине. Пацијенти са оштећеном бубрежном функцијом треба да користе елтромбопаг са опрезом и уз пажљиво праћење, на пример извођење серумског креатинина и / или анализе урина (видети одељак 4.2). Ефикасност и безбедност елтромбопага нису утврђене. код особа са умереном до тешком бубрежном инсуфицијенцијом и инсуфицијенцијом јетре.
Хепатична инсуфицијенција
Фармакокинетика елтромбопага је проучавана након примене елтромбопага код одраслих особа са хепатичном инсуфицијенцијом. Након примене појединачне дозе од 50 мг, АУЦ0-? Елтромбопага била је 41% већа код испитаника са благим оштећењем јетре, а 80% до 93% већа код испитаника са умереним до умереним оштећењем јетре, тешким, у поређењу са здравим добровољцима. Постојала је значајна варијабилност и значајно преклапање у изложености између пацијената са инсуфицијенцијом јетре и здравих добровољаца. Концентрације слободног (активног) елтромбопага за овај лек са високим степеном везивања за протеине нису мерене.
Утицај јетрене инсуфицијенције на фармакокинетику елтромбопага након поновљене примене процењен је популационом фармакокинетичком анализом код 28 здравих одраслих особа и 714 пацијената са оштећењем јетре (673 пацијента са ХЦВ инфекцијом и 41 пацијент са хроничном болешћу јетре друге етиологије). Од ових 714 пацијената, 642 је имало благу инсуфицијенцију јетре, 67 је имало умерену инсуфицијенцију јетре, а 2 су имали тешку инсуфицијенцију јетре. У поређењу са здравим добровољцима, пацијенти са благим оштећењем јетре имали су АУЦ елтромбопага у плазми (0-?) Вредности веће од приближно 111% (95% ЦИ: 45% до 283%), а пацијенти са умереним оштећењем јетре имали су АУЦ елтромбопага у плазми ( 0-?) Већи од приближно 183% (95% ЦИ: 90% до 459%).
Због тога се елтромбопаг не сме примењивати код пацијената са ИТП са умереним до тешким оштећењем јетре (Цхилд-Пугх скор ≥ 5) осим ако очекивана корист надмашује идентификовани ризик од тромбозе порталне вене (видети одељке 4.2 и 4.4). Код пацијената заражених ХЦВ -ом, елтромбопаг започните у дози од 25 мг једном дневно (видети одељак 4.2).
Трка
Утицај источноазијске етничке припадности на фармакокинетику елтромбопага процењен је популационом фармакокинетичком анализом на 111 здравих одраслих особа (31 источноазијски) и 88 пацијената са ИТП (18 источноазијских). На основу процена из популационих фармакокинетичких анализа, источноазијски ИТП пацијенти (нпр. као Јапанци, Кинези, Тајванци и Корејци) имали су приближно 49% веће вредности АУЦ елтромбопага у плазми (0-?) у поређењу са пацијентима који нису били у Источној Азији, који су били претежно белци (видети одељак 4.2).
Утицај источноазијске етничке припадности (као што су Кинези, Јапанци, Тајванци, Корејци и Тајланђани) на фармакокинетику елтромбопага процијењен је помоћу популацијске фармакокинетичке анализе на 635 пацијената заражених ХЦВ -ом (145 источноазијских и 69 југоисточних Азијата) На основу процјена становништва фармакокинетичком анализом, пацијенти источноазијске етничке припадности имали су приближно 55% веће вредности АУЦ елтромбопага у плазми (0-?) у поређењу са пацијентима других раса, за које су били претежно белци (видети одељак 4.2).
Сек
Утицај пола на фармакокинетику елтромбопага процијењен је популационом фармакокинетичком анализом код 111 здравих одраслих особа (14 жена) код 88 пацијената са ИТП (57 жена).На основу процена популационих фармакокинетичких анализа, ИТП пацијенткиње су имале приближно 23% веће вредности АУЦ (0-?) Елтромбопага у плазми у поређењу са мушким пацијентима, без прилагођавања разлика у телесној маси.
Утицај пола на фармакокинетику елтромбопага процијењен је популационом фармакокинетичком анализом код 635 пацијената заражених ХЦВ-ом (260 жена). На основу процена модела, пацијенткиње са ХЦВ инфекцијом имале су приближно 41% веће вредности АУЦ елтромбопага у плазми (0-?) У поређењу са мушкарцима.
Старост
Утицај старости на фармакокинетику елтромбопага процењен је популационом фармакокинетичком анализом код 28 здравих испитаника, 673 пацијената са ХЦВ инфекцијом и 41 пацијента са хроничном болешћу јетре друге етиологије у доби од 19 година. 74. Нема доступних фармакокинетичких података о употреба елтромбопага код пацијената старијих од 75 година. На основу процена модела, старији пацијенти (≥ 65 година) имали су приближно 41% веће вредности АУЦ елтромбопага у плазми (0-?) У поређењу са млађим пацијентима (видети одељак 4.2).
Педијатријска популација (старости 1-17 година)
Фармакокинетика елтромбопага је процењивана код 168 педијатријских испитаника са ИТП у две студије једном дневно, ТРА108062 / ПЕТИТ и ТРА115450 / ПЕТИТ-2. Привидни клиренс елтромбопага у плазми након оралне примене (ЦЛ / Ф) повећавао се са повећањем телесне тежине.
Ефекти расе и пола на процене ЦЛ / Ф елтромбопага у плазми били су конзистентни између педијатријских и одраслих пацијената. Источноазијски педијатријски пацијенти са ИТП-ом имали су приближно 43% већу АУЦ елтромбопага у плазми (0-?) У односу на неисточноазијске пацијенте. Женске педијатријске ИТП пацијенткиње имале су приближно 25% повећање "АУЦ-а (плазме) плазме (0-?) Елтромбопага у поређењу са мушкарцима .
Фармакокинетички параметри елтромбопага код педијатријских испитаника са ИТП приказани су у Табели 10.
Табела 10. Геометријска средина (95% ЦИ) стационарних фармакокинетичких параметара концентрације елтромбопага у плазми код педијатријских испитаника са ИТП (режим дозирања 50 мг једном дневно)
Подаци представљени као геометријска средина (95% ЦИ). АУЦ (0-?) И Цмак су засноване на пост хоц фармакокинетичким проценама популације.
05.3 Предклинички подаци о безбедности
Елтромбопаг не стимулише производњу тромбоцита код мишева, пацова или паса због специфичности јединственог рецептора ТПО. Стога подаци изведени од ових животиња не представљају потпуни модел за процену потенцијалних фармаколошки повезаних штетних ефеката елтромбопага на људе. репродуктивне и канцерогене студије.
Катаракта повезана са третманом откривена је код глодара и зависила је од дозе и времена. При експозицијама већим од 6 пута од клиничке изложености људи код одраслих пацијената са ИТП у дози од 75 мг / дан и при изложености 3 пута од клиничке изложености код људи код одраслих пацијената инфицираних ХЦВ-ом од 100 мг / дан, изложености засноване на АУЦ, катаракта је била примећено код мишева после 6 недеља и код пацова после 28 недеља лечења. При изложености већој или једнакој 4 пута клиничкој изложености код људи код пацијената са ИТП -ом од 75 мг / дан и Излагању 2 пута већој од клиничке изложености код људи код пацијената инфицираних ХЦВ -ом доза од 100 мг / дан, изложеност заснована на АУЦ -у, катаракта је примећена код мишева након 13 недеља и код пацова након 39 недеља лечења. У дозама које се не толеришу код малолетних пацова пре одбића који су примењени од 4. до 32. дана (приближно 2 људске године на крају периода дозирања), уочено је замућење ока (хистологија није извршена) у једнаким дозама од 75 мг / дан. 9 пута највећа клиничка изложеност код људи код педијатријских пацијената са ИТП -ом, на основу АУЦ -а. Међутим, није примећена катаракта код млађих пацова којима су даване толерисане дозе 5 пута веће од клиничке изложености људи код педијатријских пацијената са ИТП, на основу АУЦ -а. Није примећена катаракта код одраслих паса након 52 недеље лечења (2 пута већа од клиничке изложености код људи код одраслих или педијатријски пацијенти са ИТП у дози од 75 мг / дан и еквивалентно клиничкој изложености код људи код пацијената са ХЦВ инфекцијом у дози од 100 мг / дан, на основу АУЦ).
У студијама на мишевима и пацовима у трајању до 14 дана, забележена је токсичност бубрежних тубула при изложености која је генерално била повезана са морбидитетом и морталитетом. Тубуларна токсичност је такође примећена у двогодишњој оралној студији канцерогености на мишевима у дозама од 25, 75 и 150 мг / кг / дан. Ефекти су били мањи при мањим дозама и окарактерисани су низом регенеративних модификација. Изложеност при најнижој дози била је 1,2 или 0,8 пута већа од клиничке изложености код људи на основу АУЦ код одраслих или педијатријских пацијената са ИТП -ом у дози од 75 мг / дан и 0,6 пута Л. клиничка изложеност код људи у ХЦВ -а у дози од 100 мг / дан, изложености на основу АУЦ -а. Бубрежни ефекти нису примећени код пацова након 28 недеља или код пса након 52 недеље при изложености 4 и 2 пута већој од клиничке изложености.у људи код одраслих пацијената са ИТП и 3 и 2 пута у односу на клиничку изложеност код људи код педијатријских пацијената са ИТП у дози од 75 мг / дан и при излагању 2 пута и еквивалентно клиничкој изложености људи код пацијената са ХЦВ у дози од 100 мг / дан, изложености засноване на АУЦ.
Дегенерација и / или некроза хепатоцита, често праћена повишеним серумским јетреним ензимима, примећена је код мишева, пацова и паса у дозама које су биле повезане са морбидитетом и морталитетом или су се слабо подносиле. Нису примећени никакви ефекти на јетру након хроничног лечења код пацова (28 недеља) и паса (52 недеље) при изложености 4 или 2 пута већој од клиничке изложености код људи код одраслих пацијената са ИТП и изложености 3 или 2 пута веће од клиничке изложености. Код људи код педијатријских пацијената са ИТП у дози од 75 мг / дан и 2 пута или еквивалентно клиничкој изложености људи код пацијената заражених ХЦВ -ом у дози од 100 мг / дан, изложености засноване на АУЦ.
У краткотрајним студијама, при слабо подношљивим дозама код пацова и паса (изложеност већа од 10 или 7 пута већа од клиничке изложености људи код одраслих или педијатријских пацијената са ИТП-ом у дози од 75 мг / дан и изложеност већа од 4 пута 1 "клиничка за људе примећена је изложеност код пацијената инфицираних ХЦВ -ом у дози од 100 мг / дан, изложеност заснована на АУЦ -у), смањени број ретикулоцита и регенеративна еритроидна хиперплазија коштане сржи (само за пацове). до 28 недеља код пацова, 52 недеље код паса и 2 године код мишева или пацова у максимално толерисаним дозама, што је одговарало 2 до 4 пута већој изложености људи клиничкој изложености код одраслих или педијатријских пацијената са ИТП у дози од 75 мг / дан и при изложености мањој од 2 пута од клиничке изложености људи код пацијената заражених ХЦВ-ом у дози од 100 мг / дан, изложеност јони засновани на АУЦ.
Ендостеална хиперостоза је примећена у 28-недељној студији токсичности на пацовима у неподношљивој дози од 60 мг / кг / дан (6 пута или 4 пута већа од клиничке изложености људи код одраслих или педијатријских пацијената са ИТП у дози од 75 мг / дан и 3 пута већа клиничка изложеност људи у пацијената инфицираних ХЦВ -ом у дози од 100 мг / дан, изложености засноване на АУЦ -у). Нису примећене промене костију код мишева или пацова након изложености доживотном трајању (2 године) при 4 или 2 пута већој клиничкој изложености код људи код одраслих или педијатријских пацијената са ИТП у дози од 75 мг / дан и 2 пута већој клиничкој изложености код људи у пацијената са ХЦВ у дози од 100 мг / дан, изложености засноване на АУЦ.
Елтромбопаг није био канцероген код мишева у дозама до 75 мг / кг / дан или код пацова у дозама до 40 мг / кг / дан (изложеност до 4 или 2 пута већа од клиничке изложености људи код одраслих или педијатријских пацијената са ИТП на доза од 75 мг / дан и 2 пута већа од клиничке изложености људи код пацијената инфицираних ХЦВ-ом у дози од 100 мг / дан, изложеност заснована на АУЦ-у). ин виво код пацова (микронуклеусна и непланирана синтеза ДНК, 10 или 8 пута већа клиничка изложеност људи код одраслих или педијатријских пацијената са ИТП у дози од 75 мг / дан и 7 пута већа од клиничке изложености људи код пацијената са ХЦВ инфекцијом у дози од 100 мг / дан, изложености засноване на Цмак). У тесту ин витро на лимфому миша, елтромбопаг је био маргинално позитиван (повећане мутације). Ова запажања ин витро И ин виво сугеришу да елтромбопаг не представља генотоксичан ризик за људе.
Елтромбопаг не утиче на плодност женки, рани развој ембриона или ембриофетални развој код пацова у дозама до 20 мг / кг / дан (2 пута већа клиничка изложеност код људи код одраслих или адолесцената (12 до 17 година) са ИТП у дози 75 мг / дан и еквивалентно клиничкој изложености људи код пацијената са ХЦВ инфекцијом у дози од 100 мг / дан, изложености засноване на АУЦ). Такође није било ефекта на ембриофетални развој код зечева у дозама до 150 мг / кг / дан, највећој тестираној дози (0,3 до 0,5 пута већа од клиничке изложености људи код пацијената са ИТП у дози од 75 мг / дан и код ХЦВ-инфицираних пацијенти у дози од 100 мг / дан, изложености засноване на АУЦ) .Клиничка изложеност људи код пацијената са ИТП у дози од 75 мг / дан и 3 пута већа од клиничке изложености код људи у пацијената са ХЦВ инфекцијом у дози од 100 мг / дан, изложености засноване на АУЦ-у), лечење елтромбопагом било је повезано са ембрионалном смртношћу (повећан губитак пре и после имплантације), смањеном телесном тежином фетуса и тежином трудне материце у студији плодности жена и ниском учесталошћу цервикалних ребара и смањењем фетуса телесна тежина у женској студији плодности. студија ембрионалног и феталног развоја Елтромбопаг треба користити током трудноће само ако очекивана корист оправдава потенцијални ризик за фетус (видети одељак 4.6). Елтромбопаг није утицао на плодност код мушких пацова у дозама до 40 мг / кг / дан, највећа тестирана доза (3 пута већа клиничка изложеност људи код пацијената са ИТП -ом од 75 мг / дан и 2 пута л "клиничка изложеност људи код пацијената заражених ХЦВ -ом у дози од 100 мг / дан, изложености засноване на АУЦ-у). У студији пре и постнаталног развоја пацова није било штетних ефеката на трудноћу, пород или лактацију женки Ф0 пацова у неотровним дозама за мајку (10 и 20) мг / кг / дан) и нема утицаја на раст, развој, неуролошко понашање или репродуктивну функцију потомака (Ф1).
Елтромбопаг је откривен у плазми свих потомака пацова Ф1 током целог периода узорковања од 22 сата након давања лека мајкама Ф0, што указује на то да је изложеност неонаталних пацова елтромбопагу највероватније последица лактације.
образовање ин витро са елтромбопагом указују на потенцијални ризик од фототоксичности; међутим, код глодара није било доказа о фототоксичности коже (10 или 7 пута већа клиничка изложеност људи код одраслих или педијатријских пацијената са ИТП -ом у дози од 75 мг / дан и 5 пута већа од клиничке изложености код пацијената у дози од ХЦВ 100 мг / дан, изложености засноване на АУЦ -у) или фототоксичности ока (изложености веће од 4 пута од клиничке изложености људи код одраслих или педијатријских пацијената са ИТП -ом од 75 мг / дан и 3 пута веће клиничке изложености код пацијената код пацијената инфицираних ХЦВ -ом у дози од 100 мг / дан, изложености засноване на АУЦ -у). Штавише, клиничка фармаколошка студија на 36 испитаника није показала доказе да је фотосензитивност повећана након примене 75 мг елтромбопага. Ово је мерено одложеним фототоксичним индексом, али се потенцијални ризик од фотоалергије не може искључити јер се не могу извести посебне претклиничке студије.
Нема налаза код младих пацова који указују на већи ризик од токсичности при терапији елтромбопагом код педијатријских пацијената него код одраслих са ИТП.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Револаде 12,5 мг филмом обложене таблете
Језгро таблета
Магнезијум стеарат
Манитол (Е421)
Микрокристална целулоза
Повидон (К30)
Натријум скроб гликолат
Облога таблета
Хипромелоза
Макрогол 400
Полисорбат 80
Титанијум диоксид (Е171)
Револаде 25 мг филмом обложене таблете
Језгро таблета
Магнезијум стеарат
Манитол (Е421)
Микрокристална целулоза
Повидоне
Натријум скроб гликолат
Облога таблета
Хипромелоза
Макрогол 400
Полисорбат 80
Титанијум диоксид (Е171)
Револаде 50 мг филмом обложене таблете
Језгро таблета
Магнезијум стеарат
Манитол (Е421)
Микрокристална целулоза
Повидоне
Натријум скроб гликолат
Облога таблета
Хипромелоза
Црвени оксид гвожђа (Е172)
Жути оксид гвожђа (Е172)
Макрогол 400
Титанијум диоксид (Е171)
Револаде 75 мг филмом обложене таблете
Језгро таблета
Магнезијум стеарат
Манитол (Е421)
Микрокристална целулоза
Повидоне
Натријум скроб гликолат
Облога таблета
Хипромелоза
Црвени оксид гвожђа (Е172)
Црни оксид гвожђа (Е172)
Макрогол 400
Титанијум диоксид (Е171)
06.2 Некомпатибилност
Није битно.
06.3 Период важења
4 године.
06.4 Посебне мере предострожности при складиштењу
Овај лек не захтева посебне услове складиштења.
06.5 Природа непосредног паковања и садржај паковања
Филмом обложене таблете
Алуминијумски блистери (ПА / Алу / ПВЦ / Алу) у паковању које садржи 14 или 28 филмом обложених таблета и у вишеструком паковању које садржи 84 (3 паковања од 28) филм таблета.
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Неискоришћени лекови и отпад добијени из овог лека морају се одложити у складу са локалним прописима.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Новартис Еуропхарм Лимитед
Пословни парк Фримлеи
Цамберлеи ГУ16 7СР
УК
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
Револаде 12,5 мг филмом обложене таблете
ЕУ/1/10/612/010
039827100
ЕУ/1/10/612/011
039827112
ЕУ/1/10/612/012
039827124
Револаде 25 мг филмом обложене таблете
ЕУ/1/10/612/001
039827011
ЕУ/1/10/612/002
039827023
ЕУ/1/10/612/003
039827035
Револаде 50 мг филмом обложене таблете
ЕУ/1/10/612/004
039827047
ЕУ/1/10/612/005
039827050
ЕУ/1/10/612/006
039827062
Револаде 75 мг филмом обложене таблете
ЕУ/1/10/612/007
039827074
ЕУ/1/10/612/008
039827086
ЕУ/1/10/612/009
039827098
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 11. март 2010
Датум последње обнове: 15. јануар 2015
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
Новембра 2016