Активни састојци: Ленограстим
МИЕЛОСТИМ 34 милиона ИУ / мл - прах и растварач за раствор за ињекцију / инфузију
Индикације Зашто се користи Миелостим? За шта је то?
Назив вашег лека је Миелостим прах и растварач за ињекције / инфузију (у овом упутству се назива Миелостим). Миелостим садржи ленограстим, који припада групи цитокина.
Миелостим делује тако што помаже вашем телу да произведе више крвних зрнаца која се боре против инфекције.
- Ове крвне ћелије производи коштана срж.
- Миелостим стимулише коштану срж да производи више ћелија које се називају „крвне матичне ћелије“.
- Такође помаже у претварању ових незрелих крвних зрнаца у потпуно функционалне ћелије.
- Конкретно, помаже у производњи више белих крвних зрнаца која се зову неутрофили. Неутрофили су важни за борбу против инфекција.
Миелостим се користи:
Након терапије рака, ако је ниво белих крвних зрнаца пренизак ("неутропенија")
Неке терапије рака (које се називају и хемотерапије) оштећују коштану срж. Ово може смањити број ваших белих крвних зрнаца. Конкретно, "неутрофилна" бела крвна зрнца су погођена и ово стање се назива "неутропенија". То траје све док ваше тело не може да произведе више белих крвних зрнаца. Када је број неутрофила низак, лакше је доћи до инфекције. У неким случајевима могу бити веома озбиљни. Миелостим ће помоћи у смањењу времена за које су ове ћелије ниске. То чини тако што стимулише ваше тело да производи нова бела крвна зрнца.
Када требате повећати број матичних ћелија у крви („мобилизација“)
Миелостим се може користити за стимулацију коштане сржи за производњу крвних матичних ћелија. Овај процес се назива „мобилизација“. То се може догодити самостално или можда након хемотерапије. Ове крвне матичне ћелије се издвајају из ваше крви и прикупљају посебном опремом. Матичне ћелије крви могу се складиштити и поново увести у ваше тело трансфузијом.
Након трансплантације коштане сржи или крвних матичних ћелија
Ако имате трансплантацију коштане сржи или крвних матичних ћелија, прво ћете примити високу дозу хемотерапије или терапију целог тела зрачењем. Ово је за уклањање болесних ћелија. Након тога, трансплантацијом коштане сржи или крвних матичних ћелија врши се трансфузија крви. Потребно је неко време да ваша нова коштана срж почне да производи нове крвне ћелије (укључујући бела крвна зрнца). Миелостим ће помоћи вашем телу да убрза стварање нових белих крвних зрнаца.
Када жели да донира своје крвне матичне ћелије
Миелостим се такође може користити код здравих давалаца. Код ових људи стимулише коштану срж да производи додатне крвне матичне ћелије. Овај процес се назива мобилизација - види горе.
Ови здрави даваоци ће тада моћи даровати своје крвне матичне ћелије онима којима је то потребно.
Миелостим се може давати одраслима, адолесцентима и деци старијој од 2 године.
Контраиндикације Када се Миелостим не сме користити
Немојте узимати овај лек и обавестите свог лекара
- Ако сте алергични (преосетљиви) на ленограстим или неки други састојак лека Миелостим (наведен у одељку 6 испод). Симптоми алергијске реакције укључују: црвенило коже, проблеме са гутањем или дисањем, отицање усана, лица, грла и језика
- Ако имате стање које се зове "фенилкетонурија"
- Ако имате врсту рака која се назива „мијелоидни карцином“. Међутим, ако вам је недавно дијагностикована „акутна мијелоична леукемија“, у одређеним случајевима можете узети Миелостим ако сте старији од 55 година.
- Ако ћете истог дана имати хемотерапију рака.
Немојте узимати овај лек ако се било који од горе наведених услова односи на вас. Ако нисте сигурни, пре него што примите лек Миелостим, обратите се свом лекару или фармацеуту.
Предострожности при употреби Шта треба да знате пре него што узмете лек Миелостим
Пре него што узмете овај лек, обратите се свом лекару или фармацеуту ако:
- ако сте у прошлости имали неке болести, посебно алергије, инфекције, проблеме са бубрезима или јетром.
- болујете од анемије српастих ћелија или су носиоци српастих ћелија, јер граноцит може изазвати српасту ћелијску кризу
Ако нисте сигурни да ли је то случај, разговарајте са својим лекаром или фармацеутом пре употребе лека Миелостим.
Деца и адолесценти
Пре него што узмете овај лек, обратите се свом лекару ако:
- Ако имате врсту рака која се назива „акутна лимфоцитна леукемија“ и ако сте млађи од 18 година.
Интеракције Који лекови или храна могу променити ефекат лека Миелостим
Обавестите свог лекара или фармацеута ако узимате или сте недавно узимали неке друге лекове, чак и оне без рецепта, укључујући и лекове на биљној бази.
Ако желите да донирате своје крвне матичне ћелије и лечите се антикоагулансом (као што је варфарин или хепарин), уверите се да је то ваш лекар свестан пре почетка лечења Миелостимом. Реците му и ако имате других проблема са згрушавањем крви.
Ако примате хемотерапију против рака, немојте користити Миелостим 24 сата пре почетка лечења и до 24 сата након завршетка терапије.
Упозорења Важно је знати да:
Трудноћа и дојење
Миелостим није тестиран код трудница и дојиља. Немојте узимати овај лек ако сте трудни, ако бисте могли затруднети или ако дојите, осим ако вам лекар не каже да је то потребно.
Питајте свог лекара или фармацеута за савет пре него што узмете било који лек ако мислите да сте трудни.
Вожња и управљање машинама
Ефекти Миелостима на способност управљања возилима, рада са машинама или механичким алатима нису познати. Сачекајте да сазнате какве ефекте Миелостим може имати на вас пре вожње, коришћења машина или механичких алата.
Важне информације о неким састојцима лека Миелостим
Миелостим садржи фенилаланин. Ова супстанца може бити штетна за вас ако имате болест која се зове "фенилкетонурија" (погледајте одељак изнад "Немојте узимати овај лек").
Доза, начин и време примене Како се користи Миелостим: Дозирање
Миелостим треба примењивати под надзором у специјализованом онколошком или хематолошком центру. Обично администрацију врши лекар, медицинска сестра или фармацеут. Даје се ињекцијом или инфузијом.
Међутим, неки пацијенти се могу научити како сами да убризгавају ињекцију. Ако имате питања о начину примене овог лека, питајте свог лекара, медицинску сестру или фармацеута.
Колико Миелостим узети
Ако нисте сигурни зашто вам даје Миелостим или имате било каквих питања о томе колико Миелостима треба да узмете, питајте свог лекара, медицинску сестру или фармацеута.
Након трансплантације коштане сржи, хемотерапије или за мобилизацију крвних матичних ћелија након хемотерапије
- Ваш лекар ће одлучити о дози која ће вам дати на основу површине вашег тела. Ово се израчунава помоћу ваше тежине и висине. Она се "мери у" квадратним метрима "који ће бити означени као м2.
- Уобичајена доза Миелостима је 19,2 МИУ (150 микрограма) дневно за сваки м2 површине тела. Доза код деце старије од 2 године и адолесцената је иста као код одраслих.
- Ваш лекар ће одлучити колико дана треба да узимате лек Миелостим. Администрација може трајати највише 28 дана.
- Када се Миелостим даје за мобилизацију матичних ћелија крви након хемотерапије, ваш лекар ће вам рећи када ће се обавити прикупљање крвних матичних ћелија.
За мобилизацију крвних матичних ћелија само са Миелостимом
- Ваш лекар ће одредити колико лекова морате да узмете на основу своје тежине.
- Уобичајена доза Миелостима је 1,28 МИУ (10 микрограма) дневно за сваки кг телесне тежине. Доза код деце старије од 2 године и адолесцената је иста као код одраслих.
- Миелостим ће вам се давати ињекцијом под кожу 4-6 дана.
- Прикупљање ваших крвних матичних ћелија ће се обавити 5-7 дана касније.
МИЕЛОСТИМ 34 милиона ИУ / мл може се користити код пацијената са површином тела до 1,8 м2.
Ако сте заборавили да узмете лек Миелостим
Немојте узети двоструку дозу да бисте надокнадили ињекцију коју сте заборавили. Увек питајте свог лекара који ће вам рећи шта да радите.
Крвни тестови
Морате бити под лекарским надзором док узимате овај лек. Имаћете редовне тестове крви. Ово ће проверити нивое различитих крвних зрнаца (неутрофила, других белих крвних зрнаца, црвених крвних зрнаца, тромбоцита).
Било који други тестови крви које су прописали други лекари могу се променити док се лечите леком Миелостим. Ако радите тест крви, важно је да кажете свом лекару да узимате Миелостим. Може се повећати ваш број белих крвних зрнаца, број тромбоцита и ниво ензима. Ове промене се обично побољшавају након престанка узимања Миелостима. Ако вам је потребна анализа крви, важно је да кажете свом лекару да узимате Миелостим.
Ако имате додатних питања о употреби овог производа, обратите се свом лекару или фармацеуту.
Предозирање Шта треба учинити ако сте узели превише лека Миелостим
Ако вам овај лек дају лекар, медицинска сестра или фармацеут, мало је вероватно да ће вам дати превише. Они ће пратити ваш напредак и проверити дозу. Увек тражите објашњење ако нисте сигурни у вези са дозом лека коју добијате.
Ако сте сами узели превише лека Миелостим, обавестите свог лекара или одмах идите у болницу. Понесите паковање лека са собом како би ваш лекар знао шта сте узели. Посебно озбиљни нежељени ефекти могу бити ако сте узели превише лека. Највероватнија болест коју има може бити бол у мишићима и костима.
Нежељени ефекти Који су нежељени ефекти Миелостима
Као и сви лекови, Миелостим може изазвати нежељена дејства, мада се она не морају јавити код свих.
Престаните са узимањем Миелостима и одмах обавестите свог лекара ако:
- Имате бол у левој горњој левој страни абдомена или левом рамену. То могу бити симптоми повећања величине слезине. Ово је уобичајен нежељени ефекат, али врло ретко може изазвати руптуру слезине.
- Има алергијску реакцију. Симптоми укључују црвенило коже, проблеме са гутањем или дисањем, отицање усана, лица, грла или језика. Ово је веома ретка нуспојава.
- Имате веома озбиљну алергијску реакцију која се назива „анафилактички шок“. Симптоми укључују осећај несвестице, слабости, отежано дисање или отицање лица. Ово је веома ретка нуспојава.
- Имате проблема са дисањем. Симптоми укључују кашаљ, грозницу или недостатак даха. Ово је ретка нуспојава.
Обавестите свог лекара или фармацеута што је пре могуће ако доживите неки од следећих нежељених ефеката:
- Реакција на месту убризгавања. Ово је уобичајен нежељени ефекат.
- Проблеми са кожом, попут љубичастих наслага на рукама, ногама, а понекад и на лицу или врату са грозницом (симптоми Свеетовог синдрома). Црвени пликови се такође могу појавити са грозницом и главобољом (симптоми Лиелл -овог синдрома). Остали кожни проблеми могу бити задебљане црвене модрице на ногама или чиреви на тијелу с грозницом и боловима у зглобовима. Ово су веома ретки нежељени ефекти.
Остали нежељени ефекти укључују:
- Бол у костима и мишићима и главобоља. Ово је уобичајен нежељени ефекат. Ако се то догоди, бол се може контролирати нормалним средствима против болова.
Донатори крвних матичних ћелија
Као и сваки лек, Миелостим може изазвати нежељена дејства, мада се она не јављају код свих. Неки нежељени ефекти могу се појавити одмах, другима је потребно неколико дана да се појаве.
Одмах обавестите свог лекара ако:
- Имате бол у горњем левом делу трбуха или левом рамену. То могу бити симптоми повећања величине слезине, уобичајен нежељени ефекат који се назива спленомегалија. Ово стање врло ретко може изазвати руптуру слезине.
- Имате знакове алергијске реакције, чак и након прве примене лека Миелостим. Симптоми укључују кожни осип, проблеме са гутањем или дисањем, отицање усана, лица, грла или језика. Ово је веома ретка нуспојава.
- Имате веома ретку и веома озбиљну алергијску реакцију која се назива „анафилактички шок“. Ово је изненадна, по живот опасна реакција. Симптоми укључују осећај несвестице, слабости, отежано дисање или отицање лица.
- Има кашаљ, грозницу и отежано дисање (диспнеја). То могу бити симптоми акутног респираторног дистресног синдрома (АРДС) који је врло ретка нуспојава.
- Осећате било које или комбинацију следећих нежељених ефеката: едем или оток, који могу бити повезани са смањењем мокрења, отежаним дисањем, надутошћу у стомаку и осећајем ситости, и општим осећајем умора. Ови симптоми се обично брзо развијају. То могу бити симптоми неуобичајеног стања (могу се јавити у до 1 на 100 људи) под називом „синдром капиларног цурења“, који узрокује цурење крви из малих крвних судова у тијело и који захтијева хитну медицинску помоћ.
Реците свом лекару ако доживите неки од следећих врло честих нежељених ефеката:
- Можда ћете осећати бол, бол у костима и леђима, главобољу, грозницу и / или осећати мучнину (мучнина);
- Можда ћете имати привремене промене вредности крвних тестова, укључујући и оне које се односе на функцију јетре, али оне генерално не захтевају додатне мере предострожности и имају тенденцију да се нормализују након престанка узимања лека.
- Можда ћете се осећати уморно након давања крвних матичних ћелија. То је због пада броја црвених крвних зрнаца. Можда ћете такође имати смањење броја тромбоцита што може узроковати крварење или модрице лакше него иначе.
Придржавање упутстава садржаних у упутству за употребу смањује ризик од нежељених ефеката.
Пријављивање нежељених ефеката
Ако приметите било које нежељено дејство, обратите се свом лекару или фармацеуту.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нежељена дејства директно путем националног система за пријављивање на: ввв.агензиафармацо.гов.ит/ит/респонсабили.Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте Миелостим ван домашаја и погледа деце.
Немојте користити било који део праха и растварача Миелостим за комплет раствора након истека рока употребе (ЕКСП).
Рок употребе Миелостим праха наведен је на спољној кутији и на етикети сваке бочице Миелостима.
Датум истека растварача (воде за ињекције) наведен је на етикети сваке ампуле воде за ињекције, на етикети напуњеног шприца водом и на папиру у блистеру. Датум истека се односи на последњи дан наведеног месеца.
Не чувати на температури изнад 30 ° Ц. Немојте замрзавати.
Препоручује се употреба производа одмах након реконституције или разблаживања. Ако је потребно, реконституисани или разблажени раствор можете чувати до 24 сата на температури од 2 ° Ц до 8 ° Ц (у фрижидеру).
Лекове не треба одлагати у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Остале информације
-
Шта Миелостим садржи
- Активна супстанца је ленограстим (рХуГ-ЦСФ) 33,6 милиона међународних јединица (еквивалентно 263 микрограма) по мл након реконституције.
- Остале помоћне супстанце садржане у праху су аргинин, фенилаланин, метионин, манитол (Е421), полисорбат 20 и разблажена хлороводонична киселина.
- Помоћне супстанце за које је познато да имају признато „дејство или дејство“: фенилаланин.
- Растварач који се користи за реконституисање раствора је вода за ињекције
Како Миелостим изгледа и садржај паковања
Миелостим је представљен као прах и растварач за раствор за ињекцију / инфузију.
Прашак у бочици + 1 мл растварача у бочици.
МИЕЛОСТИМ је доступан у паковањима од 1 или 5 јединица.
Не могу се на тржиште ставити све величине паковања.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
МИЕЛОСТИМ 34 МИЛИОН ИУ / МЛ, ПРАХ И РАСПОРАВАЧ ЗА РЈЕШЕЊЕ ЗА УБРИЗГАВАЊЕ / ИНФУЗИЈУ
02.0 КВАЛИТАТИВНИ И КОЛИЧИНСКИ САСТАВ
Ленограстим * (рХуГ-ЦСФ) 33,6 милиона међународних јединица (еквивалентно 263 мцг) по мл након реконституције
* произведено рекомбинантном ДНК технологијом у ћелијама јајника кинеског хрчка (ЦХО).
Помоћне супстанце за које је познато да имају признато дејство или деловање: фенилаланин За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Прашак и растварач за раствор за ињекцију / инфузију.
- Бели прах
- Растварач: бистри, безбојни раствор
Растварач: бистри, безбојни раствор
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Миелостим је индициран код одраслих, адолесцената и деце старијих од 2 године за:
Смањење трајања неутропеније код пацијената (са немијелоидним малигнитетом) који су подвргнути мијелоаблативној терапији, праћено трансплантацијом коштане сржи (БМТ) и сматра се повећаним ризиком од продужене тешке неутропеније.
Смањење трајања тешке неутропеније и повезаних компликација код пацијената који су подвргнути режимима цитотоксичне хемотерапије повезаних са значајном учесталошћу фебрилне неутропеније.
Мобилизација матичних ћелија периферне крви (ПБПЦ) код пацијената, а такође и код здравих давалаца.
04.2 Дозирање и начин примене
Терапију треба спроводити само у специјализованом онколошком и / или хематолошком центру. МИЕЛОСТИМ се може применити поткожном ињекцијом или интравенозном инфузијом. Упутства за посебно руковање или припрему производа дата су у одељку 6.6.
Препоручена доза Миелостима је 19,2 МИУ (150 мцг) по м 2 дневно, што је терапеутски еквивалентно 0,64 МИУ (5 мцг) по кг дневно за: трансплантацију периферних матичних ћелија или коштане сржи, хемотерапију конвенционалном цитотоксичношћу, мобилизацију ПБПЦ после хемотерапије.
Миелостим 34 милиона ИУ / мл може се користити код пацијената са површином тела до 1,8 м2.
За мобилизацију ПБПЦ само са Миелостимом, препоручена доза је 1,28 МИУ (10 мцг) по кг дневно.
Одрасли:
Код трансплантације периферних матичних ћелија или коштане сржи
Миелостим треба примењивати дневно у препорученој дози од 19,2 МИУ (150 микрограма) по м2 дневно у облику интравенске инфузије, у трајању од 30 минута, разблажене у изотоничном раствору соли или као поткожна ињекција. Прва доза се не сме примењивати у 24. сата након имплантације коштане сржи. Давање треба наставити све док се очекивана минимална концентрација неутрофила (надир) не прекорачи и док се број неутрофила не врати на стабилне границе компатибилне са прекидом лечења, до максимално, ако је потребно, од 28 узастопних дана терапије.
Очекује се да ће се нормалан ниво неутрофила постићи у року од 14 дана од трансплантације коштане сржи код 50% пацијената.
У току је конвенционална цитотоксична хемотерапија
Миелостим у препорученој дози од 19,2 МИУ (150 микрограма) по м2 дневно треба примењивати дневно поткожном ињекцијом.Прву дозу не треба применити у року од 24 сата након цитотоксичне хемотерапије (видети одељке 4.4 и 4.5).
Свакодневну примену лека Миелостим треба наставити све док се не пређе очекивани надир и број неутрофила достигне стабилне вредности компатибилне са престанком лечења, до максимално, ако је потребно, од 28 узастопних дана терапије.
Иако се у прва два дана терапије може догодити пролазно повећање неутрофила, лијечење Миелостимом не треба прекидати јер опћенито постоји ранији почетак надира и бржи повратак у нормалу уз наставак лијечења.
У мобилизацији матичних ћелија периферне крви (ПБПЦ)
Након хемотерапије, Миелостим треба примењивати дневно у препорученој дози од 19,2 МИУ (150 микрограма) по м2 дневно супкутаном ињекцијом у року од 1 - 5 дана након завршетка хемотерапије, у складу са режимом хемотерапије датим за мобилизацију. Миелостим треба примењивати до последње леукаферезе.
Леукаферезу треба извести у периоду након надира, када расте број белих крвних зрнаца, или након одређивања садржаја ЦД34 + ћелија у крви потврђеном методом. Код пацијената који нису примили интензивну хемотерапију, једна леукафереза је често довољна да се постигне минимално прихватљиво сакупљање (≥ 2,0 к 106 ЦД34 + ћелија по кг).
У мобилизацији ПБПЦ-а уз употребу само Миелостима, Миелостим треба примењивати дневно у препорученој дози од 1,28 МИУ (10 микрограма) по кг дневно као поткожна ињекција током 4-6 дана. Леукаферезу треба извести између 5. и 7. дана. Код пацијената који нису примили интензивну хемотерапију, једна леукафереза је често довољна да се постигне минимално прихватљиво сакупљање (≥ 2,0 к 106 ЦД34 + ћелија по кг).
Код здравих давалаца, дневна доза од 10 мцг / кг која се примењује поткожно током 5-6 дана омогућава прикупљање ћелија ЦД34 + 3 к 106 / кг телесне тежине, са једном леукаферезом у 83% испитаника и са две леукаферезе у 97% предмета.
У „старешини
Мали број пацијената до 70 година старости укључен је у клиничка испитивања лека Миелостим, али нису спроведена циљана испитивања на старијим особама, па се не могу препоручити посебне дозе.
У детету
У смањењу трајања неутропеније након мијелоаблативне терапије праћене БМТ -ом или након цитотоксичне хемотерапије, доза код деце старије од 2 године и адолесцената је иста као код одраслих.
Доступни су врло ограничени подаци о мобилизацији прогениторних ћелија периферне крви у дозама за одрасле.
Безбедност и ефикасност лека Миелостим код деце млађе од 2 године нису утврђене МИЕЛОСТИМ 34 милиона ИУ / мл може се користити код пацијената са површином тела до 1,8 м2.
04.3 Контраиндикације
Миелостим се не сме давати пацијентима са познатом преосетљивошћу на ленограстим или на било коју помоћну супстанцу.
Миелостим се не сме користити за повећање интензитета дозе цитотоксичне хемотерапије изван утврђеног дозирања и уобичајених режима дозирања, јер Миелостим може смањити мијелотоксичност, али не и укупну токсичност цитотоксичних лекова.
Не сме се примењивати истовремено са цитотоксичном хемотерапијом.
Не сме се давати пацијентима
- са мијелоидном неоплазијом осим акутне мијелоичне леукемије "де ново'
- са акутном мијелоичном леукемијом "де ново"млађи од 55 година и / или са акутном мијелоичном леукемијом"де ново"са повољном цитогенетиком, односно т (8; 21), т (15; 17) и инв.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Раст малигних ћелија
Фактори стимулације колонија гранулоцита могу ин витро стимулирати раст мијелоидних ћелија; слични ефекти су примећени, поново ин витро, у неким немијелоидним ћелијама.
Безбедност и ефикасност примене Миелостима код пацијената са мијелодисплазијом или секундарном акутном мијелоичном леукемијом, или хроничном мијелоичном леукемијом нису утврђени. Због тога се не треба користити у овим индикацијама. Посебну пажњу треба посветити разликовању дијагнозе бластне трансформације хронична мијелоична леукемија узрокована акутном мијелоичном леукемијом. Клиничке студије нису утврдиле да ли Миелостим може утицати на прогресију мијелодиспластичног синдрома у акутну мијелоичну леукемију. Треба бити посебно опрезан при његовој употреби у свим пре-неопластичним мијелоидним стањима. С обзиром на то да неки карциноми са не- специфичне карактеристике могу у изузетним случајевима изразити Г-ЦСФ рецептор, треба бити посебно опрезан у случају неочекиваних рецидива тумора уочених заједно са терапијом рХуГ-ЦСФ.
Код деце са СВИМ
Забележен је повећан ризик од секундарне мијелоичне леукемије или мијелодиспластичног синдрома повезаног са ЦСФ -ом код деце са АЛЛ -ом. Сличан ризик пронађен је у систематском прегледу 25 рандомизованих контролисаних испитивања у којима је учествовало 12.804 одраслих пацијената са солидним туморима или лимфомима. Овај ризик, међутим, није имао негативан утицај на дугорочне исходе код одраслих испитаника, па се Миелостим 34 милиона ИУ / мл треба давати само деци, а нарочито онима са повољном дугорочном прогнозом, само након пажљиве процене. краткорочне користи, засноване на дугорочним ризицима.
Леукоцитоза
Број белих крвних зрнаца већи од 50к109 / л није примећен ни код једног од 174 пацијената укључених у клиничке студије и лечених са 5 мцг / кг / дан (0,64 милиона јединица / кг / дан) након трансплантације коштане сржи. Број белих крвних зрнаца једнак или већи од 70к10 9 / л примећен је код мање од 5% пацијената који су подвргнути цитотоксичној хемотерапији лечени Миелостимом у дози од 5 мцг / кг / дан (0,64 милиона јединица / кг / дан). Нису пријављени никакви нежељени догађаји који се директно приписују овом степену леукоцитозе. Због потенцијалних ризика повезаних са тешком леукоцитозом, број белих крвних зрнаца треба и даље вршити у редовним интервалима током терапије Миелостимом. Ако број леукоцита пређе 50к10 9 / л након очекиваног надила, Миелостим треба одмах прекинути.
Током мобилизације ПБПЦ, Миелостим треба прекинути ако се број белих крвних зрнаца повећа на> 70 к 109 / Л.
Нежељени догађаји у плућима
Након примене Г-ЦСФ, забележени су ретки плућни нежељени догађаји (> 0,01% и интерстицијална пнеумонија.
Пацијенти са недавном историјом плућних инфилтрата или упале плућа могу бити под високим ризиком.
Појава плућних симптома или знакова као што су кашаљ, грозница и диспнеја, заједно са радиолошким знацима плућних инфилтрата и погоршањем функције плућа, могу бити прелиминарни знаци синдрома акутног респираторног дистреса (АРДС).
Лечење Миелостимом треба одмах прекинути и дати одговарајући третман.
Код трансплантације периферних матичних ћелија или коштане сржи
Посебну пажњу треба посветити опоравку тромбоцита, јер је у двоструко слепим плацебом контролисаним клиничким испитивањима средњи број тромбоцита био мањи код пацијената лечених Миелостимом него код оних који су примали плацебо.
Ефекат Миелостима на учесталост и тежину акутне и хроничне болести трансплантата против домаћина још није добро утврђен.
У конвенционалној цитотоксичној хемотерапији
Не препоручује се употреба Миелостима у периоду од 24 сата пре до 24 сата након завршетка хемотерапије (видети одељак 4.5).
Није утврђена безбедност употребе Миелостима са антинеопластичним агенсима које карактерише кумулативна мијелотоксичност или превладавајућа тромбоцити (нитросуреа, митомицин).
Примена Миелостима могла би повећати токсичност ових агенаса, посебно према тромбоцитима.
Ризици повезани са повећањем дозе хемотерапије
Безбедност и ефикасност лека Миелостим још нису потврђене током интензивирања хемотерапије. Не треба га користити за смањивање интервала између курсева хемотерапије испод утврђених граница и / или за повећање дозе лекова за хемотерапију. Не-мијелоично оптерећење ћелија је био ограничавајући фактор у студијама интензивирања хемотерапије фазе ИИ са Миелостимом.
Посебне мере предострожности при мобилизацији матичних ћелија периферне крви
Избор методе мобилизације
Клиничке студије спроведене на истој популацији пацијената показале су да је, како је верификовано у истој лабораторији, мобилизација ПБПЦ била већа када се Миелостим користио након хемотерапије него када се користио сам. Међутим, избор између две методе мобилизације треба направити у односу на укупне циљеве лечења за сваког појединачног пацијента.
Претходно излагање радиотерапији и / или цитотоксичним агенсима
Пацијенти који су били подвргнути интензивној мијелосупресивној терапији и / или радиотерапији можда неће показати довољну мобилизацију ПБПЦ -а за постизање минимално прихватљивог прикупљања (≥ 2,0 к 106 ЦД34 + / кг) и стога адекватан хематолошки опоравак.
Програм трансплантације ПБПЦ треба дефинисати на почетку лечења пацијента е први при примени хемотерапије у високим дозама, посебну пажњу треба обратити на број мобилисаних ПБПЦ. Ако је жетва ниска, трансплантацију ПБПЦ -а треба заменити другим облицима лечења.
Процена количине прикупљених матичних ћелија
Посебну пажњу треба обратити на методу квантификације прикупљених прогенитор ћелија, будући да се резултати анализе ЦД34 + ћелија добијених проточном цитометријом разликују од лабораторије до лабораторије.
Минимална колекција ЦД34 + ћелија није добро дефинисана. Препорука за минимално сакупљање ЦД34 + ≥ 2,0 к 106 ћелија / кг заснива се на литературним подацима како би се постигла одговарајућа хематолошка реконституција. Колекције ЦД34 + ≥ 2,0 к 106 ћелија / кг повезане су са бржим опоравком, укључујући и тромбоците, док мање сакупљање доводи до споријег опоравка.
Код здравих давалаца
Мобилизација матичних ћелија периферне крви, поступак који не доводи до директних користи за здраву популацију, мора се узети у обзир само у границама које прописује закон, у складу са локалним прописима за донације коштане сржи, када је примењиво.
Ефикасност и безбедност лека Миелостим нису процењивани код донатора старијих од 60 година, па се овај поступак не препоручује за такве субјекте.На основу неких локалних прописа и због недостатка посебних студија, они не би требало да буду узети у обзир као малолетни даваоци. .
Поступак мобилизације ПБПЦ треба размотрити за даваоце који испуњавају клиничке и лабораторијске критеријуме подобности за давање коштане сржи, посебно с обзиром на нормалне хематолошке вредности.
Леукоцитоза (ВБЦ ≥ 50 к 109 / Л) је примећена код 24% испитаних субјеката. Тромбоцитопенија (тромбоцити
Због тога се леукафереза не сме изводити код давалаца лечених антикоагулансима или са познатим хемостатским оштећењима.Ако је потребно више од једне леукаферезе, посебну пажњу треба посветити даваоцима са тромбоцитима.
Ако је могуће, не треба уметати централни венски катетер, узимајући у обзир лакоћу венског приступа при избору давалаца.
Подаци о дугорочном праћењу доступни су у малом броју испитаника. Нису пријављене дугорочне последице до шест година. Међутим, постоји ризик од развоја малигног мијелоидног клона. Због тога се препоручује да центри за аферезу воде евиденцију и систематски прате донације матичних ћелија.
Током постмаркетиншког искуства, код здравих давалаца пријављени су плућни нежељени догађаји (хемоптиза, плућна крварења, плућни инфилтрати, диспнеја и хипоксија). У случају сумње или потврде плућних нежељених догађаја, треба размотрити прекид лека. Лечење леком Миелостим и треба пружити одговарајућу медицинску негу.
Код прималаца алогенских периферних матичних ћелија мобилисаних са Миелостимом
Алогена трансплантација матичних ћелија може бити повезана са повећаним ризиком од хроничне ГВХ (графт версус Хост), а дугорочни подаци о функцији трансплантата су оскудни.
Друге посебне мере предострожности
Нема довољно података о безбедности и ефикасности лека Миелостим код пацијената са тешким оштећењем бубрега или јетре.
Код пацијената са знатно смањеним мијелоидним прогениторским ћелијама, на пример због претходног интензивног излагања радио / хемотерапији, неутрофилни одговор је понекад смањен, а безбедност Миелостима није утврђена.
Уобичајени, али генерално асимптоматски случајеви спленомегалије и врло ретки случајеви руптуре слезине су примећени и код здравих давалаца и код пацијената након примене фактора стимулације колоније гранулоцита (Г-ЦСФ). Због тога се величина слезине мора пажљиво пратити (клинички прегледи, ултразвук). Ако се пријави бол у горњем левом делу трбуха или бол у врху рамена, треба посумњати на дијагнозу руптуре слезине.
Синдром капиларног цурења пријављен је након примене Г-ЦСФ, а карактерише га хипотензија, хипоалбуминемија, едем и хемоконцентрација. Код пацијената код којих се развије синдром капиларног цурења, примену Ленограстима треба прекинути, такве пацијенте треба пажљиво пратити и започети одговарајуће симптоматско лечење, што може укључивати потребу за интензивном негом (видети одељак 4.8).
Код пацијената са српастом ћелијском болешћу и код пацијената са српастоцелијским својствима, употреба ленограстима може бити повезана са српавим нападима. Због тога Миелостим треба прописати са опрезом код пацијената са српастом ћелијском болешћу или код пацијената са српастоцелијским особинама МИЕЛОСТИМ садржи фенилаланин који може бити штетно за људе са фенилкетонуријом.
04.5 Интеракције са другим лековима и други облици интеракција
С обзиром на осетљивост мијелоидних ћелија које се брзо множе на цитотоксичну хемотерапију, не препоручује се употреба Миелостима у периоду од 24 сата пре до 24 сата након завршетка хемотерапије (видети одељак 4.4). Могуће интеракције са другим факторима. Путеви раста и цитокини тек треба да се проуче посебним клиничким истраживањима.
04.6 Трудноћа и дојење
Трудноћа
Нема одговарајућих података о употреби ленограстима у трудница Студије на животињама су показале репродуктивну токсичност (видети одељак 5.3). Потенцијални ризик код људи је непознат.
Миелостим се не сме користити током трудноће, осим ако је неопходно.
Време храњења
Није познато да ли се ленограстим излучује у мајчино млеко. Екскреција ленограстима у млеко није проучавана код животиња.
Дојење треба прекинути током терапије леком Миелостим.
04.7 Утицај на способност управљања возилима и машинама
Нису спроведена испитивања о способности управљања возилима и рада са машинама.
04.8 Нежељени ефекти
Безбедносни профил је сличан код деце, адолесцената и одраслих.
Код трансплантације периферних матичних ћелија или коштане сржи
У двоструко слепим плацебом контролисаним клиничким испитивањима, просечан број тромбоцита био је мањи код пацијената лечених Миелостимом него код пацијената лечених плацебом, без повећања учесталости нежељених реакција хеморагијског типа и средњег броја дана између трансплантације коштане сржи и последња трансфузија тромбоцита била је слична у две групе (видети одељак 4.4).
У трансплантацији периферних матичних ћелија или коштане сржи и у неутропенији хемотерапије
Најчешћи нежељени догађаји пријављени у клиничким испитивањима (15%) били су исти код пацијената лечених и Миелостим -ом и плацебом.
Нежељени догађаји били су они који су се генерално јављали током режима кондиционирања и током хемотерапије код пацијената са раком.
Најчешће пријављени нежељени догађаји били су орална инфекција / упала, сепса и инфекције, грозница, дијареја, бол у трбуху, повраћање, мучнина, осип, алопеција и главобоља.
У мобилизацији прогениторних ћелија периферне крви (ПБПЦ) код здравих давалаца
Најчешће пријављени нежељени ефекти су пролазни, благи до умерени: бол, болови у костима, болови у леђима, астенија, грозница, главобоља и мучнина, повећане вредности АЛАТ / АСАТ, алкалне фосфатазе и ЛДХ.
Тромбоцитопенија повезана с аферезом и леукоцитоза примећене су код 42%, односно 24% испитаника.
Пријављени су чести, али генерално асимптоматски случајеви спленомегалије и врло ретки случајеви пуцања слезине.
Забележене су ретке нежељене реакције на плућа, попут диспнеје, хипоксије или хемоптизије, укључујући, врло ретко, синдром акутног респираторног дистреса (АРДС) (видети одељак 4.4).
Врло ретко су пријављиване алергијске реакције, укључујући анафилаксију, које су се јавиле након прве поткожне примене ленограстима.
Постмаркетиншки надзор над животно опасним нежељеним реакцијама:
Синдром капиларног цурења, који може бити опасан по живот ако се лечење одложи, у постмаркетиншком надзору пријављен је као неуобичајен догађај (≥ 1/1000 до
Учесталост нежељених реакција из клиничких испитивања и из постмаркетиншких података.
Врло често (≥10%); честа (≥1 / 100 и непозната (не може се проценити из доступних података).
1 / Ризик од бола је повећан код људи са високим бројем белих крвних зрнаца, посебно ако су бела крвна зрнца ≥ 50к109 / л
2 / Примећено је пролазно повећање АСАТ -а и / или АЛАТ -а.У многим случајевима абнормалности функције јетре су се побољшале након престанка узимања ленограстима.
3 / Неки пријављени респираторни случајеви изазвали су респираторну инсуфицијенцију или синдром акутног респираторног дистреса (АДРС) који може бити фаталан.
4 / Свеетов синдром, нодосум еритема и гангренозна пиодерма описани су углавном код пацијената са хематолошким малигнитетима, стање за које се зна да је повезано са неутрофилном дерматозом, али и код пацијената са неутропенијом повезаном са туморима.
5 / Руптура слезине је пријављена и код здравих добровољаца и код пацијената који су примали Г-ЦСФ (видети одељак 4.4).
6 / Случајеви синдрома капиларног цурења забележени су у постмаркетиншком надзору (видети одељак 4.4).
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика лека. Од здравствених радника се тражи да пријаве све сумње на нежељене реакције путем националног система за пријављивање. "Адреса: ввв .агензиафармацо.гов.ит/ит/респонсабили.
04.9 Предозирање
Ефекти предозирања Миелостимом нису идентификовани (видети одељак 5.3). Престанак терапије Миелостимом генерално резултира смањењем циркулишућих неутрофила за 1-2% у року од 1-2 дана, враћајући се на нормалне нивое за 1-7 дана. Број белих крвних зрнаца од приближно 50к109 / л описан је код једног од три пацијента који су примили највећу дозу Миелостима, једнаку 40 микрограма / кг / дан (5,12 милиона јединица / кг / дан) 5. дана лечења.
Код људи, дозе до 40 мцг / кг / дан нису биле повезане са токсичним нуспојавама, осим мишићно -коштаног бола.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: цитокини.
АТЦ ознака Л03АА10.
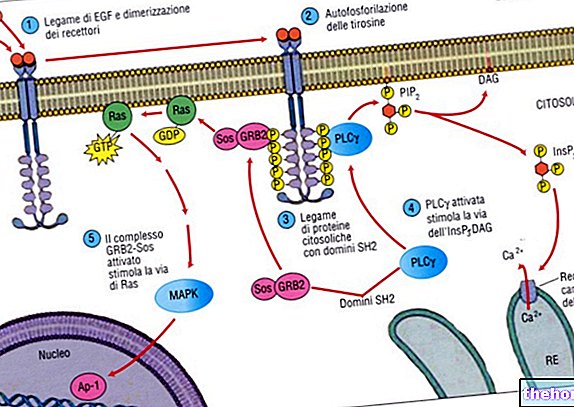
Ленограстим (рХуГ-ЦСФ) припада групи цитокина, протеина који су биолошки активни у регулисању ћелијске диференцијације и раста.
рХуГ-ЦСФ је фактор који стимулише ћелијске прекурсоре неутрофила што је показано повећањем броја ћелија ЦФУ-С и ЦФУ-ГМ у периферној крви.
Миелостим изазива значајно повећање броја неутрофила у периферној крви у року од 24 сата.
Повећање броја неутрофила зависи од дозе у распону од 1 до 10 мцг / кг / дан.У препорученој дози, поновљене примене изазивају повећање одговора неутрофила.
Утврђено је да неутрофили настали као одговор на Миелостим функционишу нормално у погледу фагоцитозе и хемотаксије.
Као и други хематопоетски фактори раста, Г-ЦСФ је показао ин витро стимулативна својства људских ендотелних ћелија.
Употреба Миелостима код пацијената на трансплантацији коштане сржи или лечених цитотоксичним хемотерапијама доводи до значајног смањења трајања неутропеније и повезаних компликација.
Употреба Миелостима, самостално или након хемотерапије, мобилише хематопоетске матичне ћелије у периферну крв. Ове аутологне ћелије матичних ћелија периферне крви (ПБПЦ) могу се прикупити и поново инфузирати након високих доза цитотоксичне хемотерапије, било као замена или као додатак коштаној сржи. пресадити.
Показано је да реинфундирани ПБПЦ, добијени након мобилизације са Миелостимом, могу да реконструишу хематопоезу и смање време потребно за трансплантацију, што је резултирало знатним смањењем броја дана зависности од трансфузије тромбоцита у поређењу са аутологном трансплантацијом коштане сржи. .
Анализом података из 3 двоструко слепе, плацебом контролисане студије на 861 пацијента (н = 411 55 година), показан је повољан однос користи и ризика за примену ленограстима код пацијената старијих од 55 година који су били на конвенционалној хемотерапији за акутну мијелоичну леукемију "де ново", са изузетком акутне мијелоичне леукемије са повољном цитогенетиком, тј. т (8; 21), т (15; 17) и инв .. Корист изазвана ленограстимом у подгрупи пацијената старијих од 55 година укључује" убрзање опоравак вредности неутрофила, повећање процента пацијената без епизода инфекције, смањење трајања инфекције, трајање хоспитализације, трајање ИВ антибиотске терапије. Међутим, ови позитивни резултати нису повезани са смањењем учесталости тешких или фаталних инфекција, нити са смањењем морталитета повезаног са инфекцијом.
Подаци из двоструко слепе плацебо контролисане студије на 446 пацијената са акутном мијелоичном леукемијом "де ново"показало је да је у подгрупи од 99 пацијената са повољном цитогенетиком преживљавање без догађаја значајно ниже у групи ленограстима него у групи која је примала плацебо; укупан нижи тренд према преживљавању такође је примећен у групи ленограстима него у подацима подгрупе. неповољна цитогенетика.
05.2 Фармакокинетичка својства
Фармакокинетика мијелостима зависи од дозе и времена.
Након поновљене примене (и.в., с.ц.), максималне концентрације у серуму (непосредно након интравенске инфузије или након поткожне ињекције) пропорционалне су убризганој дози.
Поновљене дозе Миелостима примењене било којим путем не показују ефекте акумулације лека. У препорученој дози, апсолутна биорасположивост Миелостима је 30%. Привидни волумен дистрибуције (Вд) је приближно 1 Л / кг телесне тежине. Просечно време боравка је близу 7 сати након поткожне примене.
У равнотежном стању након поновљене примене, привидни полувреме елиминације Миелостима из серума је приближно 3-4 сата након поткожне ињекције и краће (1-1,5 сати) након интравенске инфузије.
Клиренс рХуГ-ЦСФ у плазми повећан је три пута (50 до 150 мл / мин) након поновљене поткожне примене.
Мање од 1% ленограстима се излучује непромењено урином и стога се верује да се метаболише у пептиде.
Током више поткожних доза, максималне серумске концентрације ленограстима су близу 100 пг / мл / кг телесне тежине при препорученој дози. Постоји позитивна корелација између дозе и серумске концентрације Миелостима и између неутрофилног одговора и укупне количине ленограстима у серуму.
05.3 Предклинички подаци о безбедности
Студије акутне токсичности (до 1000 мцг / кг / дан код мишева) и субакутне токсичности (до 100 мцг / кг / дан код мајмуна) показале су да су ефекти предозирања ограничени на реверзибилно погоршање фармаколошких ефеката.
У студијама на пацовима и зечевима Миелостим није показао тератогену активност. Повећана учесталост побачаја је примећена код зечева, али нису пронађене малформације.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Прашина
- Аргинин
- Фенилаланин
- Метионин
- Манитол (Е421)
- Полисорбат 20
- Разблажена хлороводонична киселина (за подешавање пХ)
Солвент
Вода за ињекције
06.2 Некомпатибилност
Овај лек се не сме мешати са другим производима осим са онима који су поменути у одељку 6.6.
06.3 Период важења
2,5 године (30 месеци).
Након реконституције или разблаживања, препоручује се тренутна употреба.
Међутим, стабилност реконституисаног / разблаженог лека показана је 24 сата на 2 ° Ц-8 ° Ц (у фрижидеру).
06.4 Посебне мере предострожности при складиштењу
Не чувати на температури изнад 30 ° Ц.
Немојте замрзавати.
За услове складиштења реконституисаног / разблаженог производа видети одељак 6.3
06.5 Природа непосредног паковања и садржај паковања
263 мцг прашка у бочици (стакло типа И) са гуменим чепом (бутил гума типа И)
+ 1 мл растварача у ампули (стакло типа И); Величине паковања од 1 или 5. Не могу се ставити у промет све величине паковања.
06.6 Упутства за употребу и руковање
Неискоришћени производ / раствор или отпадни материјал морате одложити у складу са локалним прописима
Упутства за припрему
Бочице са мијелостимом су само за једнократну употребу.
Миелостим се мора реконституисати пре субкутане или интравенозне примене.
Припрема реконституисаног раствора Миелостима
Коришћењем градуисаног шприца опремљеног иглом, асептично извуците цео садржај екстракта бочице са растварачем за Миелостим.Ињектирајте цео садржај шприца у одговарајућу бочицу Миелостима.
Лагано протресите док се потпуно не раствори. Не тресите снажно. Реконституисани парентерални раствор делује бистро и без честица.
Пожељно је да се реконституисани раствор користи одмах након припреме. За услове складиштења реконституисаног / разблаженог производа видети одељак 6.3.
Припрема за субкутану примену
Припремите реконституисани раствор Миелостима како је горе описано.
Док држите иглу шприца уметнутом у бочицу, извуците потребну запремину реконституисаног раствора из бочице.Замените иглу која се користи за реконституцију и уметните одговарајућу иглу за поткожно убризгавање у шприц.
Одмах применити поткожном ињекцијом (за начине примене видети одељак 4.2).
Припрема инфузије за интравенозну примену:
За интравенозну примену, Миелостим се мора разблажити након реконституције. Припремите реконституисани раствор Миелостима како је горе описано.
Док држите иглу шприца уметнутом у бочицу, извуците потребну запремину реконституисаног раствора из бочице Разблажите реконституисани раствор Миелостима до потребне концентрације убризгавањем потребне запремине у 0,9% раствор натријум хлорида или раствор декстрозе до 5%.
Давати интравенозно (за методе примене видети одељак 4.2).
Миелостим је компатибилан са најчешће коришћеним перфузијским сетовима када се разблажи и у 0,9% физиолошком раствору (вреће од поливинилхлорида и стаклене боце) и у 5% раствору декстрозе (стаклене боце). Не препоручују се разблаживања Миелостима 34 милиона ИУ / мЛ при крајњој концентрацији испод 0,32 милиона ИУ / мЛ (2,5 мцг / мЛ). Реконституисана бочица са Миелостимом од 34 милиона ИУ / мл не може се разблажити у запреминама већим од 100 мл.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Италфармацо С.п.А. - Виале Фулвио Тести, 330 - 20126 Милано (Италија)
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
АИЦ н. 029059019 - 34 милиона ИУ / мл 1 бочица праха + 1 бочица растварача 1 мл
АИЦ н. 029059021 - 34 милиона ИУ / мл 5 бочица праха + 5 бочица растварача 1 мл
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Прво овлашћење: 13. фебруара 1995. године
Обнова овлашћења: 28. јула 2008









-cloruro.jpg)