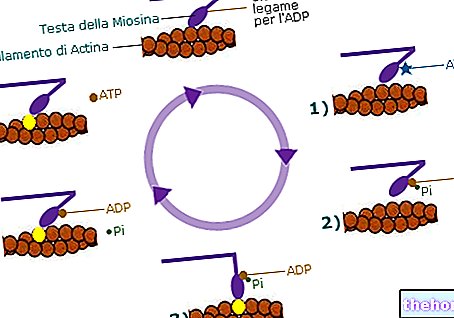
Β-оксидација је скуп процеса који се одвијају на угљенику у Β до карбонила.
Први ензим у процесу је "ацил коензим А дехидрогеназа који се налази на унутрашњој митохондријској мембрани и има ФАД као кофактор који је редукован на ФАДХ2 и даје своју редукциону моћ коензиму К (респираторни ланац); овај ензим катализује реакцију која из ацил коензима А доводи до стварања еноил коензима А (тачније транс 2,3 еноил коензима А) који је незасићен α-Β систем (алкен). Други ензим б-оксидације је "еноил коензим А хидратаза који претвара еноил у Л-Β хидрокси ацил коензим А; овај ензим је апсолутно стереоспецифичан за изомер Л-Β хидрокси ацил коензима А.
Накнадну реакцију катализује Л-Β хидрокси ацил коензим А дехидрогеназа (НАД зависни ензим) који претвара Л-Β хидрокси ацил коензим А у б-кето ацил коензим А; у исто време долази до редукције НАД + у НАДХ.
Коначно, умеша се један тиолаза (б-кето ацил коензим А тиолаза); реакција такође захтева литичко средство представљено коензимом А: формира се фрагмент са два атома угљеника (тј. "ацетил коензим А"), а преостали угљенични скелет представља ацил коензим А (у поређењу са почетним изгубио је два атома угљеника) ).
Ацил коензим А добијен са Β-оксидација, понавља процес док се не добије само ацетил коензим А.
Готово апсолутно правило: када дође до дехидрогенације између два суседна атома са јасном разликом у афинитету према електрону, кофактор ензима дехидрогеназе је скоро увек НАД, док, ако се дехидрогенација догоди између два суседна атома укључујући ц ", постоји мала разлика у афинитету електрона , кофактор је ФАД.