Активни састојци: Елетриптан
РЕЛПАКС® 20 мг филмом обложене таблете
РЕЛПАКС® 40 мг филмом обложене таблете
Зашто се користи Релпак? За шта је то?
Релпак садржи активну супстанцу елетриптан. Релпак припада класи лекова који се називају агонисти серотонинских рецептора. Серотонин је природна супстанца која се налази у мозгу и промовише сужавање крвних судова.
Релпак се може користити за лечење мигрене са или без ауре код одраслих пацијената. Пре напада мигрене, може проћи фазу која се назива „аура“, а која укључује сметње вида, утрнулост и сметње говора.
Контраиндикације Када се Релпак не сме користити
Немојте узимати РЕЛПАКС
- Ако сте алергични (преосетљиви) на елетриптан или неки други састојак овог лека (наведен у одељку 6).
- Ако имате тешку болест јетре или бубрега
- Ако имате умерену до тешку хипертензију или благу нелечену хипертензију.
- Ако патите или сте икада патили од срчаних проблема [нпр. срчани удар, ангина, затајење срца или велики абнормални срчани ритам (аритмија), нагло, привремено сужење једне од коронарних артерија].
- Ако патите од затајења циркулације (периферне васкуларне болести).
- Ако сте имали мождани удар (чак и благи који је трајао само неколико минута или сати).
- Ако сте узимали ерготамин или деривате ерготамина (укључујући метисергид) 24 сата пре или после узимања лека Релпак.
- Ако узимате друге лекове који се завршавају са „триптан“ (нпр. Суматриптан, ризатриптан, наратриптан, золмитриптан, алмотриптан и фроватриптан).
Разговарајте са својим лекаром и не узимајте Релпак ако сте икада искусили било које од горе наведених стања.
Предострожности при употреби Шта треба да знате пре него што узмете лек Релпак
Разговарајте са својим лекаром или фармацеутом пре него што узмете лек Релпак ако:
- имају дијабетес
- пушите или сте на терапији замене никотина
- је мушко и има више од 40 година
- је женског пола и у постменопаузи
- ви или члан породице имате коронарну болест срца
- речено вам је да сте у опасности од срчаних обољења, пре него што узмете лек Релпак, разговарајте са својим лекаром
Поновљена употреба лекова против мигрене
Поновљена употреба лека Релпак или других лекова против мигрене неколико дана или недеља може изазвати хроничну дневну главобољу. Реците свом лекару ако се то догоди, јер ћете можда морати да прекинете лечење.
Интеракције Који лекови или храна могу променити ефекат лека Релпак
Други лекови и Релпак
Обавестите свог лекара или фармацеута ако узимате, недавно сте узимали или бисте могли да узмете било који други лек.
Узимање лека Релпак са другим лековима може изазвати озбиљне нуспојаве. Немојте користити Релпак ако:
- узимали ерготамин или деривате ерготамина (укључујући метисергид) 24 сата пре или после узимања лека Релпак
- ако узимате друге лекове који се завршавају са „триптан“ (нпр. суматриптан, ризатриптан, наратриптан, золмитриптан, алмотриптан и фроватриптан).
Неки лекови могу утицати на начин на који Релпак делује, или Релпак може смањити ефикасност других лекова који се узимају истовремено, укључујући:
- Лекови који се користе за лечење гљивичних инфекција (нпр. Кетоконазол и итраконазол)
- Лекови који се користе за лечење бактеријских инфекција (нпр. Еритромицин, кларитромицин и јосамицин).
- Лекови који се користе за лечење АИДС -а и ХИВ -а (нпр. Ритонавир, индинавир и нелфинавир).
Кантарион (Хиперицум перфоратум) не треба узимати истовремено са овим леком.
Пре него што узмете лек Релпак, реците свом лекару ако узимате одређене лекове (који се обично називају ССРИ *или СНРИ **) за депресију или друге менталне поремећаје. Ови лекови могу повећати ризик од развоја серотонинског синдрома када се користе заједно са неким лековима за мигрену. Погледајте одељак 4 „Могући нежељени ефекти“ за више информација о симптомима серотонинског синдрома.
* ССРИ - селективни инхибитори поновног преузимања серотонина
** СНРИ - инхибитори поновног преузимања серотонина и норадреналина
РЕЛПАКС уз храну и пиће
Релпак се може узети пре или после јела и пића.
Упозорења Важно је знати да:
Трудноћа и дојење
Питајте свог лекара или фармацеута за савет пре него што узмете било који лек.
Ако сте трудни или дојите, мислите да сте трудни или планирате трудноћу, питајте лекара за савет пре него што узмете овај лек.
Препоручује се да избегавате дојење 24 сата након узимања овог лека.
Вожња и управљање машинама
Релпак или мигрене могу изазвати поспаност. Овај лек такође може изазвати вртоглавицу. Због тога се препоручује да избегавате вожњу возила или руковање машинама током кризе мигрене или након узимања овог лека.
Релпак садржи лактозу и жуто алуминијумско језеро за залазак сунца (Е 110)
Лактоза је врста шећера. Ако вам је речено да имате „нетолеранцију на неке шећере, обратите се свом лекару пре узимања овог лека. Језеро од алуминијумског заласка сунца (Е 110) може изазвати алергијске реакције.
Доза, начин и време примене Како се користи Релпак: Дозирање
Увек узимајте овај лек увек тачно онако како вам је рекао лекар. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
Одрасли
Овај лек се може узети било када након почетка напада мигрене, али најбоље је узети га што је пре могуће. Међутим, Релпак узимајте само у фази мигрене, немојте га узимати ради спречавања напада мигрене.
- Уобичајена почетна доза је једна таблета од 40 мг
- Таблету треба прогутати целу са чашом воде
- Ако прва таблета не уклони мигрену, немојте узети другу дозу за исти напад мигрене.
- Ако након прве таблете мигрена нестане, а затим се врати, можете узети другу дозу, међутим, након узимања прве таблете морате сачекати најмање 2 сата пре него што узмете другу.
- Не бисте требали узети више од 80 мг Релпака у 24 сата (2 таблете к 40 мг).
- Ако сматрате да једна таблета од 40 мг не уклања мигрену, молимо вас да обавестите свог лекара који може одлучити да повећа дозу на две таблете од 40 мг за будуће епизоде.
Употреба код деце и адолесцената млађих од 18 година
Релпак таблете се не препоручују деци и адолесцентима млађим од 18 година.
Старији грађани
Релпак таблете се не препоручују пацијентима старијим од 65 година.
Инсуфицијенција бубрега
Овај лек се може користити код пацијената са благим до умереним бубрежним проблемима.Код ових пацијената препоручује се почетна доза од 20 мг и укупна дневна доза од највише 40 мг. Ваш лекар ће вам саветовати коју дозу да узмете.
Хепатична инсуфицијенција
Овај лек се може користити код пацијената са благим до умереним обољењима јетре. Није потребно прилагођавање дозе за благо до умерено оштећење јетре.
Предозирање Шта треба учинити ако сте узели превише лека Релпак
Ако сте узели више лека Релпак него што је требало:
Ако сте случајно узели превише Релпак таблета, одмах се обратите лекару или идите у најближу хитну помоћ. Паковање лека увек носите са собом без обзира да ли вам је остала таблета или не. Нуспојаве узимања превише Релпак таблета укључују висок крвни притисак и проблеме са срцем.
Ако сте заборавили да узмете лек Релпак:
Ако сте заборавили да узмете таблету, узмите је чим се сетите, осим ако није време за следећу. Немојте узети двоструку дозу да бисте надокнадили заборављену.
Ако имате додатних питања о употреби овог лека, обратите се свом лекару или фармацеуту.
Нежељени ефекти Који су нежељени ефекти лека Релпак
Као и сви лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих.
Одмах обавестите свог лекара ако након узимања овог лека имате неки од доле наведених симптома
- Нагло пискање, отежано дисање, отечени капци, лице или усне, осип или свраб (нарочито по целом телу) јер то може бити симптом алергијске реакције.
- Бол и стезање у грудима који могу бити интензивни и утицати на грло. То могу бити симптоми проблема са циркулацијом срца (срчана исхемија).
- Знаци и симптоми серотонинског синдрома који могу укључивати узнемиреност, халуцинације, губитак координације, повећану брзину откуцаја срца, повећану телесну температуру, нагле промене крвног притиска и преактивне рефлексе.
Други нежељени ефекти који се могу појавити:
Честе (могу се јавити у до 1 на 10 особа)
- Бол у грудима или стезање или притисак, лупање срца, повећан број откуцаја срца
- Вртоглавица, осећај окретања тела или предмета (вртоглавица), главобоља, поспаност, смањена осетљивост на додир и бол
- Бол у грлу, стезање у грлу, сува уста
- Бол у стомаку и стомаку, лоше варење (стомачни поремећај), мучнина (осећај нелагоде и нелагодности у стомаку или стомаку са нагоном за повраћањем)
- Укоченост (повећан тонус мишића), мишићна слабост, болови у леђима, болови у мишићима
- Општи осећај слабости, осећај врућине, зимица, цурење из носа, знојење, трнци или ненормални осећаји, црвенило, бол.
Мање често (могу се јавити у до 1 на 100 особа)
- Тешко дисање, зијевање
- Отицање лица, руку или стопала, упала или инфекција језика, кожни осип, свраб
- Повећана осетљивост на додир или бол (хиперестезија), губитак координације, смањени или спори покрети, тремор, нејасан говор
- не осећате се као ви (деперсонализација), депресија, промењене мисли, узнемиреност, конфузија, промене расположења (еуфорија), периоди нереаговања (ступор), општи осећај нелагоде, болести или недостатка благостања (малаксалост), недостатак сна ( несаница)
- губитак апетита и тежине (анорексија), поремећај укуса, жеђ
- дегенерација зглобова (артроза), болови у костима, болови у зглобовима
- Повећана потреба за мокрењем, проблеми са мокрењем, прекомерно мокрење, дијареја
- Промена вида, бол у очима, нетолеранција на светле, суве или сузне очи
- Бол у ушима, зујање у ушима (тинитус)
- Смањена циркулација (поремећаји периферне циркулације)
Ретко (могу се јавити у до 1 на 1.000 људи)
- Шок, астма, кошница, кожни поремећаји, едем језика
- Инфекција грла или грудног коша, отечене лимфне жлезде
- Споро куцање срца
- Емоционална нестабилност (промене расположења)
- Дегенерација зглобова (артритис), мишићни поремећаји, контракције мишића
- Затвор, упала једњака, подригивање
- Бол у грудима, интензивне или продужене менструације
- Очне инфекције (коњунктивитис)
- Промена гласа
Други пријављени нежељени ефекти укључују несвестицу, висок крвни притисак, упалу дебелог црева и повраћање, несреће повезане са мозгом и крвним судовима, недовољно снабдевање крви срцем, срчани удар, грчеве артерија или срчаног мишића.
Ваш лекар може од вас тражити редовне тестове крви да провери повећане ензиме јетре или друге проблеме са крвљу.
Пријављивање нежељених ефеката
Ако приметите било које нежељено дејство, обратите се свом лекару или фармацеуту.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нежељене ефекте директно путем националног система за пријављивање на хттп://ввв.агензиафармацо.гов.ит/ит/респонсабили.Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока употребе (ЕКСП) наведеног на паковању. Датум истека се односи на последњи дан тог месеца.
ПВЦ Ацлар / Ал и ПВЦ / Ал блистери: Овај лек не захтева посебне услове складиштења. Боце од ХДПЕ -а: Чувати таблете у оригиналном паковању. Након отварања, контејнер држати добро затворен и даље од влаге.
Не бацајте никакве лекове у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Састав и фармацеутски облик
Шта Релпак садржи
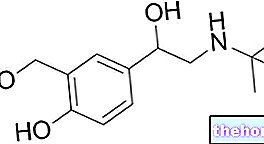
Активна супстанца лека Релпак је елетриптан (у облику елетриптан хидробромида).
Свака филмом обложена таблета Релпак 20 мг садржи 20 мг елетриптана (у облику елетриптан хидробромида).
Свака Релпак 40 мг филмом обложена таблета садржи 40 мг елетриптана (у облику елетриптан хидробромида).
Таблете такође садрже следеће састојке: микрокристалну целулозу, лактозу монохидрат, натријум кроскармелозу, магнезијум стеарат, титанијум диоксид (Е171), хипромелозу, глицерол триацетат, залазак сунца жуто ФЦФ алуминијумско језеро (Е110).
Опис како Релпак изгледа и садржај паковања
Релпак таблете су наранџасте боје и округлог облика.
Релпак 20 мг филмом обложене таблете имају ознаку „ПФИЗЕР“ на једној страни и „РЕП 20“ на другој.
Релпак 40 мг филмом обложене таблете имају ознаку "ПФИЗЕР" са једне стране и "РЕП 40" са друге стране.
Релпак је доступан у непрозирним ПВЦ Ацлар / Ал и непрозирним ПВЦ / Ал блистерима у паковањима од 2, 3, 4, 6, 10, 18, 30 и 100 таблета или у ХДПЕ бочицама са ХДПЕ / ПП затварачем отпорним на децу од 30 и 100 таблета .
Не могу се на тржиште ставити све величине паковања.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016.Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
РЕЛПАКС
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ
РЕЛПАКС 20 мг:
свака филмом обложена таблета садржи 20 мг елетриптана (у облику елетриптан хидробромида).
Помоћне супстанце: лактоза 23.000 мг; залазак сунца (Е110) 0,036 мг
РЕЛПАКС 40 мг:
свака филмом обложена таблета садржи 40 мг елетриптана (у облику елетриптан хидробромида).
Помоћне супстанце: лактоза 46.000 мг; залазак сунца (Е110) 0,072 мг
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Филмом обложене таблете.
Наранџасте, округле, конвексне таблете са ознаком "РЕП 20" или "РЕП 40" на једној страни и "Пфизер" на другој.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Акутно лечење фазе главобоље мигренских напада са или без ауре.
04.2 Дозирање и начин примене
РЕЛПАКС таблете треба узети што је пре могуће након почетка напада мигрене, али су такође ефикасне ако се узимају у каснијој фази.
Није показано да РЕЛПАКС, узет током фазе ауре, спречава нападе мигрене, па га треба узимати само у фази главобоље напада мигрене.
Таблете РЕЛПАКС не треба користити за профилаксу.
Таблете треба прогутати целе са водом.
Одрасли (од 18 до 65 година)
Препоручена почетна доза је 40 мг.
Ако се главобоља врати у року од 24 сата: Ако се напад мигрене понови у року од 24 сата након почетног одговора, друга доза лека РЕЛПАКС исте јачине показала се ефикасном у лечењу релапса. Ако је потребна друга доза, не треба је узети у року од 2 сата од узимања почетне дозе.
У случају да нема одговора: Ако пацијент не доживи побољшање главобоље у року од 2 сата од узимања прве дозе лека РЕЛПАКС, не би требало да узме другу дозу за исти напад јер клиничка испитивања нису адекватно утврдила ефикасност друге дозе у овим случајевима Клиничке студије показују да ће пацијенти који не реагују на лечење мигренског напада вероватно и даље реаговати на лечење за следећи напад.
Пацијенти који не постигну задовољавајући одговор након узимања 40 мг (нпр. Добра подношљивост и неуспех у 2 од 3 напада) могу бити задовољавајуће лечени дозом од 80 мг (2 к 40 мг таблете) у лечењу следећих напада (видети одељак 5.1 Фармакодинамичка својства - Додатне информације о клиничким студијама). Другу дозу од 80 мг не треба узети у року од 24 сата.
Максимална дневна доза не би требало да прелази 80 мг (видети одељак 4.8. Нежељени ефекти).
Старије особе (старије од 65 година)
Безбедност и ефикасност елетриптана код пацијената старијих од 65 година нису систематски процењивани због малог броја ових пацијената укључених у клиничка испитивања. Због тога се не препоручује употреба лека РЕЛПАКС код старијих пацијената.
Тинејџери (12-17 година)
Ефикасност лека РЕЛПАКС није утврђена у овој популацији пацијената, па се употреба производа не препоручује у овој старосној групи.
Педијатријски пацијенти (узраста 6-11 година)
Безбедност и ефикасност лека РЕЛПАКС код педијатријских пацијената нису процењени, па се употреба лека РЕЛПАКС не препоручује код пацијената ове старосне групе (видети 5.2 Фармакокинетичка својства).
Хепатична инсуфицијенција
Није потребно прилагођавање дозе код пацијената са благим или умереним оштећењем јетре. Пошто РЕЛПАКС није проучаван код пацијената са тешким оштећењем јетре, производ је контраиндикован код ових пацијената.
Инсуфицијенција бубрега
Пошто су ефекти лека РЕЛПАКС на крвни притисак повећани у присуству бубрежне инсуфицијенције (видети 4.4. Посебна упозорења и посебне мере опреза при употреби), препоручује се употреба почетне дозе од 20 мг код пацијената са благом или умереном бубрежном инсуфицијенцијом. максимална дневна доза не би требало да прелази 40 мг. РЕЛПАКС је контраиндикован код пацијената са тешком бубрежном инсуфицијенцијом.
04.3 Контраиндикације
Преосетљивост на елетриптан хидробромид или било коју помоћну супстанцу.
Пацијенти са тешком инсуфицијенцијом јетре или бубрега.
Умерена до тешка хипертензија или нелечена блага хипертензија.
Пацијенти са документованом коронарном артеријском болешћу, укључујући исхемијску болест срца (ангину пекторис, претходни инфаркт миокарда или документовану тиху исхемију), објективне или субјективне симптоме исхемијске болести срца или Принзметалову ангину.
Пацијенти са значајним аритмијама или срчаном инсуфицијенцијом.
Пацијенти са периферном васкулопатијом.
Пацијенти са претходном епизодом цереброваскуларне несреће (ЦВА) или пролазног исхемијског напада (ТИА).
Примена ерготамина или деривата ерготамина (укључујући метисергид) у року од 24 сата пре или после третмана елетриптаном (видети одељак 4.5. Интеракције са другим лековима и други облици интеракција). Истовремена примена других агониста 5-ХТ1 рецептора и елетриптана.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Овај лијек садржи лактозу.
Пацијенти са ретким наследним проблемима интолеранције на галактозу, недостатком Лапп-лактазе или малапсорпцијом глукозе-галактозе не би требало да узимају овај лек.
Овај лек такође садржи алуминијумско језеро за заласком сунца које може изазвати алергијске реакције.
РЕЛПАКС се не сме користити заједно са снажним инхибиторима ЦИП3А4 (нпр.кетоконазол, итраконазол, еритромицин, кларитромицин, јосамицин) и инхибиторе протеазе (ритонавир, индинавир и нелфинавир).
РЕЛПАКС треба користити само ако је успостављена јасна дијагноза мигрене. РЕЛПАКС није индикован за лечење хемиплегичне, офталмоплегичне или базиларне мигрене.
РЕЛПАКС се не сме давати за лечење "атипичних" главобоља, које су главобоље које могу бити повезане са потенцијално озбиљним медицинским стањима (мождани удар, пукнута анеуризма) у којима церебрална вазоконстрикција може бити опасна.
Употреба елетриптана може бити повезана са неким пролазним симптомима, укључујући бол у грудима и стезање у грудима, који могу бити интензивни и могу утицати на грло (видети одељак 4.8. Нежељени ефекти). Када се сматра да ови симптоми указују на исхемијску болест срца, не треба узети друге дозе и извршити одговарајућу процену.
РЕЛПАКС се не сме давати, без претходног испитивања, пацијентима код којих је вероватно недијагностикована срчана болест или пацијентима у ризику од коронарне артеријске болести (ЦАД) (нпр. Пацијентима са хипертензијом, дијабетесом, пушачима или онима који користе никотинску замену) терапију, мушкарци старији од 40 година, жене у постменопаузи и жене са значајном породичном историјом коронарне болести срца). Кардијалне претраге можда неће идентификовати све пацијенте са срчаним обољењима, а у врло ретким случајевима дошло је до озбиљних срчаних догађаја код пацијената који нису имали основну срчану болест када су давани агонисти 5-ХТ1 рецептора. РЕЛПАКС се не сме давати пацијентима са утврђеном коронарном артеријском болешћу (видети одељак 4.3 Контраиндикације).
Употреба агониста 5-ХТ1 рецептора повезана је са коронарним вазоспазмом, а ретки су случајеви исхемије миокарда или инфаркта миокарда након употребе агониста 5-ХТ1 рецептора.
Нежељени ефекти могу бити чешћи ако се триптани узимају истовремено са биљним препаратима који садрже кантарион (Хиперицум перфоратум).
У оквиру терапијских доза које су се користиле у клиничким испитивањима, употреба доза елетриптана од 60 мг или више резултирала је благим и пролазним повећањем крвног притиска. Међутим, у клиничким испитивањима нису забележени клинички докази о таквим променама крвног притиска.Ефекат је био много израженији код особа са бубрежном инсуфицијенцијом и код старијих особа. Код пацијената са бубрежном инсуфицијенцијом, опсег средњих максималних повећања систолног крвног притиска био је 14-17 ммХг (нормално 3 ммХг), а дијастолног крвног притиска 14-21 ммХг (нормално 4 ммХг). Код старијих испитаника, просечно максимално повећање систолног крвног притиска било је 23 ммХг у поређењу са 13 ммХг код младих одраслих особа (плацебо 8 ммХг).
У постмаркетиншкој фази производа, такође је забележен пораст крвног притиска код пацијената лечених дозама елетриптана од 20 мг и 40 мг и код пацијената који нису имали оштећење бубрега и који нису били старији.
Главобоља од прекомерне употребе лекова (Главобоља од прекомерне употребе лекова - МОХ)
Дуготрајна употреба било ког средства за ублажавање болова за лечење главобоље може га погоршати. Ако се сумња или се јави ово стање, пацијенту треба саветовати да потражи лекарску помоћ, а лечење треба прекинути. Ако се јаве напади, честе или свакодневне главобоље, упркос ( или због) редовне употребе лекова за лечење главобоље, треба претпоставити да су пацијенти развили главобољу од прекомерне употребе лекова (МОХ).
Пријављене су епизоде серотонинског синдрома (укључујући ментално промењена стања, аутономну нестабилност и неуромишићне абнормалности) након истовремене примене триптана и селективних инхибитора поновног преузимања серотонина (ССРИ) или лекова са инхибитором поновног преузимања серотонина и норепинефрина (СНРИ). Ове реакције могу бити озбиљне. Када је истовремена употреба елетриптана и ССРИ или СНРИ клинички оправдана, саветује се одговарајуће праћење пацијената, посебно на почетку лечења, у случају повећања дозе или у случају давања додатног лека са серотонергичком активношћу (видети одељак 4.5) .
04.5 Интеракције са другим лековима и други облици интеракција
Ефекти других лекова на елетриптан
У кључним клиничким студијама са елетриптаном нису забележени никакви докази о интеракцији са бета-блокаторима, трицикличким антидепресивима, селективним инхибиторима поновног преузимања серотонина и флунаризином, али нема података из специфичних студија интеракција са овим лековима (осим пропранолола, види доле).
Популациона ПК анализа заснована на подацима прикупљеним из клиничких испитивања сугерише да је мало вероватно да ће следећи лекови променити фармакокинетичка својства елетриптана: бета-блокатори, трициклични антидепресиви, селективни инхибитори поновног преузимања серотонина, хормонска терапија естрогенима, орални контрацептиви који садрже естроген и калцијум блокатори канала.
Елетриптан није супстрат за МАО. Због тога се не очекују интеракције између елетриптана и инхибитора МАО. Из тог разлога, нису спроведене посебне студије интеракције.
У студијама са пропранололом (160 мг), верапамилом (480 мг) и флуконазолом (100 мг), Цмак елетриптана се повећала 1,1, 2,2 и 1,4 пута. АУЦ елетриптана повећана је 1,3, 2,7 и 2,0 пута. Ови ефекти се не сматрају клинички значајним јер није било повећања крвног притиска или нежељених догађаја у поређењу са самим елетриптаном.
У клиничким студијама са еритромицином (1000 мг) и кетоконазолом (400 мг), специфичним и снажним инхибиторима ЦИП3А4, примећено је значајно повећање Цмак елетриптана (2 и 2,7 пута) и АУЦ (3,6 и 5,9 пута). Ово повећање изложености било је повезано са повећањем елетриптан т1 / 2 са 4,6 на 7,1 сат након примене еритромицина и са 4,8 на 8,3 сата након примене кетоконазола (видети 5.2 Фармакокинетичка својства). Стога се РЕЛПАКС не сме користити заједно са моћним Инхибитори ЦИП3А4 (нпр. Кетоконазол, итраконазол, еритромицин, кларитромицин, јосамицин) и инхибитори протеазе (ритонавир, индинавир и нелфинавир).
У клиничким испитивањима са оралним кофеином / ерготамином датим 1 и 2 сата након елетриптана, примећено је мало али адитивно повећање крвног притиска; таква повећања су предвидљива на основу фармакологије два лека. Због тога се препоручује да се не узимају лекови који садрже ерготамин или сличне ерготамину (нпр. Дихидроерготамин) у року од 24 сата након примене елетриптана. Слично, требало би да прође најмање 24 сата између примене препарата који садржи ерготамин и примене елетриптана.
Ефекти елетриптана на друге лекове
Не постоји ин витро или ин виво нема доказа да би терапијске дозе елетриптана (и повезане концентрације) могле резултирати "инхибицијом или индукцијом" ензима цитокрома П450, укључујући ЦИП3А4, одговорног за метаболизам лекова. Због тога се сматра да елетриптан неће изазвати клинички значајне реакције интеракције лекова посредоване овим ензимима.
Селективни инхибитори поновног преузимања серотонина (ССРИ) / инхибитори поновног преузимања серотонина норадреналина (СНРИ) и серотонински синдром:
Симптоми конзистентни са серотонинским синдромом (укључујући измењена ментална стања, аутономну нестабилност и неуромишићне абнормалности) пријављени су код неких пацијената након употребе селективних инхибитора поновног преузимања серотонина (ССРИ) или инхибитора поновног преузимања серотонин норепинефрина (СНРИ).) И триптана (видети одељак 4.4). ).
04.6 Трудноћа и дојење
Трудноћа:
Нема доступних клиничких података о употреби лека РЕЛПАКС у трудноћи. Студије на животињама не указују на директне или индиректне штетне ефекте на трудноћу, ембрионални / фетални развој, порођај или постнатални развој. РЕЛПАКС треба користити у трудноћи само ако је то неопходно.
Време храњења:
Елетриптан се излучује у мајчино млеко. У студији која је обухватила 8 жена лечених једном дозом од 80 мг, просечна укупна количина елетриптана пронађена у мајчином млеку током 24 сата била је 0,02% дозе. Међутим, потребан је опрез приликом узимања. Размислите о примени лека РЕЛПАКС дојиљама. Изложеност одојчади може се умањити избегавањем дојења 24 сата након узимања лека.
04.7 Утицај на способност управљања возилима и машинама
Лечење мигрене или леком РЕЛПАКС може изазвати поспаност или вртоглавицу код неких пацијената. Пацијенте треба саветовати да процене своју способност обављања сложених задатака, попут вожње аутомобила, током напада мигрене и након узимања лека РЕЛПАКС.
04.8 Нежељени ефекти
РЕЛПАКС је примењен у клиничким студијама на преко 5000 испитаника који су узимали једну или две дозе од 20 мг, 40 мг или 80 мг. Најчешће нежељене реакције биле су астенија, сомноленција, мучнина и вртоглавица. У рандомизираним клиничким испитивањима спроведеним у дозама од 20 мг, 40 мг и 80 мг, примећена је корелација између учесталости нежељених догађаја и повећања дозе. Следеће нежељене реакције (са „инциденцом ≥ 1% и већом од плацеба) пријављене су у клиничким испитивањима код пацијената лечених у терапијским дозама. Догађаји су категорисани према учесталости: чести (≥1 / 100,
Инфекције и инфестације
Често: фарингитис и ринитис;
Ретко: инфекције респираторног тракта.
Поремећаји крви и лимфног система
Ретко: лимфаденопатија.
Поремећаји метаболизма и исхране
Мање често: анорексија.
Психијатријски поремећаји
Мање често: Промењено мишљење, узнемиреност, конфузија, деперсонализација, еуфорија, депресија и несаница;
Ретко: емоционална нестабилност.
Поремећаји нервног система
Често: сомноленција, главобоља, вртоглавица, парестезија или дисестезија, хипертонија, хипоестезија и миастенија;
Мање често: тремор, хиперестезија, атаксија, хипокинезија, поремећаји говора, омамљеност и промењени укус.
Поремећаји ока
Мање често: оштећење вида, бол у очима, фотофобија и поремећај сузења;
Ретко: коњунктивитис.
Поремећаји уха и лавиринта
Често: вртоглавица;
Мање често: бол у ушима, тинитус.
Срчане патологије
Често: лупање срца и тахикардија;
Ретко: брадикардија.
Васкуларне патологије
Уобичајено: налети врућине;
Мање често: периферни васкуларни поремећаји;
Ретко: шок.
Поремећаји дисања, грудног коша и медијастинума
Често: стезање у грлу;
Мање често: диспнеја, респираторни поремећаји и зевање;
Ретко: астма и промењен глас.
Гастроинтестинални поремећаји
Често: бол у трбуху, мучнина, сува уста и диспепсија;
Мање често: дијареја и глоситис;
Ретко: затвор, езофагитис, едем језика и подригивање.
Хепатобилиарни поремећаји
Ретко: повећан билирубин и АСТ.
Поремећаји коже и поткожног ткива
Често: знојење;
Мање често: осип и свраб;
Ретко: промене на кожи и уртикарија.
Поремећаји мишићно -коштаног система, везивног ткива и костију
Често: болови у леђима, болови у мишићима;
Мање често: артралгија, остеоартритис и болови у костима;
Ретко: артритис, миопатија и грчеви мишића.
Бубрега и уринарног поремећаји
Мање често: полакиурија, поремећаји уринарног тракта и полиурија.
Болести репродуктивног система и дојке
Ретко: бол у дојкама и менорагија.
Општи поремећаји и стања на месту примене
Често: осећај топлоте, астенија, симптоми у грудима (бол, стезање, притисак) и зимица;
Мање често: малаксалост, едем лица, жеђ, едем и периферни едем.
Нежељени догађаји који се обично јављају код елетриптана су типични већ пријављени за класу агониста 5-ХТ1 рецептора.
У постмаркетиншкој фази производа пријављени су следећи нежељени ефекти:
Поремећаји имунолошког система: алергијске реакције, од којих неке могу бити озбиљне, укључујући ангиоедем.
Поремећаји нервног система: серотонински синдром, ретки случајеви синкопе
Васкуларне патологије: хипертензија
Гастроинтестинални поремећаји: Као и код других агониста 5-ХТ1Б / 1Д рецептора, забележени су ретки случајеви исхемијског колитиса; Повратио се.
04.9 Предозирање
Неки субјекти су лечени појединачним дозама од 120 мг без пријављивања значајних нежељених догађаја. Међутим, хипертензија или други тежи кардиоваскуларни симптоми могу се појавити у случају предозирања на основу класе лекова.
У случају предозирања, потребно је усвојити стандардне мере подршке. Полувреме елиминације елетриптана је приближно 4 сата и стога, након предозирања елетриптаном, пацијенте треба надзирати и примењивати општу супортивну негу најмање 20 сати или док се знакови и симптоми не повуку.
Учинци хемодијализе или перитонеалне дијализе на серумске концентрације елетриптана нису познати.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: Селективни агонисти рецептора серотонина (5ХТ1). АТЦ ознака: Н02ЦЦ06.
Механизам деловања / фармакологија: Елетриптан је селективни агонист васкуларних 5-ХТ1Б рецептора и неуронских 5-ХТ1Д рецептора. Елетриптан такође показује „висок афинитет за 5-ХТ1Ф рецептор и то може допринети његовом механизму деловања против мигрене“. Елетриптан има скроман афинитет за хумане рекомбинантне 5-ХТ1А, 5-ХТ2Б, 5-ХТ1Е и 5-ХТ7 рецепторе.
Сазнајте више о клиничким испитивањима
Ефикасност РЕЛПАКС-а у акутном третману мигрене процењена је у 10 плацебо контролисаних клиничких испитивања на приближно 4000 пацијената лечених РЕЛПАКС-ом у дозама у распону од 20 мг до 80 мг. Ублажавање напада мигрене догодило се већ 30 минута након оралне примјене.Стопе одговора (смањење умереног или јаког мигренског бола без бола или благи бол) 2 сата након примене биле су 59-77% за дозу од 80 мг, 54-65% за дозу од 40 мг, 47-54% за 20 мг дозе и 19-40% за плацебо РЕЛПАКС се такође показао ефикасним у лечењу симптома повезаних са мигреном као што су повраћање, мучнина, фотофобија и фонофобија.
Препорука за повећање дозе на 80 мг заснована је на дуготрајним отвореним студијама и краткотрајној двоструко слепој студији у којој је примећен само тренд ка статистичкој значајности.
РЕЛПАКС задржава своју ефикасност у лечењу мигрене повезане са менструалним циклусом.Није показано да РЕЛПАКС, када се узима током фазе ауре, спречава мигренске главобоље, па се стога РЕЛПАКС треба узимати само у фази главобоље.
У фармакокинетичкој студији која није контролисана плацебом код пацијената са оштећењем бубрега, примећен је већи пораст крвног притиска након примене дозе од 80 мг РЕЛПАКС-а него код здравих добровољаца (видети одељак 4.4). Овај налаз се не може објаснити на основу фармакокинетичких варијација и стога може представљати специфичан фармакодинамички ефекат након примене елетриптана код пацијената са бубрежном инсуфицијенцијом.
05.2 "Фармакокинетичка својства
Апсорпција:
Елетриптан се добро и брзо апсорбује из гастроинтестиналног тракта (најмање 81%) након оралне примене. Апсолутна орална биорасположивост код мушкараца и жена је приближно 50%. Средњи Тмак је 1,5 сат након оралне примене. Фармакокинетика је линеарно доказана употреба лека у терапијском распону доза (20-80 мг).
АУЦ и Цмак елетриптана повећале су се за приближно 20-30% након оралне примене уз оброк са високим садржајем масти. Након оралне примене током напада мигрене, примећено је приближно 30% смањење АУЦ -а, док се Тмак повећао на 2,8 сати.
Након поновљеног дозирања (20 мг 3 пута дневно) током 5-7 дана, фармакокинетика елетриптана остала је линеарна, а проценат акумулације остао унутар очекиваних вредности. Вишеструким дозирањем већих доза (40 мг 3 пута дневно и 80 мг 2 пута / дан), акумулација елетриптана током 7 дана била је већа од очекиване (приближно 40%).
Дистрибуција:
Волумен дистрибуције елетриптана након интравенозне примене је 138 литара, што указује на дистрибуцију ткива. Елетриптан се везује за протеине плазме само у умереном проценту (приближно 85%).
Метаболизам:
Студије ин витро указују на то да се елетриптан примарно метаболише јетреним ензимом цитокром П450, ЦИП3А4. То се показује повећањем концентрације елетриптана у плазми након истовремене примене еритромицина и кетоконазола, познатих снажних и селективних инхибитора ЦИП3А4. Студије ин витро они такође показују скромну укљученост ЦИП2Д6, иако клиничке студије не указују на било какве доказе полиморфизма са овим ензимом.
Идентификована су два главна метаболита у циркулацији који значајно доприносе радиоактивности у плазми након примене 14-обележеног елетриптана. Метаболит настао Н-оксидацијом није показао никакву активност на животињским моделима ин витро. Метаболит настао Н-деметилацијом је уместо тога показао на животињским моделима ин витро, активност слична оној елетриптана.Треће подручје радиоактивности у плазми није формално идентификовано, али се највероватније ради о комбинацији хидроксилираних метаболита који су такође откривени у урину и измету.
Концентрације активног Н-десметил метаболита у плазми су само 10-20% концентрација основног лека и стога се не очекује да ће значајно допринети терапијској активности елетриптана.
Елиминација:
Просечан укупни клиренс елетриптана у плазми након интравенозне примене износи 36 л / х са полувременом елиминације у плазми од приближно 4 сата. Средњи бубрежни клиренс након оралне примене је приближно 3,9 л / х. Бубрези чине приближно 90% укупног клиренса што указује на то да се елетриптан елиминише првенствено путем метаболизма.
Фармакокинетика у одређеним групама пацијената
Пол припадности:
Мета-анализа свих клиничких фармаколошких студија и популацијска фармакокинетичка анализа изведена на основу података из клиничких испитивања показују да пол не утиче значајно на концентрацију елетриптана у плазми.
Старије особе (старије од 65 година):
Иако није статистички значајно, примећено је мало (16%) смањење клиренса повезано са статистички значајним повећањем полувремена (са приближно 4,4 сата на 5,7 сати) код старијих пацијената (65-93 године) и млађих одраслих испитаника. старији пацијенти.
Тинејџери (12-17 година):
Фармакокинетика елетриптана (40 мг и 80 мг) код адолесцентних пацијената са мигреном који су узимали лек у међукритичном периоду била је слична оној код здравих одраслих особа.
Деца (6-11 година):
Нема разлика у клиренсу елетриптана код деце у односу на адолесценте. Међутим, волумен дистрибуције је мањи код деце, а нивои у плазми су већи од очекиваног након примене примењене дозе код одраслих.
Оштећење јетре:
Испитаници са оштећењем јетре (Цхилд-Пугх А и Б) показали су статистички значајно повећање и АУЦ (34%) и полувреме елиминације. Уочено је мало повећање Цмак (18%). Ова скромна промена у изложености лека није сматра клинички релевантним.
Оштећење бубрега:
Пацијенти са благим (клиренс креатинина 61-89 мЛ / мин), умереним (клиренс креатинина 31-60 мЛ / мин) или тешким (клиренс креатинин протеина у плазми) бубрежним оштећењем.
У овој групи пацијената примећен је пораст крвног притиска.
05.3 Предклинички подаци о безбедности
Неклинички подаци не откривају никакав посебан ризик за људе, што показују конвенционалне студије фармаколошке сигурности, токсичност при поновљеним дозама, генотоксичност, канцерогени потенцијал и репродуктивна токсичност.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Језгро: микрокристална целулоза; лактоза монохидрат; натријум кроскармелоза; магнезијум стеарат.
Премаз: титанијум диоксид (Е171); хипромелоза; лактоза монохидрат; триацетин; залазак сунца жут (Е110).
06.2 Некомпатибилност
Није битно.
06.3 Период важења
3 године.
06.4 Посебне мере предострожности при складиштењу
Непрозирни ПВЦ / Ацлар или непрозирни ПВЦ / алуминијумски блистери: производ не захтева посебне мере предострожности при складиштењу.
Боце од ХДПЕ -а: држите контејнер добро затвореним како бисте га заштитили од влаге.
06.5 Природа непосредног паковања и садржај паковања
Непрозирни ПВЦ / Ацлар или непрозирни ПВЦ / алуминијумски блистер у паковању од 2, 3, 4, 6, 10, 18, 30 и 100 таблета (20 мг, 40 мг).
ХДПЕ бочице са ХДПЕ / ПП дечијим затварачем од 30 и 100 таблета (20 мг, 40 мг).
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Нема посебних упутстава.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
ПФИЗЕР ИТАЛИА С.р.л. - Виа Исонзо, 71 - 04100 Латина
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
РЕЛПАКС 20 мг филмом обложене таблете:
Алуминијумски блистер, 2 таблете - АИЦ: 035307014 / М
Алуминијумски блистер, 3 таблете - АИЦ: 035307026 / М
Алуминијумски блистер, 4 таблете - АИЦ: 035307038 / М
Алуминијумски блистер, 6 таблета - АИЦ: 035307040 / М
Алуминијумски блистери, 10 таблета у одвојивим јединицама - АИЦ: 035307053 / М
Алуминијумски блистер, 18 таблета - АИЦ: 035307065 / М
Алуминијумски блистери, 30 таблета у одвојивим јединицама - АИЦ: 035307077 / М
Алуминијумски блистери, 100 таблета у одвојивим јединицама - АИЦ: 035307089 / М
Ацлар блистер, 2 таблете - АИЦ: 035307091 / М
Ацлар блистер, 3 таблете - АИЦ: 035307103 / М
Ацлар блистер, 4 таблете - АИЦ: 035307115 / М
Ацлар блистер, 6 таблета - АИЦ: 035307127 / М
Ацлар блистер, 10 таблета у одвојивим јединицама - АИЦ: 035307139 / М
Ацлар блистер, 18 таблета - АИЦ: 035307141 / М
Ацлар блистер, 30 таблета у одвојивим јединицама - АИЦ: 035307154 / М
Ацлар блистер, 100 таблета у одвојивим јединицама - АИЦ: 035307166 / М
ХДПЕ боца, 30 таблета - АИЦ: 035307178 / М
ХДПЕ боца, 100 таблета - АИЦ: 035307180 / М
РЕЛПАКС 40 мг филмом обложене таблете:
Алуминијумски блистер, 2 таблете - АИЦ: 035307192 / М
Алуминијумски блистер, 3 таблете - АИЦ: 035307204 / М
Алуминијумски блистер, 4 таблете - АИЦ: 035307216 / М
Алуминијумски блистер, 6 таблета - АИЦ: 035307228 / М
Алуминијумски блистери, 10 таблета у одвојивим јединицама - АИЦ: 035307230 / М
Алуминијумски блистер, 18 таблета - АИЦ: 035307242 / М
Алуминијумски блистери, 30 таблета у одвојивим јединицама - АИЦ: 035307255 / М
Алуминијумски блистери, 100 таблета у одвојивим јединицама - АИЦ: 035307267 / М
Ацлар блистер, 2 таблете - АИЦ: 035307279 / М
Ацлар блистер, 3 таблете - АИЦ: 035307281 / М
Ацлар блистер, 4 таблете - АИЦ: 035307293 / М
Ацлар блистер, 6 таблета - АИЦ: 035307305 / М
Ацлар блистер, 10 таблета у одвојивим јединицама - АИЦ: 035307317 / М
Ацлар блистер, 18 таблета - АИЦ: 035307329 / М
Ацлар блистер, 30 таблета у одвојивим јединицама - АИЦ: 035307331 / М
Ацлар блистер, 100 таблета у одвојивим јединицама - АИЦ: 035307343 / М
ХДПЕ боца, 30 таблета - АИЦ: 035307356 / М
ХДПЕ боца, 100 таблета - АИЦ: 035307368 / М
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
22. јануар 2002. / 12. фебруар 2011. године
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
15. новембра 2012
11.0 ЗА РАДИО ДРОГЕ, ПОТПУНИ ПОДАЦИ О ДОСИМЕТРИЈИ ИНТЕРНОГ ЗРАЧЕЊА
12.0 ЗА РАДИО -ЛИЈЕКОВЕ, ДОДАТНА ДЕТАЉНА УПУТСТВА О ПРИМЕРНОЈ ПРИПРЕМИ И КОНТРОЛИ КВАЛИТЕТА
ВАЖНЕ ИНФОРМАЦИЈЕ НАПОМЕНА
ДОГОВОРЕНО СА ИТАЛИЈАНСКОМ АГЕНЦИЈОМ ЗА ДРОГЕ (АИФА)
Април 2013
РЕЛПАКС (Елетриптан хидробромид): Контраиндикације у примени Релпака
Поштовани докторе / Поштовани докторе,
Пфизер, у договору са Италијанском агенцијом за лекове (АИФА), жели да вам скрене пажњу на неке важне безбедносне информације у вези са употребом лека Релпак.
Релпак садржи активну супстанцу Елетриптан хидробромид, селективни агонист васкуларних 5-; ХТ1Б рецептора и неуронских 5-; ХТ1Д рецептора, и одобрен је за акутно лечење фазе главобоље напада мигрене са или без ауре.
Анализирајући случајеве кардиоваскуларних нежељених догађаја, утврђено је да је Релпак био био у више наврата примењивати код пацијената са већ постојећим кардиоваскуларним догађајима код којих је лек контраиндикован.
Од 1. фебруара 2008. до 31. децембра 2012. године, 15 случајева, потврђених од здравствених радника, потврђено је у иностранству са цереброваскуларним догађајима истовремено са употребом елетриптана, од којих је 14 (93%) било тешких случајева. Од 15 случајева, 4 случаја су имала историја контраиндикованог стања или употреба контраиндикованог лека.
Од 1. фебруара 2008. до 31. децембра 2012. године, направљено је 85 извештаја о кардиоваскуларним догађајима који су праћени употребом елетриптана. Од 85 случајева које су здравствени радници потврдили на међународном нивоу, 55 (65%) су били тешки случајеви. Од 85 случајева, 17 случајеви су имали историју контраиндикованих стања и / или употребу контраиндикованих лекова.
Стога се сматра да је потребно скренути пажњу преписивачима да запамте у којим је ситуацијама употреба лека Релпак контраиндикована:
• Преосетљивост на елетриптан хидробромид или било коју помоћну супстанцу;
• Пацијенти са тешком инсуфицијенцијом јетре или бубрега;
• Умерена до тешка хипертензија или нелечена блага хипертензија;
• Пацијенти са документованом коронарном артеријском болешћу, укључујући исхемијску болест срца (ангину пекторис, претходни инфаркт миокарда или документовану тиху исхемију), објективне или субјективне симптоме исхемијске болести срца или Принзметалову ангину;
• Пацијенти са значајним аритмијама или срчаном инсуфицијенцијом;
• Пацијенти са периферном васкулопатијом;
• Пацијенти са претходном епизодом цереброваскуларне несреће (ЦВА) или пролазног исхемијског напада (ТИА);
• Примена ерготамина или деривата ерготамина (укључујући метисергид) у року од 24 сата пре или после третмана елетриптаном.
• Истовремена примена других агониста 5-; ХТ1 рецептора и елетриптана.
Лекари се препоручују да преписују лек Релпак тек након пажљиве процене односа користи и ризика сваког појединачног пацијента, а ни у ком случају никада у ситуацијама када је његова употреба контраиндикована.
Треба запамтити да су контраиндикације лека Релпак према пацијентима са историјом кардиоваскуларних обољења уобичајене за остале триптане на тржишту.
Такође се саветује пажљиво праћење пацијената, посебно на почетку лечења, како би се лечење одмах прекинуло када се појаве први симптоми кардиоваскуларних догађаја.
Лекари и други здравствени радници морају да пријаве сваку сумњу на нежељене реакције
повезан са Релпаком. Лекари и други здравствени радници могу, путем одговарајућег обрасца, одмах послати извештаје о сумњи на нежељене реакције управнику фармаковигиланце здравствене установе којој припадају, који ће их унети у базу података националне мреже фармаковигиланце.
АИФА користи прилику да подсети све лекаре и фармацеуте на важност пријављивања сумњи на нежељене реакције на лекове, као незаменљивог средства за потврђивање повољног односа користи и ризика у реалним условима употребе.
Ова важна информација је такође објављена на веб страници АИФА (ввв.агензиафармацо.ит) чије се редовне консултације препоручују за најбоље стручне и услужне информације грађанима.