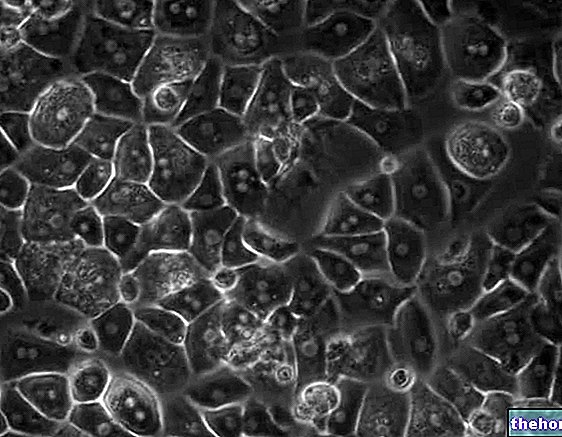
Структура и функције
Хемоглобин је металопротеин садржан у црвеним крвним зрнцима, одговоран за транспорт кисеоника у крвотоку.У ствари, кисеоник је само умерено растворљив у води; стога количине растворене у крви (мање од 2% укупне количине) нису довољне да задовоље метаболичке потребе ткива. Стога је евидентна потреба за посебним превозником.
У крвотоку, кисеоник не може да се директно и реверзибилно веже за протеине, као што се јавља уместо метала као што су бакар и гвожђе. група ЕМЕ, са металним срцем представљеним атомом гвожђа у оксидационом стању Фе2 + (редуковано стање), које везује кисеоник на реверзибилан начин.
Анализа крви
- Нормалне вредности хемоглобина у крви: 13-17 г / 100 мл
Код жена су вредности у просеку 5-10% ниже него код мушкараца.
Могући узроци високог хемоглобина
- Полицитемије
- Продужени боравак на високом терену
- Хроничне плућне болести
- Болест срца
- Допинг крви (употреба еритропоетина и деривата или супстанци које имитирају њихово деловање)
Могући узроци ниског хемоглобина
- Анемија
- Недостатак гвожђа (недостатак гвожђа)
- Обилно крварење
- Карциноми
- Трудноћа
- Тхалассемиас
- Бурнс
Садржај кисеоника у крви је стога дат збрајањем мале количине растворене у плазми са фракцијом везаном за гвожђе хемоглобин.
Више од 98% кисеоника присутног у крви везано је за хемоглобин, који заузврат циркулише у крвотоку распоређеном унутар црвених крвних зрнаца. Без хемоглобина, дакле, еритроцити не би могли да обављају свој задатак као преносиоци кисеоника у крви.
С обзиром на централну улогу овог метала, синтеза хемоглобина захтева одговарајући унос гвожђа у исхрану. Око 70% гвожђа присутног у телу заправо је садржано у хем групама хемоглобина.
Хемоглобин се састоји од 4 подјединице које су структурно врло сличне миоглобину *.
* Док хемоглобин преноси кисеоник из плућа до ткива, миоглобин преноси кисеоник који ослобађа хемоглобин у различите ћелијске органеле које га користе (нпр. Митохондрије).

Хемоглобин је велики и сложен металопротеин, који карактеришу четири глобуларна протеинска ланца омотана око групе хема која садржи Фе2 +.
За сваки молекул хемоглобина стога налазимо четири групе хема омотане у релативни глобуларни ланац протеина. Пошто у сваком молекулу хемоглобина постоје четири атома гвожђа, сваки молекул хемоглобина може везати четири атома кисеоника за себе, у складу са реверзибилном реакцијом:
Хб + 4О2 ← → Хб (О2) 4
Као што је већини познато, задатак хемоглобина је да узме кисеоник у плућима, ослободи га ћелијама којима је то потребно, узме из њих угљен -диоксид и пусти га у плућа где чило поново почиње.
Током проласка крви у капиларама плућних алвеола, хемоглобин везује кисеоник за себе, који се касније ослобађа у ткива у периферној циркулацији. До ове размене долази зато што су везе кисеоника са гвожђем ЕМЕ групе лабилне и осетљиве на многе факторе, од којих је најважнији напетост или парцијални притисак кисеоника.
Везивање кисеоника за хемоглобин и Боров ефекат
У плућима се напетост кисеоника у плазми повећава услед дифузије гаса из алвеола у крв (↑ ПО2); ово повећање узрокује да се хемоглобин жустро веже за кисеоник; супротно се дешава у периферним ткивима, где се смањује концентрација раствореног кисеоника у крви (↓ ПО2) и повећава парцијални притисак угљен -диоксида (↑ ЦО2); ово изазива хемоглобин да ослободи кисеоник и напуни се ЦО2. Поједностављивање концепта што је више могуће, што је више угљен -диоксида присутно у крви, мање кисеоника остаје везано за хемоглобин.
Иако је количина физички раствореног кисеоника у крви врло мала, он игра фундаменталну улогу. У ствари, ова количина значајно утиче на чврстоћу везе између кисеоника и хемоглобина (као и што представља „важну референтну вредност у регулисању плућне вентилације).
Сумирајући све графиконом, количина кисеоника везаног за хемоглобин расте у односу на пО2 следећи сигмоидну криву:

Чињеница да је регион платоа тако велики поставља важну сигурносну границу при максималном засићењу хемоглобина током проласка у плућа. Иако је пО2 на алвеоларном нивоу нормално једнак 100 мм Хг, посматрајући бројку коју заправо примећујемо како чак и парцијални притисак кисеоника једнак 70 ммХг (типична појава неких болести или боравак на великим надморским висинама), проценти засићеног хемоглобина остају близу 100%.
У подручју највећег нагиба, када парцијална напетост кисеоника падне испод 40 ммХг, способност хемоглобина да веже кисеоник нагло опада.
У условима мировања, ПО2 у унутарћелијским течностима је приближно 40 ммХг; на овом месту, услед закона гасова, кисеоник растворен у плазми дифундује према сиромашнијим ткивима О2, прелазећи кроз капиларну мембрану, што доводи до тога да напетост О2 у плазми додатно опада и то погодује ослобађању кисеоника из хемоглобина. . С друге стране, током интензивног физичког напора, напетост кисеоника у ткивима пада на 15 ммХг или мање, услед чега се крв знатно осиромаши кисеоником.
Као што је већ речено, у условима мировања важна количина оксигенираног хемоглобина напушта ткива, која остаје доступна у случају потребе (на пример ради суочавања са наглим повећањем метаболизма у неким ћелијама).
Пуна линија приказана на горњој слици назива се крива дисоцијације хемоглобина; типично се одређује ин витро на пХ 7,4 и на температури од 37 ° Ц.
Боров ефекат има последице како на унос О2 на нивоу плућа, тако и на његово ослобађање на нивоу ткива.
Тамо где има више раствореног угљен -диоксида у облику бикарбоната, хемоглобин лакше ослобађа кисеоник и пуни се угљен -диоксидом (у облику бикарбоната).

Исти ефекат се постиже закисељавањем крви: што се више смањује пХ крви и мање кисеоника остаје везано за хемоглобин; није изненађујуће што се угљен диоксид у крви раствара углавном у облику угљене киселине, која дисоцира.



У част свог откривача, утицај пХ или угљен -диоксида на дисоцијацију кисеоника познат је као Боров ефекат.
Као што се очекивало, у киселом окружењу хемоглобин лакше ослобађа кисеоник, док је у основном окружењу веза са кисеоником јача.

Други фактори који могу да промене афинитет хемоглобина према кисеонику укључују температуру. Конкретно, афинитет хемоглобина према кисеонику опада са повећањем телесне температуре. Ово је посебно повољно током зимских и пролећних месеци, јер температура плућне крви (у контакту са ваздух спољашњег окружења) нижи је од оног који се постиже у ткивима, где се стога олакшава ослобађање кисеоника.

2.3 дифосфоглицерат је међупродукт у гликолизи који утиче на афинитет хемоглобина према кисеонику. Ако се његове концентрације унутар црвених крвних зрнаца повећају, афинитет хемоглобина према кисеонику се смањује, чиме се олакшава ослобађање кисеоника у ткива. Није изненађујуће што концентрације еритроцита 2,3 дифосфоглицерата се повећава, на пример, код анемије, кардио-плућне инсуфицијенције и током боравка на великој надморској висини.
Уопштено, ефекат 2,3 бисфосфоглицерата је релативно спор, посебно у поређењу са брзим одговором на промене пХ, температуре и парцијалног притиска угљен -диоксида.

Боров ефекат је веома важан током интензивног мишићног рада; у таквим условима, заправо, у ткивима која су најизложенија стресу долази до локалног повећања температуре и притиска угљен -диоксида, дакле и киселости крви. Као што је горе објашњено, све ово погодује ослобађању кисеоника у ткива, померајући криву дисоцијације хемоглобина удесно.





.jpg)