Активни састојци: Бортезомиб
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције.
Индикације Зашто се користи Велцаде? За шта је то?
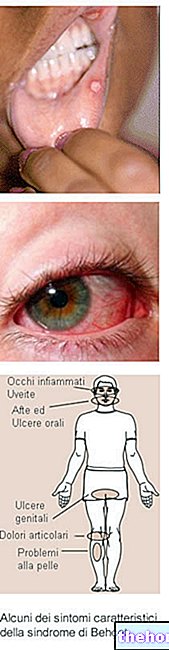
ВЕЛЦАДЕ садржи активну супстанцу бортезомиб, такозвани „инхибитор протеасома“. Протеасоми играју важну улогу у контроли функције и раста ћелија. Ометајући њихову функцију, бортезомиб може убити ћелије рака.
ВЕЛЦАДЕ се користи за лечење мултиплог мијелома (врста малигнитета коштане сржи) код пацијената старијих од 18 година:
- сами или заједно са лековима пегиловани липосомални доксорубицин или дексаметазон, за пацијенте са погоршањем (прогресивне) болести након што су примили најмање један претходни третман или код којих трансплантација матичних ћелија крви није успела или је неизводљива
- у комбинацији са лековима мелфаланом и преднизоном за пацијенте са претходно неизлеченом болешћу који не могу да приме хемотерапију у високим дозама са трансплантацијом матичних ћелија крви.
- у комбинацији са дексаметазоном или дексаметазоном заједно са талидомидом, за пацијенте са претходно нелеченом болешћу и пре него што су примили високу дозу хемотерапије са трансплантацијом матичних ћелија крви (индукциони третман)
ВЕЛЦАДЕ се користи за лечење лимфома ћелија плашта (врста малигнитета који погађа лимфне чворове) код пацијената старијих од 18 година. У овом случају, ВЕЛЦАДЕ се користи у комбинацији са лековима ритуксимаб, циклофосфамид, доксорубицин и преднизон, за пацијенте са претходно неизлеченом болешћу и за које трансплантација матичних ћелија крви није изводљива.
Контраиндикације Када се Велцаде не сме користити
Не користите ВЕЛЦАДЕ
- ако сте алергични на бортезомиб, бор или било који други састојак овог лека (наведен у одељку 6)
- ако имате тешке проблеме са плућима или срцем.
Предострожности при употреби Шта треба да знате пре него што узмете лек Велцаде
Реците свом лекару ако имате:
- низак број црвених крвних зрнаца или белих крвних зрнаца
- проблеми са крварењем и / или низак број тромбоцита у крви
- дијареја, затвор, мучнина или повраћање
- претходна искуства несвестице, вртоглавице или вртоглавице
- проблеми са бубрезима
- умерени до тешки проблеми са јетром
- претходне тегобе као што су утрнулост, трнци или бол у рукама или стопалима (неуропатија)
- поремећај срца или крвног притиска
- отежано дисање или кашаљ
- конвулзије
- шиндре (такође се налазе око очију или се шире по остатку тела)
- симптоми синдрома лизе тумора као што су, на пример, грчеви у мишићима, мишићна слабост, конфузија, поремећен вид или губитак вида и отежано дисање
- губитак памћења, потешкоће у размишљању, потешкоће при ходању или губитак вида. То могу бити знаци озбиљне инфекције мозга, а ваш лекар може да укаже на даље тестове и провере.
Пре и током терапије ВЕЛЦАДЕ -ом мораћете редовно да радите тестове крви да бисте стално проверили вредности крвних зрнаца.
Ако имате лимфом ћелије плашта и узимате ритуксимаб заједно са леком ВЕЛЦАДЕ, морате рећи свом лекару:
- ако мислите да имате хепатитис или сте га раније имали. У неким случајевима, пацијенти који су имали хепатитис Б могу имати нови напад хепатитиса, који може бити и фаталан. Ако сте у прошлости имали инфекцију хепатитисом Б, ваш лекар ће вас морати пажљиво пратити ради знакова и симптома активног хепатитиса Б.
Прочитајте упутства о лековима свих лекова које узимате у комбинацији са ВЕЛЦАДЕ -ом за информације о овим лековима пре почетка лечења ВЕЛЦАДЕ -ом.
Када се ВЕЛЦАДЕ даје заједно са леком талидомид, обратите посебну пажњу на савете о тестирању трудноће и програм превенције трудноће (погледајте „Трудноћа и дојење“ у овом одељку).
Деца и адолесценти
ВЕЛЦАДЕ се не сме користити код деце и адолесцената јер није познато како лек делује код ових особа.
Интеракције Који лекови или храна могу променити ефекат Велцаде -а
Реците свом лекару или фармацеуту ако узимате или сте недавно узимали или бисте могли да узимате било које друге лекове.
Посебно реците свом лекару ако користите лекове који садрже било коју од следећих активних супстанци:
- кетоконазол, који се користи за лечење гљивичних инфекција
- ритонавир, који се користи за лечење ХИВ инфекције - рифампицин, антибиотик који се користи за лечење бактеријских инфекција
- карбамазепин, фенитоин или фенобарбитал, који се користе за лечење епилепсије
- Кантарион (Хиперицум перфоратум), користи се за лечење депресије или других стања
- орални антидијабетички агенси.
Упозорења Важно је знати да:
Трудноћа и дојење
Не бисте смели да користите ВЕЛЦАДЕ ако сте трудни, осим ако је неопходно.
Мушкарци и жене на терапији леком ВЕЛЦАДЕ треба да користе ефикасне методе контрацепције током и до 3 месеца након лечења. Ако упркос овим мерама предострожности затрудните, одмах обавестите свог лекара.
Не би требало да дојите док узимате ВЕЛЦАДЕ. Разговарајте са својим лекаром о најбољем времену за поновно дојење након завршетка терапије.
Лек талидомид изазива урођене мане и смрт фетуса. Када се ВЕЛЦАДЕ примењује истовремено са талидомидом, морате следити програм превенције трудноће са талидомидом (погледајте упутство за употребу талидомида).
Вожња и управљање машинама
ВЕЛЦАДЕ може изазвати умор, вртоглавицу, несвестицу или замагљен вид. Немојте возити аутомобиле или користити машине ако осетите било који од ових симптома. Такође обратите посебну пажњу ако се ови ефекти не појаве.
Доза, начин и време примене Како се користи Велцаде: Дозирање
Ваш лекар ће израчунати дозу ВЕЛЦАДЕ -а сразмерно вашој висини и тежини. Стандардна почетна доза ВЕЛЦАДЕ -а је 1,3 мг / м2 телесне површине два пута недељно. Ваш лекар може да промени дозу и укупан број курсева лечења у зависности од вашег одговора на лечење, појаве одређених нуспојава и општих здравствених стања (нпр. Проблема са јетром).
Мултипли мијелом у прогресији
Када се ВЕЛЦАДЕ даје сам, примит ћете 4 дозе ВЕЛЦАДЕ-а интравенозно или поткожно 1., 4., 8. и 11. дана. Након тога слиједи 10-дневни период "одмора" без лијечења.
Овај период од 21 дана (3 недеље) одговара једном току лечења.
Можете примити до 8 циклуса (24 недеље). Такође можете примити ВЕЛЦАДЕ заједно са лековима за пегиловани липосомални доксорубицин или дексаметазон.
Када се ВЕЛЦАДЕ даје заједно са пегилованим липосомалним доксорубицином, добићете 21-дневни курс интравенског или поткожног ВЕЛЦАДЕ-а и 30 мг / м2 пегилованог липосомалног доксорубицина ће се дати 4. дана 21-дневног циклуса лечења ВЕЛЦАДЕ-ом као инфузија интравенозно након ињекције ВЕЛЦАДЕ -а.
Можете примити до 8 циклуса (24 недеље лечења).
Када се ВЕЛЦАДЕ примењује истовремено са дексаметазоном, добићете 21-дневни курс лечења интравенским или поткожним ВЕЛЦАДЕ-ом и оралним дексаметазоном у дози од 20 мг 1., 2., 4., 5., 8., 9., 11. и 12. дана, 21-дневног курса лечења ВЕЛЦАДЕ-ом.
Можете примити до 8 циклуса (24 недеље лечења).
Раније необрађен мултипли мијелом
Ако се никада раније нисте лечили од мултиплог мијелома и нисте кандидат за трансплантацију крвних матичних ћелија, примићете ВЕЛЦАДЕ заједно са два друга лека: мелфаланом и преднизоном.
У овом случају, терапија траје 42 дана (6 недеља). Добиће 9 циклуса (54 недеље).
- У циклусима 1-4, ВЕЛЦАДЕ се примењује два пута недељно 1., 4., 8., 11., 22., 25., 29. и 32. дана.
- У циклусима 5-9, ВЕЛЦАДЕ се примењује једном недељно 1., 8., 22. и 29. дана.
Мелфалан (9 мг / м2) и преднизон (60 мг / м2) се дају орално 1., 2., 3. и 4. дан прве недеље сваког циклуса.
Ако никада раније нисте били лечени од мултиплог мијелома, а кандидат сте за трансплантацију матичних ћелија крви, примићете ВЕЛЦАДЕ интравенозно или поткожно заједно са лековима: дексаметазоном, или дексаметазоном и талидомидом, као индукцијски третман.
Када се ВЕЛЦАДЕ примењује истовремено са дексаметазоном, добићете 21-дневни курс лечења интравенским или поткожним ВЕЛЦАДЕ-ом и оралним дексаметазоном 40 мг 1., 2., 3., 4., 8., 9., 10. и 11. дана циклуса. -дневни ВЕЛЦАДЕ третман.
Добићете 4 циклуса (12 недеља лечења).
Када се ВЕЛЦАДЕ даје заједно са талидомидом и дексаметазоном, курс лечења траје 28 дана (4 недеље).
Дексаметазон 40 мг се примењује орално 1., 2., 3., 4., 8., 9., 10. и 11. дана 28-дневног циклуса лечења ВЕЛЦАДЕ-ом, а талидомид се даје орално у дози од 50 мг дневно до 14. дана првог циклуса и, ако се толерише, доза талидомида се повећава на 100 мг 15-28 дана, а затим се може повећати до 200 мг дневно од другог циклуса па надаље. Можете примити до 6 циклуса (24 недеље лечења).
Раније необрађен лимфом ћелије плашта
Ако никада раније нисте примали специфичан третман за лимфом ћелије плашта, добићете ВЕЛЦАДЕ интравенозно или поткожно заједно са лековима ритуксимабом, циклофосфамидом, доксорубицином и преднизоном.
ВЕЛЦАДЕ се примењује интравенозно или поткожно 1., 4., 8. и 11. дана, након чега следи период "одмора" без лечења. Трајање курса лечења је 21 дан (3 недеље).
Можете добити до 8 курсева лечења (24 недеље).
Следећи лекови се дају првог дана сваког 21-дневног циклуса лечења ВЕЛЦАДЕ-ом у облику интравенозне инфузије: ритуксимаб при 375 мг / м2, циклофосфамид при 750 мг / м2 и доксорубицин при 50 мг / м2.
Преднизон се примењује орално у дози од 100 мг / м2 1., 2., 3., 4. и 5. дана циклуса третмана ВЕЛЦАДЕ.
Како се даје ВЕЛЦАДЕ
Овај лек је за интравенозну или поткожну употребу. ВЕЛЦАДЕ ће примењивати здравствени радник са искуством у употреби цитотоксичних лекова. Прах ВЕЛЦАДЕ -а мора се растворити пре примене. То ће урадити здравствени радник. Добијени раствор се затим брзо убризгава у вену или поткожно. Л "ињекција у вену је брза, у периоду од 3 до 5 секунди. Поткожна ињекција се може извршити или у бутину или у стомак.
Предозирање Шта учинити ако сте узели превише лека Велцаде
Будући да вам овај лек даје лекар или медицинска сестра, мало је вероватно да ћете узети више него што је потребно. У мало вероватном случају предозирања, ваш лекар ће пратити нежељена дејства.
Нежељени ефекти Који су нежељени ефекти Велцаде -а
Као и сви други лекови, и овај лек може изазвати нежељена дејства, мада се она не морају јавити код свих. Неки од ових ефеката могу бити озбиљни.
Ако сте примили ВЕЛЦАДЕ за мултипли мијелом или лимфом ћелије плашта, одмах обавестите свог лекара ако приметите неки од следећих симптома:
- мишићни грчеви, слабост мишића
- збуњеност, поремећен или губитак вида, слепило, напади, главобоља
- отежано дисање, отицање стопала или промене у откуцајима срца, висок крвни притисак, умор, несвестица
- кашаљ и отежано дисање или стезање у грудима.
Лечење ВЕЛЦАДЕ -ом врло често може изазвати смањење броја црвених и белих крвних зрнаца и крвних плочица. Због тога ћете пре и током лечења леком ВЕЛЦАДЕ морати редовно да радите тестове крви како бисте редовно проверили број крвних зрнаца. Можда ћете доживети смањење броја:
- тромбоцити, који би вас могли учинити склонијим модрицама или крварењу без приметних повреда (на пример, крварење у цревима, желуцу, устима и деснима или крварење у мозгу или јетри)
- црвена крвна зрнца, која могу изазвати анемију, са симптомима као што су умор и бледило
- бела крвна зрнца, што вас може учинити подложнијим инфекцијама или симптомима сличним грипу.
Ако сте добили ВЕЛЦАДЕ за лечење мултиплог мијелома, доњи споредни ефекти који се могу јавити су наведени испод.
Веома чести нежељени ефекти (могу се јавити код више од 1 на 10 особа)
- Преосетљивост, утрнутост, пецкање или пецкање коже или бол у шакама или стопалима због оштећења нерва.
- Смањење броја црвених и / или белих крвних зрнаца (види горе).
- Грозница.
- Осећај мучнине или повраћања, губитак апетита.
- Затвор са или без вишка гасова (може бити озбиљан).
- Пролив: ако се то догоди, важно је да пијете много више воде него обично. Ваш лекар може прописати лекове за контролу дијареје.
- Умор (умор), осећај слабости.
- Бол у мишићима, бол у костима.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа)
- Низак крвни притисак, нагли пад крвног притиска у стојећем положају што може довести до несвестице.
- Повећан крвни притисак.
- Смањена функција бубрега.
- Главобоља.
- Опште лоше осећање, бол, вртоглавица, вртоглавица, осећај слабости или губитак свести.
- Зимица.
- Инфекције, укључујући упалу плућа, респираторне инфекције, бронхитис, гљивичне инфекције, кашаљ са слузи, болести сличне грипу.
- Херпес зостер инфекција (локализована, укључујући око очију, или се шири по телу).
- Бол у грудима или отежано дисање током физичке активности.
- Различите врсте осипа на кожи (осип).
- Свраб коже, грудвице на кожи или сува кожа.
- Црвенило лица или мали ломови у капиларама.
- Црвенило коже.
- Дехидрација.
- Жгаравица, надутост, подригивање, гасови, болови у стомаку, цревно или желудачно крварење.
- Промена функције јетре.
- Иритација уста или усана, сува уста, чиреви у устима или грлобоља.
- Губитак тежине, губитак укуса.
- Грчеви у мишићима, грчеви мишића, мишићна слабост, бол у рукама и ногама.
- Замагљен вид.
- Инфекција најудаљенијег слоја очију и унутрашње површине капака (коњунктивитис).
- Крварење из носа (крварење).
- Поремећаји или проблеми са спавањем, знојење, анксиозност, промене расположења, депресивно расположење, немир или узнемиреност, промене менталног статуса, дезоријентација.
- Отицање тела, укључујући отицање око очију и других делова тела.
Мање чести нежељени ефекти (могу се јавити у до 1 на 100 људи)
- Срчана инсуфицијенција, срчани удар, бол у грудима, нелагодност у грудима, повећан или смањен број откуцаја срца.
- Инсуфицијенција бубрега.
- Упала вене, крвни угрушци у венама и плућима.
- Проблеми са згрушавањем крви.
- Кршење циркулације.
- Упала мембране која окружује срце или присуство течности око срца.
- Инфекције укључујући инфекције уринарног тракта, грип, инфекције вирусом херпеса, инфекције уха и целулитис.
- Крв у столици или крварење слузокоже, на пример уста, вагине.
- Цереброваскуларни поремећаји.
- Парализа, конвулзије, пад, поремећаји кретања, абнормална, промењена или смањена осетљивост (осећај, слух, укус, мирис), поремећај пажње, тремор, грчеви.
- Артритис, укључујући упалу зглобова прстију, прстију и вилице.
- Поремећаји који утичу на плућа, спречавајући ваше тело да добије довољно кисеоника. Неки од њих укључују отежано дисање, отежано дисање, тешко дисање чак и без физичке активности, потешкоће у плитком дисању или потребу за престанком, пискање.
- Штуцање, поремећаји говора.
- Повећана или смањена производња урина (оштећење бубрега), болно мокрење или крв / протеини у урину, задржавање течности.
- Промењени нивои свести, конфузија, оштећење или губитак памћења.
- Преосетљивост.
- Губитак слуха, глувоћа или зујање у ушима, нелагодност у уху.
- Хормонске промене које могу утицати на реапсорпцију соли и воде.
- Хиперактивност штитне жлезде.
- Немогућност производње довољне количине инсулина или отпорност на нормалне нивое инсулина.
- Болне или упаљене очи, прекомерно влажне очи, бол у очима, суво око, инфекције ока, исцједак из очију, сметње вида, крварење из ока.
- Повећани лимфни чворови.
- Укоченост зглобова или мишића, осећај тежине, бол у препонама.
- Губитак косе или абнормална текстура косе.
- Алергијске реакције.
- Црвенило или бол на месту убризгавања.
- Бол у устима.
- Инфекција или упала уста, чиреви у устима, једњаку, желуцу и цревима понекад повезани са болом или крварењем, поремећена покретљивост црева (укључујући и блокаду црева), нелагодност у трбуху или једњаку, отежано гутање, повраћање крви.
- Инфекције коже.
- Бактеријске и вирусне инфекције.
- Инфекција зуба.
- Упала панкреаса, опструкција жучних канала.
- Бол у гениталијама, проблеми са ерекцијом.
- Добијање на тежини.
- Осећате жеђ.
- Хепатитис.
- Поремећаји на месту убризгавања или на месту катетера.
- Кожне реакције или поремећаји (који могу бити озбиљни и опасни по живот), улцерације на кожи.
- Модрице, падови и повреде.
- Упала или крварење крвних судова које се могу манифестовати као мале црвене или љубичасте тачке (обично на ногама) које могу постати сличне великим модрицама на кожи или ткиву.
- Бенигне цисте.
- Озбиљно и реверзибилно стање мозга које укључује нападе, висок крвни притисак, главобољу, умор, збуњеност, слепило или друге проблеме са видом.
Ретки нежељени ефекти (могу се јавити у до 1 на 1.000 људи)
- Срчани проблеми укључујући срчани удар, ангину пекторис.
- Флусхес.
- Промена боје вена.
- Запаљење кичменог нерва.
- Проблеми са ушима, крварење из уха.
- Смањена активност штитне жлезде.
- Будд-Цхиаријев синдром (клинички знаци су узроковани зачепљењем вена јетре).
- Промена или абнормална функција црева.
- Церебрално крварење (крварење).
- Жута промена боје очију и коже (жутица).
- Знаци тешке алергијске реакције (анафилактички шок) укључују отежано дисање, бол у грудима или стезање у грудима, и / или осећај вртоглавице / слабости, јак свраб коже или грудвице на кожи, отицање лица, усана, језика и / или грла тешкоће при гутању, колапс.
- Поремећаји груди.
- Вагинални исцједак.
- Отицање гениталија.
- Немогућност толерисања конзумирања алкохола.
- Губитак или губитак телесне масе.
- Повећан апетит.
- Фистуле.
- Заједнички излив.
- Циста на мембрани која прекрива зглобове (синовијалне цисте).
- Преломи.
- Распад мишићних влакана доводи до других компликација.
- Повећана јетра, крварење у јетри.
- Рак бубрега.
- Стање коже слично псоријази.
- Рак коже.
- Бледица коже.
- Повећање тромбоцита или плазма ћелија (врста белих крвних зрнаца) у крви.
- Абнормална реакција на трансфузију крви.
- Делимичан или потпуни губитак вида.
- Смањен либидо.
- Губитак пљувачке.
- Избочење очију.
- Фотофобија (прекомерна осетљивост ока на светлост).
- Убрзано дисање.
- Бол у ректуму.
- Жучни каменци.
- Херниа.
- Повреде.
- Крхки или слаби нокти.
- Абнормално таложење протеина у виталним органима.
- Кома.
- Чиреви на цревима.
- Оштећење више органа.
- Смрт.
Ако сте добили ВЕЛЦАДЕ заједно са другим лековима за лечење лимфома ћелија плашта, нежељени ефекти који се могу јавити наведени су у наставку.
Веома чести нежељени ефекти (могу се јавити код више од 1 на 10 особа)
- Упала плућа.
- Губитак апетита.
- Преосетљивост, утрнутост, пецкање или пецкање коже или бол у шакама или стопалима због оштећења нерва.
- Мучнина и повраћање.
- Пролив.
- Чиреви у устима.
- Цревни затвор.
- Бол у мишићима, бол у костима.
- Губитак косе или абнормална текстура косе.
- Умор, осећај слабости.
- Грозница.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа)
- Херпес зостер инфекција (локализована, укључујући око очију или се шири по телу).
- Инфекција вирусом херпеса.
- Бактеријске и вирусне инфекције.
- Респираторне инфекције, бронхитис, кашаљ са слузи, болест слична грипу.
- Гљивичне инфекције.
- Преосетљивост (алергијска реакција).
- Немогућност производње довољне количине инсулина или отпорност на нормалне нивое инсулина.
- Задржавање воде.
- Потешкоће или проблеми са спавањем.
- Губитак свести.
- Промењени ниво свести, конфузија.
- Врти ми се у глави.
- Повећан број откуцаја срца, висок крвни притисак, знојење.
- Поремећаји вида, замагљен вид.
- Срчана инсуфицијенција, срчани удар, бол у грудима, нелагодност у грудима, повећан или смањен број откуцаја срца.
- Висок или низак крвни притисак.
- Нагли пад крвног притиска у стојећем положају што може довести до несвестице.
- Краткоћа даха током физичке активности.
- Кашаљ.
- Штуцање.
- Зујање у ушима, нелагодност у уху.
- Цревно или желучано крварење.
- Бол у стомаку.
- Бол у стомаку, надутост.
- Потешкоће при гутању.
- Инфекција или упала желуца и црева.
- Бол у стомаку.
- Иритација уста или усана, грлобоља.
- Промена функције јетре.
- Свраба коже.
- Црвенило коже.
- Осип.
- Грчење мишића.
- Инфекција уринарног тракта.
- Бол у удовима.
- Отицање тела, укључујући отицање око очију и других делова тела.
- Зимица.
- Црвенило и бол на месту убризгавања.
- Осећај опште слабости.
- Губитак телесне тежине.
- Повећање телесне тежине.
Мање чести нежељени ефекти (могу се јавити у до 1 на 100 људи)
- Хепатитис.
- Тешка алергијска реакција (анафилактичка реакција) чији знаци могу укључивати отежано дисање, бол у грудима или стезање у грудима, и / или осећај вртоглавице / слабости, јак свраб коже или грудвице на кожи, отицање лица, усана, језика и / или грло које може изазвати потешкоће при гутању, колапс.
- Поремећаји покрета, парализа, контракције.
- Вртоглавица.
- Губитак слуха, глувоћа.
- Поремећаји који утичу на плућа, спречавајући ваше тело да добије довољно кисеоника. Неки од њих укључују отежано дисање, недостатак даха, пискање чак и без физичке активности, дисање које постаје плитко, отежано или престаје, пискање.
- Крвни угрушци у плућима.
- Жута промена боје очију и коже (жутица).
Пријављивање нежељених ефеката
Ако приметите било које нежељено дејство, обратите се свом лекару или фармацеуту.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нежељена дејства директно путем националног система за пријављивање наведеног у Додатку В. Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока ваљаности наведеног на бочици и кутији иза ознаке „Рок употребе“.
Чувати на температури која не прелази 30 ° Ц. Бочицу чувајте у спољном паковању ради заштите лека од светлости.
Реконституисани раствор треба користити одмах након припреме. Ако се реконституисани раствор не употреби одмах, услови и време употребе су одговорност приправљача. Међутим, реконституисани раствор је стабилан 8 сати на 25 ° Ц пре примене када се чува у оригиналној бочици и / или у шприцу, са максималним временом чувања реконституисаног лека не више од 8 сати.
ВЕЛЦАДЕ је само за једнократну употребу. Неискоришћени производ и отпад морају се одложити у складу са важећим локалним прописима.
Рок "> Остале информације
Шта ВЕЛЦАДЕ садржи
- Активни састојак је бортезомиб. Свака бочица садржи 3,5 мг бортезомиба (као борни естар манитола). Након реконституције, 1 мл раствора за ињекције садржи 1 мг бортезомиба.
- Помоћни састојци су манитол (Е421) и азот.
Реконституција за интравенозну употребу: Након реконституције, 1 мл раствора за интравенозну ињекцију садржи 1 мг бортезомиба.
Реконституција за поткожну употребу: Након реконституције, 1 мл раствора за поткожну ињекцију садржи 2,5 мг бортезомиба.
Опис изгледа ВЕЛЦАДЕ -а и садржај паковања
ВЕЛЦАДЕ прашак за раствор за ињекције је беле до кремасто беле боје.
Свако паковање ВЕЛЦАДЕ 3,5 мг садржи 1 стаклену бочицу од 10 мл са плавим поклопцем, која се налази у провидном блистеру.
Рок "> Информације за здравствене раднике
Следеће информације су намењене само здравственим радницима
ОБНОВА ЗА ИНТРАВЕНО УБРИЗГАВАЊЕ
Напомена: ВЕЛЦАДЕ је цитотоксично средство. Сходно томе, током руковања и припреме потребно је обратити посебну пажњу. Препоручује се ношење рукавица и друге заштитне одеће како би се спречио контакт са кожом.
ЗБОГ ОДСУСТВА БИЛО КОЈЕ ВРСТЕ КОНЗЕРВАТИВА, АСЕПТИЧКИ ТЕХНИЧКИ СТАНДАРДИ МОРАЈУ БИТИ ПОТРЕБНИ ТОКОМ РУКОВАЊА ВЕЛЦАДЕ -ом.
- Припрема бочице од 3,5 мг: Додајте 3,5 мл стерилног раствора натријум хлорида 9 мг / мл (0,9%) за ињекцију у бочицу која садржи прах ВЕЛЦАДЕ. Лиофилизовани прах се потпуно раствара за мање од 2 минута.
Концентрација добијеног раствора је једнака 1 мг / мл. Раствор ће бити бистар и безбојан са коначним пХ између 4 и 7. Није потребно проверавати пХ раствора.
- Раствор треба визуелно прегледати пре примене како би се проверило да ли постоје честице или промена боје.У присуству честица или промене боје, раствор се не сме користити и треба га одбацити.
Потврдите концентрацију на бочици како бисте били сигурни да се тачна доза даје интравенозно (1 мг / мл).
- Реконституисани раствор не садржи конзервансе и треба га користити одмах након припреме, док је хемијски и физички стабилан 8 сати на 25 ° Ц у оригиналној бочици и / или у шприцу са највише 8 сати у шприцу. Укупно време складиштења реконституисаног лека не може бити дуже од 8 сати пре примене. Ако се реконституисани раствор не користи одмах након припреме, одговорност је корисника да се придржава услова складиштења производа и времена пре употребе.
Није потребно заштитити реконституисани лек од светлости.
АДМИНИСТРАЦИЈА
- Када се раствори, повуците одговарајућу количину реконституисаног раствора у складу са дозом израчунатом на основу површине тела пацијента.
- Пре употребе потврдите дозу и концентрацију у шприцу (проверите да ли је шприц означен за интравенозну примену).
- Ињектирајте раствор интравенозно као болус од 3-5 секунди, кроз периферни или централни интравенозни катетер.
- Исперите интравенозни катетер стерилним раствором за ињекције натријум хлорида 9 мг / мл (0,9%).
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције је за субкутану или интравенску употребу. Немојте давати другим путевима. Интратекална администрација довела је до смрти.
ОДЛАГАЊЕ
Бочица је само за једнократну употребу, а преостали раствор треба одбацити.
Неискоришћени лек и отпад из овог лека треба одложити у складу са локалним прописима.
Следеће информације су намењене само здравственим радницима:
Само бочица од 3,5 мг може се примењивати поткожно као што је доле описано.
ОБНОВА ЗА СУБКУТАНО УБРИЗГАВАЊЕ
Напомена: ВЕЛЦАДЕ је цитотоксично средство. Сходно томе, током руковања и припреме потребно је обратити посебну пажњу. Препоручује се ношење рукавица и друге заштитне одеће како би се спречио контакт са кожом.
ЗБОГ ОДСУСТВА БИЛО КОЈЕ ВРСТЕ КОНЗЕРВАТИВА, АСЕПТИЧКИ ТЕХНИЧКИ СТАНДАРДИ МОРАЈУ БИТИ ПОТРЕБНИ ТОКОМ РУКОВАЊА ВЕЛЦАДЕ -ом.
- Припрема бочице од 3,5 мг: Додајте 1,4 мл стерилног раствора натријум хлорида 9 мг / мл (0,9%) за ињекције у бочицу која садржи прах ВЕЛЦАДЕ. Лиофилизовани прах се потпуно раствара за мање од 2 минута.
Концентрација добијеног раствора је једнака 2,5 мг / мл. Раствор ће бити бистар и безбојан са коначним пХ између 4 и 7. Није потребно проверавати пХ раствора.
- Раствор треба визуелно прегледати пре примене како би се проверило да ли постоје честице или промена боје.У присуству честица или промене боје, раствор се не сме користити и треба га одбацити.
Потврдите концентрацију на бочици како бисте били сигурни да се тачна доза примењује поткожно (2,5 мг / мл).
- Реконституисани раствор не садржи конзервансе и треба га користити одмах након припреме, док је хемијски и физички стабилан 8 сати на 25 ° Ц у оригиналној бочици и / или у шприцу са највише 8 сати у шприцу. Укупно време складиштења реконституисаног лека не може бити дуже од 8 сати пре примене. Ако се реконституисани раствор не користи одмах након припреме, одговорност је корисника да се придржава услова складиштења производа и времена пре употребе.
Није потребно заштитити реконституисани лек од светлости.
АДМИНИСТРАЦИЈА
- Када се раствори, повуците одговарајућу количину реконституисаног раствора у складу са дозом израчунатом на основу површине тела пацијента.
- Пре употребе потврдите дозу и концентрацију у шприцу (проверите да ли је шприц означен за субкутану примену).
- Ињектирајте раствор поткожно, под углом од 45-90 °
- Реконституисани раствор се примењује поткожно у бутине (десно или лево) или стомак (десно или лево)
- У наредним применама потребно је мењати место убризгавања у ротацији.
- Ако дође до локалних реакција на месту убризгавања након поткожне ињекције ВЕЛЦАДЕ -а, може се применити нижа концентрација 3,5 мг раствора ВЕЛЦАДЕ -а (1 мг / мл уместо 2,5 мг / мл) или се препоручује прелазак на „интравенозну ињекцију.
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције је за субкутану или интравенску употребу. Немојте давати другим путевима. Интратекална администрација довела је до смрти.
ОДЛАГАЊЕ
Бочица је само за једнократну употребу, а преостали раствор треба одбацити.
Неискоришћени лек и отпад из овог лека треба одложити у складу са локалним прописима.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА -
ВЕЛЦАДЕ 3,5 МГ прах за раствор за ињекције
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ -
Свака бочица садржи 3,5 мг бортезомиба (као борни естар манитола).
Након реконституције, 1 мл раствора за ињекције за поткожну примену садржи 2,5 мг бортезомиба.
Након реконституције, 1 мл раствора за ињекције за интравенозну примену садржи 1 мг бортезомиба.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК -
Прашак за раствор за ињекције.
Бели до кремасти бели прах (сабијен или не).
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ -
04.1 Терапијске индикације -
ВЕЛЦАДЕ као монотерапија или у комбинацији са пегилованим липосомским доксорубицином или дексаметазоном је индикован за лечење одраслих пацијената са прогресивним мултиплим мијеломом који су већ примили најмање једну претходну линију лечења и који су већ прошли или нису подобни за трансплантацију матичних ћелија. .
ВЕЛЦАДЕ у комбинацији са мелфаланом и преднизоном је индикован за лечење одраслих пацијената са претходно нелеченим мултиплим мијеломом који нису подобни за хемотерапију високим дозама са трансплантацијом крвотворних матичних ћелија.
ВЕЛЦАДЕ у комбинацији са дексаметазоном или са дексаметазоном и талидомидом је индикован за индукционо лечење одраслих пацијената са претходно нелеченим мултиплим мијеломом који испуњавају услове за хемотерапију у високим дозама са трансплантацијом крвотворних матичних ћелија.
ВЕЛЦАДЕ у комбинацији са ритуксимабом, циклофосфамидом, доксорубицином и преднизоном је индикован за лечење одраслих пацијената са претходно нелеченим лимфомом плаштних ћелија који нису подобни за трансплантацију хематопоетских матичних ћелија.
04.2 Дозирање и начин примене -
Лечење треба започети и спровести под надзором лекара обученог и искусног у употреби хемотерапеутских агенаса.ВЕЛЦАДЕ треба да реконструише здравствени радник.
Дозирање за лечење прогресивног мултиплог мијелома (пацијенти који су примили најмање једну претходну линију лечења)
Монотерапија
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље током 1., 4., 8. и 11. дана у једном 21 -дневном циклусу третмана Овај период од 3 недеље сматра се циклусом лечења.
Препоручује се да пацијенти добију 2 курса ВЕЛЦАДЕ -а након потврде да је постигнут потпуни одговор.
Пацијентима који реагују на лечење, али не постигну потпуну ремисију, препоручује се да примене укупно 8 курсева ВЕЛЦАДЕ -а.
Требало би да прође најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
Прилагођавање дозе током лечења и наставак као монотерапија
Терапију ВЕЛЦАДЕ-ом треба прекинути на почетку било које нехематолошке токсичности степена 3 или било које хематолошке токсичности степена 4, искључујући неуропатију, како је доле назначено (видети такође одељак 4.4). Токсичност, лечење ВЕЛЦАДЕ-ом се може наставити са 25% нижом дозом ( 1,3 мг / м² смањен на 1,0 мг / м²; 1,0 мг / м² смањен на 0,7 мг / м²) .у случају да симптоми токсичности нису нестали, или ако се понове при смањеној дози, треба размотрити прекид терапије леком ВЕЛЦАДЕ, осим ако нема користи терапије јасно надмашују ризике.
Неуропатски бол и / или периферна неуропатија
Пацијенте код којих се јави неуропатски бол повезан са бортезомибом и / или периферна неуропатија треба лечити према Табели 1 (видети одељак 4.4).
Пацијенти са већ постојећом тешком неуропатијом могу се лечити леком ВЕЛЦАДЕ само након „пажљиве процене ризика / користи“.
Табела 1: Препоручене модификације дозе * у случају неуропатије повезане са применом бортезомиба
Комбинована терапија са пегилованим липосомалним доксорубицином
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље током 1., 4., 8. и 11. дана у једном циклусу од 21 дана Овај период од 3 недеље сматра се циклусом лечења Треба проћи најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
Пегиловани липосомални доксорубицин се примењује у дози од 30 мг / м² 4. дана циклуса третмана ВЕЛЦАДЕ у облику интравенозне инфузије која траје 1 сат након ињекције ВЕЛЦАДЕ -а.
Може се применити до 8 циклуса ове комбиноване терапије све док пацијенти не покажу прогресију и не толеришу лечење. Пацијенти који постигну потпуни одговор могу наставити лечење најмање 2 циклуса након првих доказа потпуног одговора, чак и ако то захтева лечење дуже од 8 циклуса. Пацијенти код којих ниво парапротеина наставља да опада након 8 циклуса, могу наставити терапију све док се лечење толерише и настави да показује одговор.
За додатне информације о пегилованом липосомалном доксорубицину, погледајте одговарајући Сажетак карактеристика производа.
Комбинација са дексаметазоном
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље током 1., 4., 8. и 11. дана у једном циклусу од 21 дана Овај период од 3 недеље сматра се циклусом лечења Треба проћи најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
Дексаметазон се примењује орално у дози од 20 мг 1., 2., 4., 5., 8., 9., 11. и 12. дана циклуса лечења ВЕЛЦАДЕ.
Пацијенти који постигну одговор на болест или стабилизацију након 4 циклуса ове комбиноване терапије могу наставити да примају исту комбинацију до 4 додатна циклуса.
За додатне информације у вези са дексаметазоном, погледајте одговарајући Сажетак карактеристика производа.
Прилагођавање дозе за комбиновану терапију код пацијената са прогресивним мултиплим мијеломом
За прилагођавање дозе ВЕЛЦАДЕ -а у комбинованој терапији, следите препоруке за модификацију дозе описане у горњем одељку о монотерапији.
Дозирање за лечење претходно нелеченог мултиплог мијелома код пацијената који нису подобни за високу дозу хемотерапије са трансплантацијом хематопоетских матичних ћелија.
Комбинована терапија са мелфаланом и преднизоном
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у комбинацији са оралним мелфаланом и оралним преднизоном како је наведено у Табели 2. Период од 6 недеља сматра се током лечења. У циклусима 1-4 ВЕЛЦАДЕ се даје два пута недељно у данима 1, 4, 8, 11, 22, 25, 29 и 32. У циклусима 5-9 ВЕЛЦАДЕ се даје једном недељно у данима 1, 8, 22 и 29. Требало би да прође најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
И мелфалан и преднизон треба примењивати орално 1., 2., 3. и 4. дан прве недеље сваког циклуса лечења ВЕЛЦАДЕ -ом. Примењује се 9 циклуса лечења ове комбиноване терапије.
Табела 2: Распоред препоручених доза ВЕЛЦАДЕ -а у комбинацији са мелфаланом и преднизоном
Прилагођавање дозе током лечења и његов наставак у комбинацији са мелфаланом и преднизоном
Пре почетка новог курса терапије:
• број тромбоцита треба да буде ≥ 70 к 109 / Л, а апсолутни број неутрофила (АНЦ) ≥ 1,0 к 109 / Л
• Нехематолошке токсичности морале су се смањити на степен 1 или на почетну вредност
Табела 3: Промене у дозирању током наредних курсева терапије ВЕЛЦАДЕ -ом у комбинацији са мелфаланом и преднизоном
За више информација у вези с мелфаланом и преднизоном, погледајте њихове сажетке карактеристика производа.
Дозирање за лечење претходно нездрављеног мултиплог мијелома код пацијената који испуњавају услове за трансплантацију хематопоетских матичних ћелија (индукциона терапија).
Комбинована терапија са дексаметазоном
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље у току 1., 4., 8. и 11. дана у једном циклусу од 21 дана Овај период од 3 недеље сматра се циклусом лечења Треба проћи најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
Дексаметазон се примењује орално у дози од 40 мг 1., 2., 3., 4., 8., 9., 10. и 11. дана циклуса лечења ВЕЛЦАДЕ.
Спроводе се четири циклуса лечења ове комбиноване терапије.
Комбинована терапија са талидомидом и дексаметазоном
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље током 1., 4., 8. и 11. дана у једном циклусу третмана од 28 дана Овај период од 4 недеље сматра се циклусом лечења.
Требало би да прође најмање 72 сата између примене две узастопне дозе ВЕЛЦАДЕ -а.
Дексаметазон се примењује орално у дози од 40 мг 1., 2., 3., 4., 8., 9., 10. и 11. дана циклуса лечења ВЕЛЦАДЕ.
Талидомид се примењује орално у дневној дози од 50 мг у данима 1-14; ако се толерише, доза се повећава на 100 мг 15-28 дана, а затим се може додатно повећати на 200 мг дневно од 2. циклуса (видети Табелу 4).
Спроводе се четири циклуса лечења ове комбиноване терапије.
За пацијенте који постигну барем делимичан одговор, препоручују се додатна 2 курса лечења.
Табела 4: Дозирање комбиноване терапије са ВЕЛЦАДЕ -ом за лечење претходно нездрављеног мултиплог мијелома код пацијената подобних за трансплантацију хематопоетских матичних ћелија.
Прилагођавање дозе кандидатима за трансплантацију
За прилагођавање дозе ВЕЛЦАДЕ -а за неуропатију, погледајте Табелу 1.
Осим тога, када се ВЕЛЦАДЕ примењује у комбинацији са другим хемотерапеутским агенсима, потребно је размотрити одговарајуће смањење дозе ових лекова у случају токсичности према препорукама у одговарајућем Сажетку карактеристика производа.
Дозирање за пацијенте са претходно нелеченим лимфомом ћелија плашта (МЦЛ)
Комбинована терапија са ритуксимабом, циклофосфамидом, доксорубицином и преднизоном (ВцР-ЦАП)
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције се примењује интравенозно или поткожно у препорученој дози од 1,3 мг / м² телесне површине два пута недељно током две недеље, 1., 4., 8. и 11. дана, након чега следи дан одмора од 10 дана 12 до 21. Овај период од 3 недеље сматра се током лечења Најмање 72 сата би требало да прође између примене две узастопне дозе ВЕЛЦАДЕ -а.
Препоручује се 6 циклуса лечења овом комбинованом терапијом. Пацијентима са документованим првим одговором на циклус 6 могу се дати 2 додатна курса лечења.
Следећи лекови се дају као интравенозна инфузија првог дана сваког тронедељног циклуса лечења ВЕЛЦАДЕ-ом: ритуксимаб у дози од 375 мг / м², циклофосфамид у дози од 750 мг / м² и доксорубицин у дози од 50 мг / м².
Преднизон се примењује орално у дози од 100 мг / м² 1., 2., 3., 4. и 5. дана сваког циклуса третмана са ВЕЛЦАДЕ -ом.
Прилагођавање дозе током лечења пацијената са претходно нелеченим МЦЛ
Пре почетка новог курса терапије:
• Број тромбоцита мора бити ≥ 100.000 ћелија / мцЛ, а апсолутни број неутрофила (АНЦ) мора бити ≥ 1.500 ћелија / мцЛ
• Број тромбоцита треба да буде ≥ 75.000 ћелија / мцЛ код пацијената са инфилтрацијом коштане сржи или секвестрацијом слезине
• Хемоглобин мора бити ≥ 8 г / дЛ
• Нехематолошке токсичности треба смањити на степен 1 или на почетну вредност.
Лечење ВЕЛЦАДЕ-ом треба прекинути на почетку било које степене ≥ 3 нехематолошке токсичности повезане са ВЕЛЦАДЕ (искључујући неуропатију) или степена ≥ 3 хематолошке токсичности (видети такође одељак 4.4). За прилагођавање дозе видети Табелу 5 испод.
У случају хематолошке токсичности, фактори раста гранулоцита могу се применити у складу са локалном стандардном праксом. Требало би размотрити превентивну употребу фактора раста гранулоцита у случају поновљених одлагања у спровођењу курсева терапије.Када је то клинички прикладно, треба размотрити трансфузију тромбоцита за лечење тромбоцитопеније.
Табела 5: Прилагођавање дозе током лечења пацијената са претходно нелеченим МЦЛ
Осим тога, када се ВЕЛЦАДЕ примењује у комбинацији са другим хемотерапеутским агенсима, "потребно је размотрити одговарајуће смањење дозе ових лекова у случају токсичности, према препорукама садржаним у одговарајућем Сажетку карактеристика производа".
Посебне популације
Старији пацијенти
Нема клиничких доказа који указују на потребу прилагођавања дозе код пацијената старијих од 65 година са мултиплим мијеломом или лимфомом ћелија плашта.
Не постоје студије о употреби ВЕЛЦАДЕ-а код старијих пацијената са претходно нелеченим мултиплим мијеломом који су кандидати за хемотерапију високим дозама са трансплантацијом хематопоетских матичних ћелија.
Због тога се у овој популацији не могу дати препоруке о дозама.
У студији на претходно нелеченим пацијентима са лимфомом ћелија плашта, 42,9% и 10,4% пацијената изложених ВЕЛЦАДЕ-у били су у распону од 65-74 године, односно ≥ 75 година. Код пацијената старијих од 75 година, оба режима, ВЕЛЦАДЕ у комбинацији са ритуксимабом, циклофосфамидом, доксорубицином и преднизоном (ВцР-ЦАП) и ритуксимабом, циклофосфамидом, доксорубицином, винкристином и преднизоном (Р-ЦХОП), били су мање подношљиви (видети параграф 8) ).
Дисфункција јетре
Пацијентима са благим оштећењем јетре није потребно прилагођавање дозе и треба их лечити препорученом дозом.Пацијенти са умереним или тешким оштећењем јетре треба да започну лечење ВЕЛЦАДЕ -ом у смањеној дози од 0,7 мг / м² по ињекцији током првог циклуса лечења, а касније повећање дозе на 1,0 мг / м² или даље смањење дозе на 0,5 мг / м² треба узети у обзир на основу толеранције пацијената (видети Табелу 6 и одељке 4.4 и 5.2).
Табела 6: Препоручене почетне дозе ВЕЛЦАДЕ -а за пацијенте са оштећењем јетре
Дисфункција бубрега
На фармакокинетику бортезомиба нема утицаја код пацијената са благим до умереним оштећењем бубрега (клиренс креатинина [ЦрЦЛ]> 20 мл / мин / 1,73 м²); стога није потребно прилагођавање дозе код ових пацијената. Није познато да ли је фармакокинетика бортезомиба промењена код пацијената са тешким оштећењем бубрега који нису на дијализи (ЦрЦЛ
Педијатријска популација
Безбедност и ефикасност лека ВЕЛЦАДЕ код пацијената млађих од 18 година нису утврђени (видети одељке 5.1 и 5.2). Нема података.
Начин примене
ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције намењен је за интравенозну или поткожну примену.
ВЕЛЦАДЕ 1 мг прашак за раствор за ињекције служи само за интравенозну примену.
ВЕЛЦАДЕ се не сме примењивати другим путевима. Интратекална администрација је изазвала смрт.
Интравенозна ињекција
Реконституисани раствор ВЕЛЦАДЕ 3,5 мг се примењује интравенозно као болус од 3-5 секунди, преко периферног или централног интравенозног катетера, након чега следи испирање са 9 мг / мл натријум хлорида (0,9%). Између две узастопне дозе ВЕЛЦАДЕ -а требало би да прође најмање 72 сата.
Поткожна ињекција
Реконституисани раствор лека ВЕЛЦАДЕ 3,5 мг се примењује поткожно у бутине (десно или лево) или стомак (десно или лево). Раствор се убризгава поткожно под углом од 45-90 °.
Места убризгавања морају се мењати у ротацији за наредне ињекције.
Ако дође до реакције на месту убризгавања након поткожне примене ВЕЛЦАДЕ -а, може се применити поткожно мање концентрисан раствор ВЕЛЦАДЕ -а (ВЕЛЦАДЕ 3,5 мг реконституисан у 1 мг / мл уместо у 2,5 мг / мл) или се препоручује прелазак на интравенозну примену.
Када се ВЕЛЦАДЕ примењује у комбинацији са другим лековима, упутства о примени потражите у Сажетку карактеристика ових лекова.
04.3 Контраиндикације -
Преосетљивост на активну супстанцу, бор или било коју помоћну супстанцу наведену у одељку 6.1.
Акутна дифузна инфилтративна плућна болест и перикардиопатија.
Када се ВЕЛЦАДЕ примењује у комбинацији са другим лековима, додатне релевантне контраиндикације потражите у одговарајућем Сажетку карактеристика производа.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби -
Када се ВЕЛЦАДЕ примењује у комбинацији са другим лековима, пре почетка лечења леком ВЕЛЦАДЕ треба консултовати одговарајући Сажетак карактеристика лека. Посебну пажњу треба посветити испитивању трудноће и прописима о превенцији трудноће када се даје талидомид. Видети одељак 4.6).
Интратекална администрација
Било је случајева смрти услед ненамерне интратекалне примене лека ВЕЛЦАДЕ. ВЕЛЦАДЕ 1 мг прашак за раствор за ињекције намењен је само за интравенозну примену, док је ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције намењен за интравенозну или поткожну примену. ВЕЛЦАДЕ се не сме примењивати интратекално.
Гастроинтестинална токсичност
Гастроинтестинални токсични ефекти, укључујући мучнину, пролив, повраћање и затвор, веома су чести током лечења леком ВЕЛЦАДЕ. Ретко су пријављивани случајеви паралитичког илеуса (видети одељак 4.8). Због тога је потребно пажљиво пратити пацијенте са констипацијом.
Хематолошка токсичност
Лечење ВЕЛЦАДЕ -ом је врло често повезано са хематолошким токсичним ефектима (тромбоцитопенија, неутропенија и анемија). У студијама спроведеним код пацијената са рецидивираним мултиплим мијеломом лечених ВЕЛЦАДЕ-ом и код пацијената са претходно нелеченим МЦЛ леченим ВЕЛЦАДЕ-ом у комбинацији са ритуксимабом, циклофосфамидом, доксорубицином и преднизоном (ВцР-ЦАП), једна од најчешћих хематолошких токсичности била је пролазна тромбоцитопенија. Тромбоцити су били на најнижем нивоу 11. дана сваког циклуса третмана ВЕЛЦАДЕ и враћали су се на почетне нивое обично током следећег циклуса. Није било доказа о кумулативној тромбоцитопенији. Средњи надир вредности тромбоцита био је приближно 40% основне вредности у студијама мултиплог мијелома са ВЕЛЦАДЕ -ом који се користио као монотерапија и 50% у МЦЛ студији. Код пацијената са узнапредовалим мијеломом, тежина тромбоцитопеније била је повезана са вредностима тромбоцита пре третмана: за вредности тромбоцита на почетку 75.000 / мцл, само 14% од 309 пацијената имало је број тромбоцита ≤ 25.000 / мцл током студије.
Код пацијената са МЦЛ (студија ЛИМ-3002), била је већа инциденција (56,7% наспрам 5,8%) Тромбоцитопенија степена ≥ 3 у ВЕЛЦАДЕ терапијској групи (ВцР-ЦАП) у односу на не-ВЕЛЦАДЕ групу (ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон [Р-ЦХОП]). Две групе лечења биле су сличне у укупној учесталости крварења свих степена (6,3% у групи ВцР-ЦАП и 5,0% у групи Р-ЦХОП) и степена 3 и великог крварења (ВцР-ЦАП: 4 пацијента [ 1,7%]; Р-ЦХОП: 3 пацијента [1,2%]). У ВцР-ЦАП групи, 22,5% пацијената је добило трансфузију тромбоцита у поређењу са 2,9% пацијената у групи Р-ЦХОП.
Гастроинтестинална и интрацеребрална крварења су пријављена у вези са третманом ВЕЛЦАДЕ -ом. Због тога треба пратити нивое тромбоцита пре примене сваке дозе лека ВЕЛЦАДЕ. Терапију ВЕЛЦАДЕ -ом треба прекинути када број тромбоцита достигне вредности
Комплетну крвну слику, са диференцијалним бројем и укључујући број тромбоцита, треба често пратити током лечења леком ВЕЛЦАДЕ.Када је то клинички примерено, треба размотрити трансфузију тромбоцита (видети одељак 4.2).
Код пацијената са МЦЛ без доказа о кумулативној неутропенији, примећена је пролазна реверзибилна неутропенија између курсева лечења. Неутрофили су били на најнижем нивоу 11. дана сваког циклуса лечења ВЕЛЦАДЕ -ом и обично су се враћали на почетну вредност у следећем циклусу. У студији ЛИМ-3002, подршка фактору раста примењена је код 78% пацијената у групи са ВцР-ЦАП и 61% пацијената у групи са Р-ЦХОП. Пошто су пацијенти са неутропенијом под повећаним ризиком од инфекција, треба их пратити због знакова и симптома инфекције и одмах их лечити. Фактори раста гранулоцита могу се применити за лечење хематолошке токсичности у складу са локалном стандардном праксом. У случају поновљених одлагања у спровођењу терапијских токова, треба размотрити превентивну употребу фактора раста гранулоцита (видети одељак 4.2).
Реактивација вируса Херпес зостер
Пацијентима који примају ВЕЛЦАДЕ препоручује се антивирусна профилакса. У студији фазе ИИИ спроведеној код пацијената са претходно нелеченим мултиплим мијеломом, укупна учесталост реактивације херпес зостера била је чешћа код пацијената лечених леком ВЕЛЦАДЕ + Мелпхалан + Преднизон него код пацијената лечених Мелпхаланом + Преднизоном (респективно 14 % наспрам 4 %).
Код пацијената са МЦЛ (студија ЛИМ-3002), учесталост инфекције херпес зостером била је 6,7% у групи са ВцР-ЦАП и 1,2% у групи са Р-ЦХОП (видети одељак 4.8).
Реактивација и инфекција вирусом хепатитиса Б (ХБВ)
Када се ритуксимаб користи у комбинацији са ВЕЛЦАДЕ -ом, пре почетка лечења код пацијената код којих постоји ризик од инфекције ХБВ -ом увек треба извршити скрининг на ХБВ. Носиоце хепатитиса Б и пацијенте са историјом хепатитиса Б треба пажљиво пратити због клиничких и лабораторијских знакова активне ХБВ инфекције током и после лечења ритуксимабом у комбинацији са ВЕЛЦАДЕ -ом. Треба размотрити антивирусну профилаксу. За више информација погледајте Сажетак карактеристика производа за ритуксимаб.
Прогресивна мултифокална леукоенцефалопатија (ПМЛ)
Веома ретки случајеви инфекције вирусом Јохн Цуннингхам (ЈЦ) који су резултирали ПМЛ -ом и смрћу пријављени су код пацијената лечених леком ВЕЛЦАДЕ, са непознатим узроком. Пацијенти са дијагнозом ПМЛ су претходно узимали имуносупресивну терапију или су је узимали истовремено. Већина случајева ПМЛ -а дијагностикована је у року од 12 месеци од узимања прве дозе лека ВЕЛЦАДЕ. Пацијенте треба редовно надзирати ради откривања нових или погоршања неуролошких симптома или знакова који могу указивати на ПМЛ међу диференцијалним дијагнозама проблема централног нервног система. Ако се сумња на дијагнозу ПМЛ -а, пацијенте треба упутити лекару који је специјализован за лечење ПМЛ -а и применити одговарајуће дијагностичке мере за ПМЛ. У случају потврђене дијагнозе ПМЛ -а, лечење леком ВЕЛЦАДЕ треба прекинути.
Периферна неуропатија
Лечење ВЕЛЦАДЕ -ом најчешће је повезано са настанком периферне, првенствено сензорне неуропатије, али су забележени случајеви тешке моторне неуропатије са или без периферне сензорне неуропатије.
Учесталост периферне неуропатије расте на почетку лечења и достиже врхунац у петом циклусу.
Пацијенте треба пажљиво пратити због симптома неуропатије као што су пецкање, хиперестезија, хипоестезија, парестезија, малаксалост, неуропатски бол или слабост.
У клиничкој студији фазе ИИИ која је поредила ВЕЛЦАДЕ даван интравенозно са поткожним путем, инциденција периферне неуропатије степена 2 била је 24% у групи са поткожном применом и 41% у групи са интравенозном ињекцијом (п = 0,0124). неуропатија се јавила код 6% пацијената у групи за поткожно лечење у поређењу са 16% у групи за интравенозно лечење (п = 0,0264). сви степени периферне неуропатије са интравенозном применом ВЕЛЦАДЕ били су нижи у претходним студијама где се ВЕЛЦАДЕ примењивао интравенозно него у студији ММИ -3021.
Неуролошка процена се препоручује код пацијената са појавом или погоршањем периферне неуропатије, за које може бити потребна промена дозе или режима или промена начина примене на поткожни пут (видети одељак 4.2). Неуропатија се лечи супортивним или другим терапијама.
Код пацијената који примају ВЕЛЦАДЕ у комбинацији са лековима за које је познато да су повезани са неуропатијом (на пример талидомид) треба размотрити рано и редовно праћење симптома неуропатије повезане са лечењем са неуролошком проценом и треба узети у обзир смањење дозе или прекид лечења .
Поред периферне неуропатије, аутономна неуропатија може допринети настанку неких нежељених реакција, попут постуралне хипотензије и тешког затвора илеуса. Још увек су доступне ограничене информације о аутономној неуропатији и њеном доприносу овим нежељеним ефектима.
Грчеви
Напади су ретко пријављивани код пацијената без историје напада или епилепсије. Посебна пажња је потребна при лечењу пацијената са ризиком од напада.
Хипотензија
Лечење ВЕЛЦАДЕ -ом је обично повезано са ортостатском / постуралном хипотензијом. Већина нежељених реакција су благе до умерене тежине и примећене су током лечења. Пацијенти који су доживели ортостатску хипотензију са ВЕЛЦАДЕ -ом (убризгано интравенозно) нису имали претходне епизоде ортостатске хипотензије пре лечења. Терапија за лечење ортостатске хипотензије била је потребна код већине пацијената. Мањи број пацијената са ортостатском хипотензијом доживео је епизоде синкопе. Ортостатска / постурална хипотензија није била акутно повезана са болусном инфузијом ВЕЛЦАДЕ -а.
Механизам овог догађаја није познат, иако се компонента може одредити аутономном неуропатијом. Аутономна неуропатија може бити повезана са бортезомибом, или је могуће да лек може погоршати већ постојеће стање, као што је дијабетичка или амилоидотична неуропатија. Треба бити крајње опрезан у лечењу пацијената са синкопом у анамнези који се лече лековима за које је познато да су повезани са хипотензијом, или пацијената који показују дехидрацију услед понављајуће дијареје или повраћања. Ортостатска / постурална хипотензија се може лечити прилагођавањем дозе антихипертензивне лекове, рехидратацију или примену минералокортикостероида и / или симпатомиметичких лекова.Пацијенте треба саветовати да се консултују са својим лекаром у случају вртоглавице, вртоглавице или кратких епизода несвестице.
Синдром задње реверзибилне енцефалопатије (ПРЕС)
Било је извештаја о ПРЕС -у код пацијената који су примали ВЕЛЦАДЕ. ПРЕС је ретка неуролошка форма коју карактерише брза, често реверзибилна еволуција која се може манифестовати нападима, хипертензијом, главобољом, летаргијом, конфузијом, слепилом и другим визуелним и неуролошким променама. Дијагноза се потврђује радиолошким снимкама можданих структура, по могућности добијеним помоћу нуклеарне магнетне резонанце (МРИ). Код пацијената са ПРЕС -ом, терапију ВЕЛЦАДЕ -ом треба прекинути.
Отказивање срца
Током лечења бортезомибом примећен је акутни почетак или погоршање конгестивне срчане инсуфицијенције и / или развој смањене фракције избацивања леве коморе. Задржавање течности може бити предиспонирајући фактор за знакове и симптоме срчане инсуфицијенције. Пацијенти са срчаном инсуфицијенцијом или са факторима ризика за срчану инсуфицијенцију треба пажљиво пратити.
Електрокардиографска испитивања
Појединачни случајеви продужења КТ интервала примећени су у клиничким студијама, чија узрочност није утврђена.
Плућне промене
Ретки случајеви акутне дифузне инфилтративне плућне болести непознате етиологије, попут упале плућа, интерстицијске пнеумоније, плућне инфилтрације и акутног респираторног дистрес синдрома (АРДС), пријављени су код пацијената који су примали ВЕЛЦАДЕ (видети одељак 4.8). Неке од ових епизода биле су фаталне. Радиографски снимак грудног коша пре третмана препоручује се као полазна основа за могуће плућне промене након третмана.
У случају појаве или погоршања плућних симптома (нпр. Кашаљ, диспнеја), мора се извршити хитна дијагностичка процена пацијента и последично одговарајуће лечење. Пре наставка терапије леком ВЕЛЦАДЕ треба размотрити равнотежу ризика и користи.
Током клиничке студије, два од два пацијента који су примали високе дозе цитарабина (2 г / м² дневно) као 24-часовну континуирану инфузију у комбинацији са даунорубицином и ВЕЛЦАДЕ-ом за лечење релапса акутне мијелоичне леукемије умрла су услед АРДС-а. почетној фази терапије, студија је прекинута. Стога се не препоручује овај специфични режим комбиниране терапије с високим дозама цитарабина (2 г / м² дневно) у континуираној инфузији од 24 сата.
Оштећена функција бубрега
Бубрежне компликације су честе код пацијената са мултиплим мијеломом. Пацијенте са бубрежном инсуфицијенцијом треба пажљиво пратити (видети одељке 4.2 и 5.2).
Оштећена функција јетре
Бортезомиб се метаболише помоћу ензима јетре. Код пацијената са умереним или тешким оштећењем јетре, изложеност бортезомибу је повећана; такве пацијенте треба лечити смањеном дозом ВЕЛЦАДЕ -а и треба их пажљиво пратити због појаве токсичности (видети одељке 4.2 и 5.2.).
Јетрене реакције
Ретки случајеви затајења јетре забележени су код пацијената који су примали ВЕЛЦАДЕ и истовремену терапију лековима и са тешком основном болешћу.Забележене су и друге реакције у јетри, попут повишених јетрених ензима, хипербилирубинемије и хепатитиса. Ове промене могу бити реверзибилне након престанка терапије бортезомибом (видети одељак 4.8).
Синдром лизе тумора
Пошто је бортезомиб цитотоксична супстанца и стога је у стању да брзо уништи малигне плазма ћелије и МЦЛ ћелије, могу се уочити компликације изазване синдромом лизе тумора. Пацијенти у ризику од развоја синдрома туморске лизе су они који су показали велико оптерећење тумором пре почетка лечења. Ове пацијенте треба пажљиво пратити и предузети мере предострожности.
Истовремена примена других лекова
Пацијенте на истовременој терапији бортезомибом и снажним инхибиторима ЦИП3А4 треба пажљиво пратити. Треба бити посебно опрезан при истовременој примени супстрата бортезомиба и ЦИП3А4 или ЦИП2Ц19 (видети одељак 4.5).
Нормалну функцију јетре треба потврдити код пацијената који примају оралне хипогликемике и лечити их опрезно (видети одељак 4.5).
Потенцијално имунолошки комплекс посредоване реакције
Повремено су пријављиване потенцијалне реакције повезане са имунолошким комплексом, попут серумске болести, полиартритиса са осипом и пролиферативног гломерулонефритиса. У случају озбиљних догађаја, примену бортезомиба треба прекинути.
04.5 Интеракције са другим лековима и други облици интеракција -
образовање ин витро указују да је бортезомиб слаб инхибитор изоензима цитокрома П450 (ЦИП) 1А2, 2Ц9, 2Ц19, 2Д6 и 3А4. С обзиром на ограничен допринос (7%) изоензима ЦИП2Д6 метаболизму бортезомиба, верује се да овај фенотип са ниским метаболизмом не утиче на укупну доступност бортезомиба.
Студија интеракције лекова и лекова, заснована на подацима од 12 пацијената, ради испитивања ефеката кетоконазола, снажног инхибитора ЦИП3А4, на фармакокинетику бортезомиба (убризгава се интравенозно) показала је средњи пораст АУЦ. 35% бортезомиба (90% ЦИ [ 1.032-1.772)] Због тога треба пажљиво пратити пацијенте који примају истовремени третман бортезомибом и снажним инхибиторима ЦИП3А4 (нпр. Кетоконазол, ритонавир).
У студији интеракције лекова и лекова, заснованој на подацима 17 пацијената, да би се испитао утицај омепразола, снажног инхибитора ЦИП2Ц19, на фармакокинетику бортезомиба (убризганог интравенозно) није било доказа о ефекту значајног на фармакокинетику бортезомиба .
Клиничка студија интеракције лекова и лекова, заснована на подацима 6 пацијената, ради испитивања ефеката рифампицина, снажног индуктора ЦИП3А4, на фармакокинетику бортезомиба (убризганог интравенозно) показала је просечно смањење АУЦ. 45% бортезомиба. Стога је истовремена примена не препоручује се употреба бортезомиба са снажним индукторима ЦИП3А4 (нпр. рифампицин, карбамазепин, фенитоин, фенобарбитал и кантарион) јер се ефикасност може смањити.
У истој клиничкој студији интеракције лекова, на основу података од 7 пацијената, ради провере дејства дексаметазона, слабог индуктора ЦИП3А4, на фармакокинетику бортезомиба (убризганог интравенозно) није било значајног утицаја на фармакокинетику бортезомиба.
Студија интеракције лекова и лекова, заснована на подацима 21 пацијента, за процену ефекта мелфалан-преднизона на фармакокинетику бортезомиба (ињектиран интравенозно), показала је повећање АУЦ бортезомиба за 17%.
Ово се није сматрало клинички релевантним.
У клиничким испитивањима, хипогликемија и хипергликемија су ретко пријављиване код пацијената са дијабетесом који су примали оралне хипогликемијске лекове. Пацијентима на оралној антидијабетичкој терапији који примају ВЕЛЦАДЕ може бити потребно пажљиво праћење глукозе у крви и прилагођавање дозе антидијабетичких лекова.
04.6 Трудноћа и дојење -
Контрацепција код мушкараца и жена
Мушкарци и жене у репродуктивном периоду морају да користе одговарајуће мере контрацепције током примене и 3 месеца након лечења.
Трудноћа
Нема доступних клиничких података о изложености бортезомибу током трудноће .. Тератогени потенцијал бортезомиба није у потпуности истражен.
У претклиничким студијама, примена бортезомиба у максимално толерисаним дозама од стране мајке није показала никакав утицај на ембриофетални развој код пацова и зечева. Студије на животињама нису спроведене да би се утврдио било какав утицај на пород и постнатални развој (видети одељак 5.3). ВЕЛЦАДЕ се не сме користити током трудноће осим ако клиничко стање пацијента то захтева.
Пацијенткињу треба обавестити о потенцијалним ризицима по фетус ако се ВЕЛЦАДЕ примењује током трудноће, или ако пацијенткиња затрудне током лечења.
Талидомид је моћан тератоген код људи и изазива тешке, по живот опасне урођене мане. Талидомид је контраиндикован током трудноће и код жена у репродуктивној доби осим ако су испуњени сви услови програма превенције трудноће са талидомидом. Пацијенти који примају ВЕЛЦАДЕ у комбинацији са талидомидом морају да се придржавају Програм превенције трудноће са талидомидом За додатне информације погледајте Сажетак карактеристика производа талидомида.
Време храњења
Није познато да ли се бортезомиб излучује у мајчино млеко. Због могућности озбиљних нежељених реакција ВЕЛЦАДЕ -а код дојенчади, дојење треба прекинути током терапије ВЕЛЦАДЕ -ом.
Плодност
Студије плодности нису спроведене са леком ВЕЛЦАДЕ (видети одељак 5.3).
04.7 Утицај на способност управљања возилима и рада на машинама -
ВЕЛЦАДЕ може умерено утицати на способност управљања возилима и машинама.
ВЕЛЦАДЕ може бити врло често повезан са умором, обично са вртоглавицом, ретко са синкопом, обично са ортостатском / постуралном хипотензијом или замагљеним видом. Пацијенти треба да буду изузетно опрезни при управљању возилима или раду са машинама (видети одељак 4.8).
05.0 ФАРМАКОЛОШКА СВОЈСТВА -
05.1 "Фармакодинамичка својства -
Фармакотерапијска група: антинеопластични лекови, други антинеопластични лекови.
АТЦ код: Л01КСКС32.
Механизам дејства
Бортезомиб је инхибитор протеасома. Посебно је назначено да инхибира активност 26С протеасома сличну кимотрипсину у ћелијама сисара. 26С протеасом је велики полипептидни комплекс, одговоран за разградњу убиквинираних протеина. Метаболички пут убиквитин-протеасома игра битну улогу у контроли промета специфичних протеина, чиме се одржава хомеостаза у ћелијама. Инхибиција протеасома 26С спречава ову циљану протеолизу и утиче на пренос сигнала унутар ћелије, што резултира смрћу ћелија рака.
Бортезомиб је високо селективан за протеасом. У концентрацијама од 10 мцМ, бортезомиб не инхибира ниједан од бројних процењених рецептора и протеаза и више је 1.500 пута селективнији за протеасом од другог циљног ензима. Оцењивана је кинетика инхибиције протеосома ин витро а бортезомиб дисоцира од протеасома са т½ од 20 минута, показујући тако да је инхибиција бортезомиба реверзибилна.
Инхибиција протеасома посредована бортезомибом има бројне ефекте на ћелије рака, укључујући, али без ограничења, промену регулаторних протеина који контролишу напредовање ћелијског циклуса и „активацију нуклеарног фактора кБ (НФ-кБ). протеасом доводи до застоја ћелијског циклуса и апоптозе.
НФ-кБ је транскрипциони фактор чија је активација потребна у многим фазама карциногенезе, укључујући раст и преживљавање ћелија, ангиогенезу, ћелијску интеракцију и метастазе. Код мијелома, бортезомиб утиче на способност ћелија мијелома да ступају у интеракцију са микроокружењем коштане сржи.
Испитивања су показала да је бортезомиб цитотоксичан за бројне врсте ћелија рака и да су те ћелије много осетљивије на проапоптотичне ефекте инхибиције протеасома од нормалних.Бортезомиб узрокује смањење раста тумора. ин виво у многим предклиничким моделима рака, укључујући мултипли мијелом.
Подаци ин витро, ек виво и на животињским моделима сугеришу да бортезомиб повећава остеобластну диференцијацију и активност и инхибира остеокластичну функцију.Ови ефекти су примећени код пацијената са мултиплим мијеломом са узнапредовалом остеолитичком болешћу и лечени бортезомибом.
Клиничка ефикасност код претходно нелеченог мултиплог мијелома
Међународно, рандомизовано (1: 1), отворено, проспективно клиничко испитивање фазе ИИИ (ММИ-3002 ВИСТА) спроведено је на 682 пацијента како би се проценило да ли је ВЕЛЦАДЕ (Вц) (1,3 мг / м² интравенозно убризган) у комбинацији са мелфаланом ( М) (9 мг / м²) и преднизон (П) (60 мг / м²) побољшали су време до прогресије (ТТП) у поређењу са мелфаланом (9 мг / м²) и преднизоном (60 мг / м²) код пацијената са претходно нелеченим мултиплим мијеломом . Лечење је трајало до 9 циклуса (приближно 54 недеље) и прекинуто је рано у случају прогресије болести или неприхватљиве токсичности. У студији је средња старост пацијената била 71 година, 50% су били мушкарци, 88% су били белци, а средња вредност резултата перформанси Карнофског била је 80. Пацијенти су имали ИгГ / ИгА / мијелом лаког ланца у 63% / 25 % / 8% случајева, средњи хемоглобин од 105 г / л и средњи број тромбоцита од 221,5 к 109 / л. У две групе, проценат пацијената који су имали клиренс креатинина ≤ 30 био је сличан. Мл / мин ( 3% у свакој руци).
У времепривремена анализа планирано, примарна крајња тачка, време до прогресије, је достигнуто и пацијентима у М + П групи је понуђен третман Вц + М + П. Просечно праћење је било 16,3 месеца. Након медијалног праћења Коначна цифра преживљавања је ажурирана 60,1 месеци. Статистички значајна корист од преживљавања примећена је у корист групе за лечење Вц + М + П (ХР = 0,695, п = 0,00043) упркос накнадним терапијама, укључујући режиме засноване на ВЕЛЦАДЕ. Средње преживљавање у лечењу Вц + М + П група је имала 56,4 месеца у поређењу са 43,1 месеца у групи која је примала М + П. Резултати ефикасности приказани су у Табели 11.
Табела 11: Резултати ефикасности након коначног ажурирања података о преживљавању ВИСТА -е
Пацијенти кандидати за трансплантацију матичних ћелија
Спроведена су два рандомизована, отворена мултицентрична клиничка испитивања фазе ИИИ (ИФМ-2005-01, ММИ-3010) како би се показала безбедност и ефикасност ВЕЛЦАДЕ-а у двострукој и трострукој комбинацији са другим хемотерапеутским агенсима као индукциона терапија пре трансплантације матичних ћелија код пацијената претходно није лечен од мултиплог мијелома.
У студији ИФМ-2005-01 ВЕЛЦАДЕ у комбинацији са дексаметазоном [ВцДк, н = 240] упоређен је са винкристин-доксорубицин-дексаметазоном [ВДДк, н = 242]. Пацијенти у групи ВцДк примили су четири 21-дневна циклуса, од којих се сваки састојао од ВЕЛЦАДЕ-а (1,3 мг / м² интравенозно два пута недељно 1., 4., 8. и 11. дана) и оралног дексаметазона (40 мг / м2) дневно. дана 1 до 4 и дана 9 до 12, у циклусима 1 и 2, и у данима 1 до 4 у циклусима 3 и 4).
Сто деведесет осам пацијената (82%) и 208 пацијената (87%) у групама ВДДк и ВцДк, било је подвргнуто аутологној трансплантацији матичних ћелија; већина пацијената је подвргнута једној трансплантацији. Демографске карактеристике пацијената и основне карактеристике болести биле су сличне између две групе лечења. У студији је просечна старост пацијената била 57 година, 55% су били мушкарци, а 48% пацијената је имало висок цитогенетски ризик.Медијан трајања терапије је био 13 недеља за групу са ВДДк и 11 недеља за групу са ВДДк. Средњи број циклуса примљених у обе групе био је 4 циклуса.
Примарна крајња тачка ефикасности студије била је стопа одговора након индукције (ЦР + нЦР). Статистички значајна разлика у ЦР + нЦР је примећена у корист групе ВЕЛЦАДЕ у комбинацији са дексаметазоном. Секундарне крајње тачке ефикасности укључивале су стопе одговора (ЦР + нЦР, ЦР + нЦР + ВГПР + ПР) након трансплантације, преживљавање без прогресије и укупно преживљавање Главни резултати ефикасности приказани су у Табели 12.
Табела 12: Резултати ефикасности у студији ИФМ-2005-01
У студији ММИ-3010 ВЕЛЦАДЕ у комбинацији са талидомидом и дексаметазоном [ВцТДк, н = 130] упоређен је са талидомид-дексаметазоном [ТДк, н = 127]. Пацијенти у групи са ВцТДк примили су шест циклуса од 4 недеље, од којих се сваки састојао од ВЕЛЦАДЕ-а (1,3 мг / м² примењеног два пута недељно 1., 4., 8. и 11. дана, након чега следи период одмора од 17 дана од 12 до 28), дексаметазон (40 мг орално дано 1 до 4 дана и 8 до 11 дана) и талидомид (50 мг дневно орално дано 1-14 дана, са повећањем дозе до 100 мг 15-28 дана, а затим 200 мг по дану дан).
Сто и пет пацијената (81%) и 78 пацијената (61%) у групама ВцТДк и ТДк, респективно. били су подвргнути једној аутологној трансплантацији матичних ћелија. Демографске карактеристике пацијената и основне карактеристике болести биле су сличне између две групе лечења. Пацијенти у групама ВцТДк и ТДк имали су средњу старост од 57 и 56 година, 99% и 98% пацијената су били белци; 58% и 54% били су мушкарци. У групи са ВцТДк 12% пацијената је цитогенетски класификовано као високоризично у поређењу са 16% пацијената у групи са ТДк. Средње трајање лечења је 24,0 недеља, а медијан број примљених циклуса лечења је 6,0 и био је доследан у свим групама лечења.
Примарне крајње тачке ефикасности студије биле су стопе одговора након индукције и после трансплантације (ЦР + нЦР). Уочена је статистички значајна разлика у ЦР + нЦР у корист групе која је примала ВЕЛЦАДЕ у комбинацији са дексаметазоном и талидомидом. Секундарне крајње тачке ефикасности укључивале су преживљавање без прогресије и укупно преживљавање. Главни резултати ефикасности приказани су у Табели 13.
Табела 13: Резултати ефикасности из студије ММИ-3010
Клиничка ефикасност код пацијената са рецидивом или рефракторним мултиплим мијеломом
Профили безбедности и ефикасности ВЕЛЦАДЕ -а (ињектирани интравенозно) процењени су у две студије у препорученој дози од 1,3 мг / м²: рандомизована, контролисана студија ИИИ фазе дексаметазона (Дек) (АПЕКС) спроведена на 669 пацијената са повратним и рефракторним мултиплим мијеломом , који су прошли 1 до 3 претходне линије лечења и једнофазно испитивање фазе ИИ, спроведено код 202 пацијента са повратним и рефракторним мултиплим мијеломом, који су прошли најмање две претходне линије лечења са прогресијом болести након последње терапије.
У студији фазе ИИИ, код свих пацијената, укључујући и оне који су примили само једну претходну линију терапије, лечење ВЕЛЦАДЕ -ом је довело до значајног продужења времена до прогресије, значајног продужења преживљавања и значајног повећања стопе одговора. у поређењу са третманом дексаметазоном (видети Табелу 14).
На основу података добијених из „привремена анализа Унапред планирано, Одбор за праћење је препоручио прекид терапије дексаметазоном у корист терапије ВЕЛЦАДЕ за све пацијенте рандомизоване на лечење дексаметазоном, без обзира на статус болести. Због овог раног укрштања, просечно трајање праћења пацијената уживо било је 8,3 месеца. у групи за лечење ВЕЛЦАДЕ -ом, укупно преживљавање је било дуже и стопа одговора је била већа и код пацијената који су били рефракторни на последњу терапију и код оних који нису.
Од 669 уписаних пацијената, 245 (37%) је било 65 година или више. Параметри одговора, као и ТТП, били су значајно бољи за ВЕЛЦАДЕ без обзира на старост.Сви параметри ефикасности (време до прогресије, укупно преживљавање и стопа одговора) значајно су побољшани у групи ВЕЛЦАДЕ, без обзира на нивое б2-микроглобулина на почетку.
У ватросталној популацији студије ИИ фазе, одговоре је оценила независна комисија, а примењени критеријуми одговора су они који су утврђени. од стране Европске групе за трансплантацију коштане сржи. Просечан укупни опстанак свих пацијената укључених у студију био је 17 месеци (распон Перформанце Статус, од статуса брисања хромозома 13 или од броја или врсте претходних терапија. Стопа одговора пацијената који су већ били на 2-3 или више година) од 7 линија третмана то је било 32% (10/32) и 31% (21/67), респективно.
Табела 14: Резиме резултата ефикасности из фаза ИИИ (АПЕКС) и ИИ студија
У студији фазе ИИ, пацијенти који нису постигли оптималан одговор на монотерапију ВЕЛЦАДЕ -ом лечени су високим дозама дексаметазона и ВЕЛЦАДЕ -а. Протокол је пацијентима који су постигли мање од оптималног одговора на монотерапију ВЕЛЦАДЕ -ом омогућио примање дексаметазона.
Укупно 74 процењивана пацијента лечена су дексаметазоном и ВЕЛЦАДЕ -ом. Комбиновани третман је омогућио добијање одговора или побољшање одговора [МР 11% или ПР 7%] код 18% пацијената.
Клиничка ефикасност код пацијената са повратним / рефракторним мултиплим мијеломом са поткожном применом ВЕЛЦАДЕ -а
Неинфериорно, отворено, рандомизирано клиничко испитивање фазе ИИИ упоредило је ефикасност и безбедност поткожне примене ВЕЛЦАДЕ-а у односу на интравенозну примену.Ово истраживање обухватило је 222 пацијента са релапсом / рефракторним мултиплим мијеломом, рандомизованим у односу 2: 1 за примање 1,3 мг / м² ВЕЛЦАДЕ -а поткожно или интравенозно током 8 циклуса. За оне пацијенте који нису постигли оптималан одговор на само ВЕЛЦАДЕ (мањи од потпуног одговора [ЦР]) након 4 циклуса, било им је дозвољено да приме 20 мг дексаметазона на дан пацијента са почетном степеном ≥ 2 периферне неуропатије или бројем тромбоцита
Ова студија је испунила примарни циљ неинфериорности процењене на стопи одговора (ЦР + ПР) након 4 циклуса монотерапије ВЕЛЦАДЕ-ом за супкутани и интравенозни начин примене, са стопом одговора од 42% у оба случаја. Додатно, секундарне крајње тачке ефикасности у вези са одговором и временом до догађаја показали су конзистентне резултате и за поткожни и за интравенозни пут (Табела 15).
Табела 15: Сажетак анализа ефикасности које упоређују супкутану и интравенозну примену ВЕЛЦАДЕ -а
Третман ВЕЛЦАДЕ-ом у комбинацији са пегилованим липосомалним доксорубицином (студија ДОКСИЛ-ММИ-3001)
Отворена, рандомизирана, мултицентрична студија фазе ИИИ паралелне групе спроведена је на 646 пацијената упоређујући безбедност и ефикасност ВЕЛЦАДЕ плус пегилованог липосомалног доксорубицина са ВЕЛЦАДЕ монотерапијом код пацијената са мултиплим мијеломом који раније нису примали најмање 1 терапију, а који раније нису показала прогресију болести током терапије антрациклинима. Примарна крајња тачка ефикасности било је време до прогресије (ТТП), док су секундарне крајње тачке ефикасности биле укупно преживљавање (ОС) и укупна стопа одговора (ОРР: (потпун одговор + делимичан одговор) користећи критеријуме "Европска група за крв и срж Трансплантација (ЕБМТ).
Резултати "привремена анализа дефинисан протоколом (заснован на 249 ТТП догађаја) довео је до превременог прекида студије ради ефикасности. Ова привремена анализа показала је смањење ризика од ТТП за 45% (95% ЦИ; 29-57%, стр
Коначна анализа укупног преживљавања (ОС) извршена након медијана праћења од 8,6 година није показала значајну разлику у ОС између две групе лечења. Средња вредност ОС била је 30,8 месеци (95% ЦИ; 25,2-36,5 месеци) за пацијенте на ВЕЛЦАДЕ-у монотерапије и 33,0 месеци (95% ЦИ; 28,9-37,1 месеци) за пацијенте на комбинованој терапији са ВЕЛЦАДЕ-ом и пегилованим липосомалним доксорубицином.
Третман ВЕЛЦАДЕ -ом у комбинацији са дексаметазоном
У одсуству директног поређења између ВЕЛЦАДЕ-а и ВЕЛЦАДЕ-а у комбинацији са дексаметазоном код пацијената са прогресивним мултиплим мијеломом, изведена је „упарена статистичка анализа“ да би се упоредили резултати не-рандомизованог крака ВЕЛЦАДЕ-а у комбинацији са дексаметазоном (фаза ИИ студије отворена ознака ММИ-2045), са резултатима добијеним у групама за терапију монотерапије ВЕЛЦАДЕ из различитих рандомизованих испитивања фазе ИИИ (М34101-039 [АПЕКС] и ДОКСИЛ ММИ-3001) у истој индикацији.
Анализа усклађених парова је статистичка метода у којој су пацијенти у терапијској групи која је проучавана (нпр. ВЕЛЦАДЕ у комбинацији са дексаметазоном) и пацијенти у упоредној групи (нпр. ВЕЛЦАДЕ) упоредиви у односу на збуњујуће факторе кроз појединачно упаривање испитаника. Ова метода минимизира ефекте збуњујућих фактора који су уочени при процени ефеката третмана коришћењем не-рандомизованих података.
Идентификовано је 127 упарених парова пацијената. Анализа је показала побољшање укупне стопе одговора (ОРР: ЦР + ПР) (однос шанси 3.769; 95% ЦИ 2.045-6.947; п
Доступне су ограничене информације о поновном лечењу ВЕЛЦАДЕ -ом код рецидивираног мултиплог мијелома.
Друга фаза ММИ-2036 (РЕТРИЕВЕ), студија са једном руком, спроведена је како би се утврдила ефикасност и безбедност поновног лечења ВЕЛЦАДЕ-ом. Сто тридесет пацијената (старости ≥ 18 година) са мултиплим мијеломом који су претходно имали најмање један парцијални одговор на режим који садржи ВЕЛЦАДЕ повучен је након прогресије. Најмање 6 месеци након претходне терапије, ВЕЛЦАДЕ је започет последњом толерисаном дозом од 1,3 мг / м² (н = 93) или ≤ 1,0 мг / м² (н = 37) и примењен 1., 4., 8. и 11. дана сваке 3 недеље у трајању до 8 циклуса, било као монотерапија или у комбинацији са дексаметазоном према стандардној терапији. Дексаметазон је даван у комбинацији са ВЕЛЦАДЕ -ом 83 пацијента у првом циклусу, а додатних 11 пацијената је примало дексаметазон током следећих циклуса поновног лечења ВЕЛЦАДЕ -ом.
Примарна крајња тачка била је најбоље потврђен одговор на поновно лечење према критеријумима ЕБМТ -а. Најбоља укупна стопа одговора (ЦР + ПР) на поновљено лечење код 130 пацијената била је 38,5% (95% ЦИ: 30,1; 47)., 4).
Клиничка ефикасност код претходно нездрављених пацијената са лимфомом ћелија плашта (МЦЛ)
ЛИМ-3002 је рандомизирана, отворена студија фазе ИИИ, која упоређује ефикасност и безбедност комбинације ВЕЛЦАДЕ, ритуксимаба, циклофосфамида, доксорубицина и преднизона (ВцР-ЦАП; н = 243) са онима из ритуксимаба, циклофосфамида, доксорубицина, винкристин и преднизон (Р-ЦХОП; н = 244) код претходно нездрављених одраслих пацијената са МЦЛ (Фаза ИИ, ИИИ или ИВ). Пацијенти у групи за лечење ВцР-ЦАП-ом примали су ВЕЛЦАДЕ (1,3 мг / м²; 1., 4., 8., 11. дан, период одмора 12-21), ритуксимаб 375 мг / м² ИВ дан; циклофосфамид 750 мг / м² ИВ првог дана; доксорубицин 50 мг / м² ИВ првог дана и преднизон 100 мг / м² орално 1. до 5. дана 21-дневног циклуса третмана ВЕЛЦАДЕ. Пацијенти са документованим првим одговором на циклус 6 добили су два додатна курса лечења.
Примарна крајња тачка ефикасности била је преживљавање без прогресије на основу процене независног одбора за преглед (ИРЦ). Секундарне крајње тачке укључивале су време до прогресије (ТТП), време до следећег третмана против лимфома (ТНТ), трајање „интервала без лечења (ТФИ) ), укупну стопу одговора (ОРР) и потпуну стопу одговора (ЦР / ЦРу), укупно преживљавање (ОС) и трајање одговора.
Демографске карактеристике и основне карактеристике болести биле су генерално добро избалансиране између две групе лечења: средња старост пацијената била је 66 година, 74% су били мушкарци, 66% су били белци и 32% азијци, 69% пацијената. / или МЦЛ позитивна биопсија коштане сржи, 54% пацијената имало је оцену Међународног прогностичког индекса (ИПИ) ≥ 3, а 76% је имало ИВ фазу болести. Трајање лечења (средња вредност = 17 недеља) и трајање праћења (средња вредност = 40 месеци) били су упоредиви у обе групе лечења. Пацијенти у обе руке су примали медијану од 6 циклуса, при чему је 14% испитаника у групи ВцР-ЦАП и 17% пацијената у групи Р-ЦХОП примало додатна 2 циклуса. Већина пацијената у обе групе је завршило лечење, 80% у ВцР-ЦАП групи и 82% у Р-ЦХОП групи. Резултати ефикасности приказани су у Табели 16:
Табела 16: Резултати ефикасности из студије ЛИМ-3002
Медијан ПФС-а који је одредио истраживач био је 30,7 месеци у ВцР-ЦАП групи и 16,1 месец у Р-ЦХОП групи (однос опасности [ХР] = 0,51; п
Медијан трајања потпуног одговора био је 42,1 месец у групи са ВцР-ЦАП у поређењу са 18 месеци у групи са Р-ЦХОП. Укупно трајање одговора било је 21,4 месеца дуже у групи са ВцР-ЦАП (средња вредност 36,5 месеци наспрам 15,1 месеци у групи Р-ЦХОП). При средњем трајању праћења од 40 месеци, медијан укупног преживљавања (ОС) био је у корист ВцР-ЦАП (56,3 месеца у групи Р-ЦХОП, а није постигнут у групи ВцР-ЦАП), (процена ХР = 0,80; п = 0,173). Постојао је тренд ка продуженом укупном преживљавању у корист групе ВцР-ЦАП; процењена 4-годишња стопа преживљавања била је 53,9% у Р-ЦХОП групи и 64,4% у ВцР-ЦАП групи.
Пацијенти са претходно леченом амилоидозом лаког ланца (АЛ)
Отворена, не-рандомизована студија фазе И / ИИ спроведена је да би се утврдила безбедност ВЕЛЦАДЕ-а код пацијената са претходно леченом амилоидозом лаког ланца (АЛ). Током студије нису примећене нове забринутости за безбедност, а посебно ВЕЛЦАДЕ није довео до погоршања оштећења органа (срца, бубрега и јетре).
У истраживачкој анализи ефикасности, за две повезане кохорте доза, пријављена је стопа одговора од 67,3% (од чега 28,6% потпуног одговора) у смислу хематолошког одговора (протеин М), код 49 пацијената који су могли да се процењују са максимално дозвољеним дозама 1,6 мг / м² једном недељно и 1,3 мг / м² два пута недељно.За два повезана курса дозе, једногодишње преживљавање је било 88,1%.
Педијатријска популација
Европска агенција за лекове одустала је од обавезе достављања резултата студија са ВЕЛЦАДЕ -ом у свим подскупинама педијатријске популације са мултиплим мијеломом и лимфомом ћелија плашта (видети одељак 4.2 за информације о употреби у педијатрији).
05.2 "Фармакокинетичка својства -
Апсорпција
Након интравенске болусне примене од 1,0 мг / м² и 1,3 мг / м² 11 пацијената са мултиплим мијеломом и клиренсом креатинина већим од 50 мл / мин, средње максималне концентрације бортезомиба у плазми у првим дозама биле су 57 и 112 нг / мЛ , редом. У наредним дозама, средње максималне запажене концентрације у плазми кретале су се од 67 до 106 нг / мЛ за дозу од 1,0 мг / м² и између 89 и 120 нг / мЛ за дозу од 1,3 мг / м².
Након поновљеног интравенозног болуса или поткожне ињекције дозе од 1,3 мг / м² код пацијената са мултиплим мијеломом (н = 14 у интравенозној групи, н = 17 у поткожној групи), укупна системска изложеност лековима (АУЦласт) била је еквивалентна за поткожно и интравенозни начин давања.Цмак након поткожне примене (20,4 нг / мл) била је нижа од интравенозне (223 нг / мл). Средњи геометријски однос АУЦ је био 0,99 и са интервалима поузданости од 90% износио је 80,18% - 122,80%.
Дистрибуција
Код пацијената са мултиплим мијеломом, средњи волумен дистрибуције (Вд) бортезомиба се кретао од 1659 до 3294 л након једнократног или поновљеног интравенозног дозирања од 1,0 мг / м² или 1,3 мг / м². Ово сугерише да је бортезомиб широко распрострањен у периферним ткивима. У опсегу концентрације бортезомиба од 0,01 до 1,0 μг / мл, везивање за протеине хумане плазме ин витро у просеку је износио 82,9%. Фракција бортезомиба везана за протеине плазме није зависила од концентрације.
Биотрансформација
образовање ин витро на микросомима људске јетре и изоензимима цитокрома П450 израженим хуманом ц-ДНК указује да се бортезомиб углавном подвргава оксидативном метаболизму преко ензима цитокрома П450, 3А4, 2Ц19 и 1А2. Главни метаболички пут састоји се од деборонизације која води до два деборонизована метаболита који се затим хидроксилују у различите метаболите. Деборовани метаболити бортезомиба су неактивни као инхибитори 26С протеасома.
Елиминација
Средњи полувреме елиминације (т1 / 2) бортезомиба током лечења са више доза креће се од 40 до 193 сата. Бортезомиб се брже уклања након прве дозе него у следећим дозама. Средњи укупни клиренс био је 102 и 112 л / х након прве дозе од 1,0 мг / м² и 1,3 мг / м², односно између 15 и 32 л / х и између 18 и 32 л / х за наредне дозе од 1,0 мг / м² и 1,3 мг / м², респективно.
Посебне популације
Хепатична инсуфицијенција
Учинак јетрене инсуфицијенције на фармакокинетику бортезомиба проучаван је у првој фази клиничке студије на 61 пацијенту са примарним солидним туморима са различитим степеном оштећења јетре и лечен дозама бортезомиба укључујући између 0,5 и 1,3 мг / м².
Блага хепатична инсуфицијенција није променила дозу нормализовану АУЦ бортезомиба у поређењу са оном која се примећује код пацијената са нормалном функцијом јетре. Међутим, дозе нормализоване средње вредности АУЦ повећане су за приближно 60% код пацијената са умереним или тешким оштећењем јетре. Препоручује се нижа почетна доза код пацијената са умереним или тешким оштећењем јетре., Те такве пацијенте треба пажљиво пратити (видети одељак 4.2, Табела 6).
Инсуфицијенција бубрега
Фармакокинетичка студија спроведена је код пацијената са различитим степеном оштећења бубрега, који су према вредностима клиренса креатинина (ЦрЦЛ) класификовани у следеће групе: Нормални (ЦрЦЛ ≥60 мл / мин / 1,73 м², н = 12), Благи ( ЦрЦЛ = 40-59 мл / мин / 1,73 м², н = 10), Умерено (ЦрЦЛ = 20-39 мл / мин / 1,73 м², н = 9) и Тешко (Интравенски ЦрЦЛ у дозама у распону од 0,7 до 1,3 мг / мин) м² два пута недељно. Изложеност ВЕЛЦАДЕ -у (АУЦ и Цмак нормализована дозом) била је слична у свим групама пацијената (видети одељак 4.2).
05.3 Предклинички подаци о безбедности -
У концентрацијама
Бортезомиб није показао генотоксичност у тесту мутагености ин витро (Амесов тест), нити у тесту микронуклеуса ин виво спроведено на мишевима.
У студијама развојне токсичности спроведеним на пацовима и зечевима, ембрионално -фетални морталитет је приказан при дозама токсичним за мајку, али није било ембриофеталне токсичности испод дозе токсичног за мајку. Студије плодности нису спроведене, али је извршена процена репродуктивног ткива у студијама опште токсичности. У шестомесечној студији на пацовима откривени су дегенеративни ефекти и на тестисе и на јајнике. Стога је вероватно да бортезомиб може имати потенцијални утицај на плодност мушкараца и жена. Студије о перинаталном и постнаталном развоју нису спроведене.
Студије опште токсичности у више циклуса спроведене на пацовима и мајмунима откриле су да су главни циљни органи: гастроинтестинални тракт, што је довело до повраћања и / или дијареје; хематопоетска и лимфна ткива, што резултира цитопенијом у периферној крви, атрофијом лимфног ткива и хематопоетском хипоцелуларношћу коштане сржи; периферна неуропатија (виђена код мајмуна, мишева и паса) која утиче на аксоне сензорних нерава; и благе промене у бубрезима. Након прекида лечења, сви ови циљни органи показали су делимичан до потпуни опоравак.
На основу студија на животињама, чини се да је пролаз бортезомиба кроз крвно -мождану баријеру ограничен, а значај код људи је непознат.
Фармаколошке студије о кардиоваскуларној сигурности спроведене на мајмунима и псима показују да интравенозна примена доза мг / м2 2 до 3 пута већа од клинички препоручене дозе доводи до повећања откуцаја срца, смањене срчане контрактилности, хипотензије и смрти. Код паса, смањена срчана контрактилност и хипотензија су контролисани акутним третманом са позитивним инотропним агенсима или вазопресорима и примећено је благо повећање коригованог КТ интервала.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ -
06.1 Помоћне супстанце -
Манитол (Е421)
Азот
06.2 Некомпатибилност "-
Овај лек се не сме мешати са другим производима осим са онима који су поменути у одељку 6.6.
06.3 Период важења "-
Неотворена бочица
3 године.
Реконституисани раствор
Реконституисани раствор треба користити одмах након припреме.
Ако се не употреби одмах, одговорност је корисника да се придржава услова и времена складиштења лека пре употребе.
Међутим, физичка и хемијска стабилност реконституисаног раствора показана је 8 сати на 25 ° Ц када се чува у оригиналној бочици и / или у шприцу. Укупно време складиштења реконституисаног лека пре примене не би требало да прелази 8 сати.
06.4 Посебне мере предострожности за складиштење -
Чувати на температури која не прелази 30 ° Ц.
Бочицу чувајте у спољном паковању ради заштите лека од светлости.
За услове складиштења након реконституције лека, видети одељак 6.3.
06.5 Природа непосредног паковања и садржај паковања -
Бочица од 10 мл од стакла типа И, са сивим бромбутилним чепом и алуминијумским затварачем, са краљевски плавим чепом садржи 3,5 мг бортезомиба.
Бочица се налази у прозирном блистеру који се састоји од послужавника са поклопцем.
Свако паковање садржи 1 бочицу за једнократну употребу.
06.6 Упутства за употребу и руковање -
Опште мере предострожности
Бортезомиб је цитотоксично средство. Због тога треба бити посебно опрезан при руковању и припреми ВЕЛЦАДЕ -а. Препоручује се ношење рукавица и друге заштитне одеће како би се спречио контакт са кожом.
Руковање ВЕЛЦАДЕ -ом мора се вршити уз строго придржавање асептичних техника због одсуства конзерванса.
Било је случајева смрти услед ненамерне интратекалне примене лека ВЕЛЦАДЕ. ВЕЛЦАДЕ 1 мг прашак за раствор за ињекције намењен је само за интравенозну примену, док је ВЕЛЦАДЕ 3,5 мг прашак за раствор за ињекције намењен за интравенозну или поткожну примену.ВЕЛЦАДЕ се не сме примењивати интратекално.
Упутства за реконституцију
ВЕЛЦАДЕ мора реконституисати здравствени радник.
Интравенозна ињекција
Свака бочица од 10 мл која садржи ВЕЛЦАДЕ 3,5 прашак за раствор за ињекцију мора се реконституисати са 3,5 мл раствора за ињекције натријум хлорида 9 мг / мл (0,9%). Растварање лиофилизованог праха траје мање од 2 минута. Након реконституције, сваки мл раствора садржи 1 мг бортезомиба. Реконституисани раствор је бистар и безбојан, са коначним пХ између 4 и 7. Реконституисани раствор треба визуелно прегледати пре примене како би се проверило да ли има честица или је дошло до промене боје. раствор се не сме користити и треба га одбацити.
Поткожна ињекција
Свака бочица од 10 мл која садржи ВЕЛЦАДЕ 3,5 прашак за раствор за ињекцију мора се реконституисати са 1,4 мл раствора за ињекције натријум хлорида 9 мг / мл (0,9%). Растварање лиофилизованог праха траје мање од 2 минута. Након реконституције, сваки мл раствора садржи 2,5 мг бортезомиба. Реконституисани раствор је бистар и безбојан, са коначним пХ између 4 и 7. Реконституисани раствор треба визуелно прегледати пре примене како би се проверило да ли има честица или је дошло до промене боје. раствор се не сме користити и треба га одбацити.
Одлагање
ВЕЛЦАДЕ је само за једнократну употребу.
Неискоришћени лек и отпад из овог лека треба одложити у складу са локалним прописима.
07.0 НОСИЛАЦ „Овлашћења за промет“ -
ЈАНССЕН-ЦИЛАГ ИНТЕРНАТИОНАЛ Н.В.
Турнхоутсевег, 30
Б-2340 Беерсе
Белгија
08.0 БРОЈ ОВЛАШЋЕЊА ЗА ПРОМЕТ -
ЕУ/1/04/274/001
036559019
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШТЕЊА -
Датум прве ауторизације: 26. април 2004
Датум последњег обнављања овлашћења: 26. април 2014
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА -
04/2015