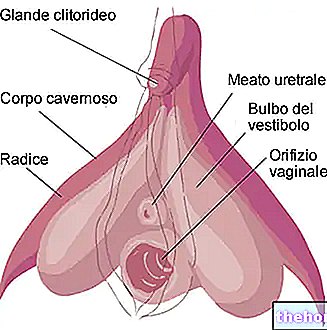
Активни састојци: Езетимибе, Симвастатин
ГОЛТОР 10 мг / 10 мг
ГОЛТОР 10 мг / 20 мг
ГОЛТОР 10 мг / 40 мг
ГОЛТОР 10 мг / 80 мг таблете
Индикације Зашто се Голтор користи? За шта је то?
ГОЛТОР садржи активне супстанце езетемибе и симвастатин. ГОЛТОР је лек који се користи за смањење нивоа укупног холестерола, "лошег" холестерола (ЛДЛ холестерола) и масних супстанци које се зову триглицериди у крви. Осим тога, ГОЛТОР повећава ниво "доброг" холестерола (ХДЛ холестерола).
ГОЛТОР делује на два начина за снижавање холестерола. Активна супстанца езетимиб смањује холестерол апсорбован у дигестивном тракту. Активни састојак симвастатин који припада класи "статина" инхибира производњу холестерола који синтетише тело.
Холестерол је једна од неколико масних супстанци које се налазе у крвотоку. Укупни холестерол се углавном састоји од ЛДЛ холестерола и ХДЛ холестерола. ЛДЛ холестерол се често назива "лошим" холестеролом јер се може накупити у зидовима артерија и формирати плакове. Временом, ово накупљање плака може довести до сужавања артерија. Ово сужавање може успорити или блокирати проток крви до виталних органа, попут срца и мозга. Ова блокада протока крви може узроковати срчани или мождани удар.
ХДЛ холестерол се често назива "добрим" холестеролом јер помаже у спречавању накупљања лошег холестерола у артеријама и штити од срчаних болести.
Триглицериди су још један облик масти у крви који може повећати ризик од срчаних обољења.
ГОЛТОР се користи за пацијенте који не могу да контролишу ниво холестерола само исхраном. Док узимате овај лек, и даље треба да следите дијету за смањење холестерола.
ГОЛТОР се користи као додатак вашој исхрани за снижавање холестерола ако имате:
- повишен ниво холестерола у крви (примарна хиперхолестеролемија) [породична и не-породична хетерозигота] или повишени ниво масноће у крви (мешовита хиперлипидемија):
- који нису добро контролисани само статином;
- за које сте узимали статине и езетимиб као посебне таблете;
- наследна болест (хомозиготна породична хиперхолестеролемија) која повећава ниво холестерола у крви. Могуће је да се лечите и другим третманима.
ГОЛТОР вам не помаже да смршате.
Контраиндикације Када се Голтор не сме користити
Немојте узимати ГОЛТОР ако:
- ако сте алергични (преосетљиви) на „езетимиб, симвастатин или било који други састојак овог лека
- тренутно има проблема са јетром
- сте трудни или дојите
- узимате лекове са једном или више следећих активних супстанци:
- итраконазол, кетоконазол, посаконазол или вориконазол (користи се за лечење гљивичних инфекција)
- еритромицин, кларитромицин или телитромицин (користе се за лечење инфекција)
- Инхибитори ХИВ протеазе као што су индинавир, нелфинавир, ритонавир и саквинавир (инхибитори ХИВ протеазе се користе за лечење ХИВ инфекција)
- боцепревир или телапревир (користе се за лечење инфекција вирусом хепатитиса Ц)
- нефазодон (користи се за лечење депресије)
- цобицистат
- гемфиброзил (користи се за снижавање холестерола)
- циклоспорин (често се користи код пацијената са трансплантацијом органа)
- даназол (људски хормон који се користи за лечење ендометриозе, стања у којем слузница материце расте изван материце).
- узимате или сте у последњих 7 дана узимали или сте узимали лек који се зове фусидатна киселина (користи се за лечење бактеријске инфекције).
Не узимајте више од 10 мг / 40 мг ГОЛТОР -а ако узимате ломитапид (користи се за лечење озбиљног и ретког генетског стања холестерола).
Питајте свог лекара за савет ако нисте сигурни да ли је лек који користите један од горе наведених.
Предострожности при употреби Шта треба да знате пре него што узмете лек Голтор
Реците свом лекару:
- свих ваших здравствених стања, укључујући алергије.
- ако конзумирате велике количине алкохола или сте икада имали болест јетре. У овом случају ГОЛТОР можда није прикладан за вас.
- ако имате операцију. Можда ћете на кратко морати да престанете са узимањем лека ГОЛТОР.
- ако сте Азијат, друга доза може бити одговарајућа за вас.
Ваш лекар мора да уради крвни тест пре него што узмете ГОЛТОР и ако имате симптоме проблема са јетром док узимате ГОЛТОР. Ова анализа се ради да би се утврдило да ли јетра правилно функционише.
Ваш лекар може такође наредити крвне претраге за проверу функције јетре након почетка терапије ГОЛТОР -ом.
Док се лечите овим леком, ваш лекар ће пажљиво проверити да немате дијабетес или да нисте у опасности од развоја дијабетеса. У опасности сте од развоја дијабетеса ако имате висок ниво шећера и масти у крви, ако имате прекомерну тежину и висок крвни притисак.
Реците свом лекару ако имате тешку болест плућа. Треба избегавати примену ГОЛТОР-а са фибратима (неке врсте лекова за снижавање холестерола) јер употреба ГОЛТОР-а са фибратима није проучавана.
Одмах се обратите свом љекару ако имате болове у мишићима, осјетљивост мишића и слабост мишића неутврђеног узрока, јер проблеми с мишићима ријетко могу бити озбиљни и довести до озљеде мишићног ткива узрокујући оштећење бубрега, а врло ријетко је дошло и до смрти. Ризик од повреде мишића је већи при већим дозама ГОЛТОР -а, посебно при дози од 10 мг / 80 мг.
Ризик од повреде мишића је такође већи код неких пацијената. Реците свом лекару ако се нешто од следећег односи на вас:
- имају проблеме са бубрезима
- имате проблеме са штитном жлездом
- има 65 или више година
- је женско
- су икада имали проблема са мишићима током лечења лековима за снижавање холестерола који се називају „статини“ (као што су симвастатин, аторвастатин и росувастатин) или фибрати (као што су гемфиброзил и безафибрат)
- ви или ваша ужа породица имате наследну болест мишића.
Такође, реците свом лекару или фармацеуту ако имате сталну слабост мишића. Можда ће бити потребни додатни тестови и лекови за дијагностиковање и лечење овог стања.
Деца и адолесценти
Употреба ГОЛТОР -а се не препоручује деци млађој од 10 година.
Интеракције Који лекови или храна могу да промене учинак Голтора
Обавестите свог лекара ако узимате, недавно сте узимали или бисте могли узети било који други лек са било којом од следећих активних супстанци. Узимање ГОЛТОР -а са било којим од следећих лекова може повећати ризик од проблема са мишићима (неки су већ горе поменути у одељку „Немојте узимати ГОЛТОР ако“):
- циклоспорин (често се користи код пацијената на трансплантацији органа)
- даназол (вештачки хормон који се користи за лечење ендометриозе, стања у којем слузница материце расте изван материце)
- лекови са активном супстанцом као што су итраконазол, кетоконазол, флуконазол, посаконазол или вориконазол (користе се за лечење гљивичних инфекција)
- фибрати са активним састојцима као што су гемфиброзил и безафибрат (користе се за снижавање холестерола)
- еритромицин, кларитромицин, телитромицин или фусидатна киселина (користи се за лечење бактеријских инфекција). Немојте узимати фусидатну киселину док користите овај лек. Види такође параграф 4 ове брошуре.
- Инхибитори ХИВ протеазе као што су индинавир, нелфинавир, ритонавир и саквинавир (користе се за лечење СИДЕ)
- боцепревир или телапревир (користе се за лечење инфекција вирусом хепатитиса Ц)
- нефазодон (користи се за лечење депресије)
- лекови са активном супстанцом кобицистат
- амиодарон (користи се за лечење неправилног рада срца)
- верапамил, дилтиазем или амлодипин (користе се за лечење високог крвног притиска, болова у грудима повезаних са срчаним обољењима или другим срчаним обољењима)
- ломитапид (користи се за лечење озбиљног и ретког генетског стања холестерола
- високе дозе (1 г или више дневно) ниацина или никотинске киселине (такође се користе за снижавање холестерола)
- колхицин (користи се за лечење гихта).
Осим горе наведених лекова, обавестите свог лекара или фармацеута ако узимате или сте недавно узимали било које друге лекове, укључујући и оне који се набављају без рецепта. Посебно реците свом лекару ако узимате нешто од следећег:
- лекови са активним састојком за спречавање стварања крвних угрушака, као што су варфарин, флуиндион, фенпрокумон или аценокумарол (антикоагуланти)
- холестирамин (такође се користи за снижавање холестерола) јер утиче на начин деловања ГОЛТОР -а
- фенофибрат (такође се користи за снижавање холестерола)
- рифампицин (користи се за лечење туберкулозе).
Такође морате рећи сваком лекару који вам преписује нови лек да узимате ГОЛТОР.
ГОЛТОР уз храну и пиће
Сок од грејпа садржи једну или више супстанци које мењају метаболизам неких лекова, укључујући ГОЛТОР. Конзумирање сока од грејпа треба избјегавати јер може повећати ризик од проблема с мишићима.
Упозорења Важно је знати да:
Трудноћа и дојење
Немојте користити ГОЛТОР ако сте трудни, ако намеравате да затрудните или сумњате на трудноћу. Ако затрудните док узимате ГОЛТОР, одмах престаните са узимањем и обратите се лекару. ГОЛТОР се не сме користити током дојења јер није познато да ли лек прелази у мајчино млеко.
Питајте свог лекара или фармацеута за савет пре него што узмете било који лек.
Вожња и управљање машинама
Не очекује се да ће ГОЛТОР ометати вашу способност управљања возилима и рада на машинама. Међутим, треба имати на уму да су неки људи доживели вртоглавицу након узимања ГОЛТОР -а.
ГОЛТОР садржи лактозу
ГОЛТОР таблете садрже шећер, лактозу. Ако вам је лекар рекао да имате „нетолеранцију на неке шећере, обратите се лекару пре узимања овог лека.
Дозирање и начин употребе Голтор: Дозирање
Ваш лекар ће утврдити која јачина таблете вам одговара, на основу вашег тренутног третмана и вашег профила ризика.
Таблете нису сломљене и не треба их делити.
Увек узимајте овај лек тачно онако како вам је рекао ваш лекар или фармацеут. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
- Пре него што почнете да узимате ГОЛТОР, мора да сте већ били на дијети за снижавање нивоа холестерола.
- Током лечења леком ГОЛТОР требало би да наставите да се придржавате ове дијете како бисте смањили холестерол.
Одрасли: доза је 1 таблета ГОЛТОР -а орално једном дневно.
Употреба код адолесцената (од 10 до 17 година): Доза је 1 таблета ГОЛТОР -а орално једном дневно (не сме се прекорачити максимална доза од 10 мг / 40 мг једном дневно).
Доза од 10 мг / 80 мг ГОЛТОР -а се препоручује само одраслим пацијентима са веома високим нивоом холестерола и високим ризиком од срчаних обољења који нису постигли идеални ниво холестерола са најнижим дозама.
Узмите ГОЛТОР увече. Можете га узети са или без хране.
Ако вам је лекар преписао ГОЛТОР са другим леком за снижавање холестерола који садржи активну супстанцу холестирамин или било које друго средство за одвајање жучних киселина, требало би да узмете ГОЛТОР најмање 2 сата пре или 4 сата након узимања средства за одвајање жучних киселина.
Ако сте заборавили да узмете ГОЛТОР
- немојте узети двоструку дозу да бисте надокнадили заборављену таблету, само узмите нормалну дозу лека ГОЛТОР следећег дана у уобичајено време.
Ако престанете да узимате ГОЛТОР
- разговарајте са својим лекаром или фармацеутом јер ваш холестерол може поново порасти. Ако имате додатних питања о употреби овог лека, обратите се свом лекару или фармацеуту.
Предозирање Шта учинити ако сте узели превише Голтора
Ако сте узели више лека ГОЛТОР него што је потребно, обратите се свом лекару или фармацеуту.
Нежељени ефекти Који су нежељени ефекти Голтора
Као и сви лекови, ГОЛТОР може изазвати нежељена дејства, мада се она не морају јавити код свих (погледајте одељак 2 Шта треба да знате пре него што узмете ГОЛТОР).
Пријављени су следећи уобичајени нежељени ефекти (могу се јавити у до 1 на 10 особа):
- болови у мишићима
- повећање вредности лабораторијских тестова крви за функцију јетре (трансаминазе) и / или мишића (ЦК)
Пријављени су следећи неуобичајени нежељени ефекти (могу се јавити у до 1 на 100 људи):
- повећање вредности крвних тестова у вези са функцијом јетре; повећање вредности мокраћне киселине у крви; повећање времена потребног за згрушавање крви; присуство протеина у урину; смањење телесне тежине
- вртоглавица главобоља; пецкање
- бол у стомаку; лоше варење; надутост; мучнина; Повратио се; абдомена надимање; дијареја; Сува уста; бол у стомаку
- осип; свраб; уртикарија
- бол у зглобовима; бол у мишићима; осетљивост; слабост или грчеви; Бол у врату; бол у рукама или ногама; болови у леђима • неуобичајен умор или слабост; уморни; бол у грудима; отицање, посебно шака и стопала
- поремећај сна; тешко заспати
Осим тога, пријављени су и следећи нежељени ефекти код људи који узимају ГОЛТОР или лекове који садрже активне супстанце езетимиб или симвастатин:
- низак број црвених крвних зрнаца (анемија); смањен број крвних зрнаца, што може изазвати модрице / крварење (тромбоцитопенија)
- губитак осећаја или слабости у рукама и ногама; лоше памћење; губитак памћења; збуњеност
- проблеми са дисањем, укључујући упорни кашаљ и / или отежано дисање или грозницу
- констипација
- упала панкреаса често са јаким боловима у стомаку
- упала јетре са следећим симптомима: жутило коже и очију; свраб; урин тамне боје или столице светле боје; осећај умора или слабости; губитак апетита; инсуфицијенција јетре; камење у жучној кеси или упала жучне кесе (што може изазвати бол у стомаку, мучнину и повраћање)
- губитак косе; повишен црвени осип, понекад са лезијама у облику циља (еритема мултиформе)
- реакција преосјетљивости која укључује неке од сљедећих карактеристика: преосјетљивост (алергијске реакције укључујући отицање лица, усана, језика и / или грла које могу узроковати отежано дисање или гутање и захтијевају хитно лијечење, бол или упалу зглобова, упалу крви крвних судова, абнормалне модрице, осип и оток, осип, осетљивост коже на сунце, грозницу, црвенило, отежано дисање и мучнину, симптоме сличне лупусу (који укључују осип, проблеме са кожом) зглобове и ефекте на бела крвна зрнца).
- бол у мишићима; осетљивост; мишићна слабост или грчеви; повреде мишића; проблеми са тетивама, понекад компликовани пуцањем тетиве.
- смањен апетит
- валунзи; висок крвни притисак
- бол
- еректилна дисфункција
- депресија
- промене у неким вредностима крвних тестова које се односе на функцију јетре
Додатни могући нежељени ефекти пријављени код неких статина:
- поремећаји сна, укључујући ноћне море
- сексуалне тешкоће
- дијабетес. Већа је вероватноћа ако имате висок ниво шећера и масти у крви, имате прекомерну тежину и висок крвни притисак. Ваш лекар ће вас пратити током лечења овим леком.
- бол у мишићима, осетљивост или слабост који су константни и који можда неће нестати након престанка узимања лека ГОЛТОР (учесталост није позната).
Одмах се обратите свом љекару ако имате болове у мишићима, осјетљивост мишића и слабост мишића неутврђеног узрока, јер проблеми с мишићима ријетко могу бити озбиљни и довести до озљеде мишићног ткива узрокујући оштећење бубрега, а врло ријетко је дошло и до смрти.
Пријављивање нежељених ефеката
Ако приметите било које нежељено дејство, обратите се свом лекару или фармацеуту.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нежељена дејства директно путем националног система за пријављивање на: ввв.агензиафармацо.гов.ит/ит/респонсабили.Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока употребе који је наведен на амбалажи иза „ЕКСП“.
Немојте чувати ГОЛТОР таблете на температурама изнад 30 ° Ц.
Жуљеви: Чувати у оригиналном паковању ради заштите лека од светлости и влаге.
Боце: Чувајте боце добро затворене да бисте заштитили лек од светлости и влаге.
Не бацајте никакве лекове у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Остале информације
Шта значи ГОЛТОР
Активне супстанце ГОЛТОР -а су езетимиб и симвастатин.
Свака таблета садржи 10 мг езетимиба и 10 мг, 20 мг, 40 мг или 80 мг симвастатина.
Помоћни састојци су: бутилхидроксианизол, монохидрат лимунске киселине, натријум кроскармелоза, хипромелоза, лактоза монохидрат, магнезијум стеарат, микрокристална целулоза, пропил галат.
Опис изгледа ГОЛТОР -а и садржај паковања
ГОЛТОР је доступан у облику белих до готово белих таблета у облику капсуле са кодом "311", "312", "313" или "315" на једној страни. Таблете нису сломљене и не треба их делити.
ГОЛТОР је доступан у паковањима од 7, 10, 14, 28, 30, 50, 56, 84, 90, 98, вишеструко паковање које садржи 98 (2 паковања од 49), 100 или 300 таблета.
Не могу се на тржиште ставити све величине паковања.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ГОЛТОР ТАБЛЕТИ
02.0 КВАЛИТАТИВНИ И КОЛИЧИНСКИ САСТАВ
Свака таблета садржи 10 мг езетимиба и 10, 20, 40 или 80 мг симвастатина.
Помоћне супстанце:
Свака таблета од 10 мг / 10 мг садржи 58,2 мг лактозе монохидрата.
Свака таблета од 10 мг / 20 мг садржи 126,5 мг лактозе монохидрата.
Свака таблета од 10 мг / 40 мг садржи 262,9 мг лактозе монохидрата.
Свака таблета од 10 мг / 80 мг садржи 535,8 мг лактозе монохидрата.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Таблет.
Беле до готово беле таблете у облику капсуле са кодом „311“, „312“, „313“ или „315“ на једној страни.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Хиперхолестеролемија
ГОЛТОР је индикован као додатак исхрани код пацијената са примарном хиперхолестеролемијом (породична и не-породична хетерозигота) или са мешовитом хиперлипидемијом где је назначена употреба комбинованог производа:
• пацијенти који немају адекватну контролу само на статину;
• пацијенти који су већ лечени статином и езетимибом.
ГОЛТОР садржи езетимиб и симвастатин. Показало се да симвастатин (20-40 мг) смањује учесталост кардиоваскуларних догађаја (видети одељак 5.1). Још није доказан благотворан учинак езетимиба на кардиоваскуларни морбидитет и морталитет.
Хомозиготна породична хиперхолестеролемија (Хомозиготна ИФ)
ГОЛТОР је индикован као додатак исхрани код пацијената са хомозиготном породичном хиперхолестеролемијом. Пацијенти се такође могу подвргнути додатним терапијским мерама (на пример, афереза липопротеина ниске густине [ЛДЛ]).
04.2 Дозирање и начин примене
Хиперхолестеролемија
Пацијент треба да се придржава адекватног режима исхране са ниским садржајем масти и да настави са дијетом током лечења ГОЛТОР-ом.
Лек треба давати орално. Распон доза ГОЛТОР -а је 10 мг / 10 мг / дан до 10 мг / 80 мг / дан увече. Дозе можда нису све доступне у свим државама чланицама. Уобичајена доза је 10 мг / 20 мг / дан. О 10 мг / 40 мг / дан примењивано увече као појединачна доза. Доза од 10 мг / 80 мг се препоручује само код пацијената са тешком хиперхолестеролемијом и са високим ризиком од кардиоваскуларних компликација који нису постигли терапијске циљеве са нижим дозама и када очекује се да ће користи надмашити потенцијалне ризике (видети одељке 4.4 и 5.1).
Ниво липопротеина холестерола ниске густине (ЛДЛ-Ц), ризик од коронарне болести срца и одговор пацијента на тренутну терапију снижавања холестерола треба узети у обзир на почетку лечења или када се промени доза.
Дозу ГОЛТОР-а треба индивидуализовати на основу признате ефикасности различитих јачина ГОЛТОР-а (видети одељак 5.1, Табела 1) и одговора на текућу терапију снижавања холестерола. Дозу треба прилагођавати, ако је потребно, у интервалима. мање од 4 недеље ГОЛТОР се може примењивати са или без оброка Таблету не треба делити.
Хомозиготна породична хиперхолестеролемија
Препоручена почетна доза за пацијенте са хомозиготном породичном хиперхолестеролемијом је ГОЛТОР 10 мг / 40 мг / дан увече. Доза од 10 мг / 80 мг се препоручује само када се очекује да ће користи надмашити потенцијалне ризике (видети горе; одељци 4.3 и 4.4). ГОЛТОР се може користити код ових пацијената као помоћно средство у другим третманима за смањење липида (нпр. ЛДЛ афереза) или ако такви третмани нису доступни.
Истовремена примена са другим лековима
Лек ГОЛТОР треба да се примени ≥ 2 сата пре или ≥ 4 сата након примене средства за одвајање жучних киселина.
Код пацијената који узимају амиодарон, амлодипин, верапамил или дилтиазем истовремено са ГОЛТОР -ом, доза ГОЛТОР -а не би требало да прелази 10 мг / 20 мг / дан (видети одељке 4.4 и 4.5).
Код пацијената који примају дозе ниацина за снижавање липида (≥ 1 г / дан) истовремено са ГОЛТОР-ом, доза ГОЛТОР-а не би требало да прелази 10 мг / 20 мг / дан (видети одељке 4.4 и 4.5).
Употреба код старијих особа
Није потребно прилагођавање дозе код старијих пацијената (видети одељак 5.2).
Употреба код деце и адолесцената
Започињање лечења мора се спровести под надзором специјалисте.
Адолесценти ≥ 10 година (пубертетски статус: дечаци у Таннеровој фази ИИ и вишој и девојчице које су биле у постменархету најмање годину дана): Клиничко искуство код педијатријских и адолесцентних пацијената (10 до 17 година) је ограничено. Уобичајено препоручује се почетак доза је 10 мг / 10 мг једном дневно увече Препоручени распон доза је 10 мг / 10 мг до највише 10 мг / 40 мг / дан (видети одељке 4.4 и 5.2).
Деца
Користити у случају оштећења јетре
Није потребно прилагођавање дозе за благо (Цхилд-Пугх скор 5 до 6) оштећење јетре. Лечење ГОЛТОР-ом се не препоручује код пацијената са умереним (Цхилд-Пугх скор 7 до 9) или тешким оштећењем јетре (Цхилд-Пугх скор> 9 ), (види одељке 4.4 и 5.2).
Употреба у случају оштећења бубрега
Није потребна промена дозе код пацијената са благим оштећењем бубрега (процењена брзина гломеруларне филтрације ≥60 мл / мин / 1,73 м2). Код пацијената са хроничном бубрежном болешћу и процењеном брзином гломеруларне филтрације 2, препоручена доза ГОЛТОР -а је 10/20 мг једном дневно увече (видети одељке 4.4, 5.1 и 5.2). Веће дозе треба примењивати са опрезом.
04.3 Контраиндикације
Преосјетљивост на езетимиб, симвастатин или било коју помоћну твар.
Трудноћа и дојење (видети одељак 4.6).
Активна болест јетре или повишене, перзистентне и неодређене вредности серумских трансаминаза.
Истовремена примена моћних инхибитора ЦИП3А4 (агенаса који повећавају АУЦ приближно 5 или више пута) (нпр. Итраконазол, кетоконазол, посаконазол, вориконазол, еритромицин, кларитромицин, телитромицин, инхибитори протеазе ХИВ-а (нпр. Нелфинавир), боцепревир, телаодвир) (непретиназ) видети одељке 4.4 и 4.5).
Истовремена примена гемфиброзила, циклоспорина или даназола (видети одељке 4.4 и 4.5).
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Миопатија / рабдомиолиза
У постмаркетиншком искуству са езетимибом забележени су случајеви миопатије и рабдомиолизе. Већина пацијената који су развили рабдомиолизу били су на истовременој терапији езетимибом и статином. Међутим, рабдомиолиза је пријављена врло ретко са езетимибом и монотерапијом. Веома ретко са додатком езетимиб другим лековима за које је познато да су повезани са повећаним ризиком од рабдомиолизе.
ГОЛТОР садржи симвастатин. Симвастатин, као и други инхибитори ХМГ-ЦоА редуктазе, повремено изазива миопатију, која се манифестује као бол у мишићима, осетљивост или слабост повезана са повећањем нивоа креатин киназе (ЦК) изнад 10 пута горње границе нормале. Миопатија се понекад манифестује као рабдомиолиза са или без акутна бубрежна инсуфицијенција која је последица миоглобинурије и врло ретко је дошло до фаталног исхода Ризик од миопатије је повећан високим нивоом инхибиторне активности ХМГ-ЦоА редуктазе у плазми.
Као и код других инхибитора ХМГ-ЦоА редуктазе, ризик од миопатије / рабдомиолизе је доза повезана са симвастатином.У бази података клиничког испитивања у којој је 41.413 пацијената лечено симвастатином, од којих је 24.747 (приближно 60%) укључено у студије са средњом вредношћу након најмање 4 године праћења, учесталост миопатије била је приближно 0,03%, 0,08% и 0,61% при 20, 40 и 80 мг / дан, респективно. У овим студијама, пацијенти су помно праћени, а неки лекови у интеракцији су искључени.
У клиничкој студији у којој су пацијенти са историјом инфаркта миокарда лечени симвастатином од 80 мг / дан (просечно праћење од 6,7 година), учесталост миопатије била је приближно 1,0% у поређењу са инциденцом од 0,02% која је виђена код пацијената лечено са 20 мг / дан. Приближно половина ових случајева миопатије се десила током прве године лечења. Учесталост миопатије током сваке наредне године лечења била је приближно 0,1% (видети одељке 4.8 и 5.1).
Ризик од миопатије је већи код пацијената лечених ГОЛТОР-ом 10/80 мг него код других терапија заснованих на статинима са сличном ефикасношћу у снижавању ЛДЛ-Ц. Стога, дозу ГОЛТОР -а од 10/80 мг треба користити само код пацијената са тешком хиперхолестеролемијом и са високим ризиком од кардиоваскуларних компликација који нису постигли циљеве лечења нижим дозама и када се очекује да ће користи премашити потенцијалне ризике. Код пацијената лечених ГОЛТОР-ом 10/80 мг за које је потребно средство за интеракцију, треба применити нижу дозу ГОЛТОР-а или алтернативни режим статина са мањим потенцијалом за интеракцију између лекова (видети доле). Мере за смањење ризика од миопатије изазване интеракцијама лекова и ставови 4.2, 4.3 и 4.5).
У клиничкој студији у којој је више од 9.000 пацијената са хроничном бубрежном болешћу рандомизовано да примају ГОЛТОР 10/20 мг дневно (н = 4.650) или плацебо (н = 4.620) (медијан праћења од 4.9 година), л "инциденција миопатије износила је 0,2% за ГОЛТОР и 0,1% за плацебо (видети одељак 4.8).
У клиничкој студији у којој су пацијенти са високим ризиком од кардиоваскуларних болести лечени симвастатином од 40 мг / дан (медијан праћења 3,9 година), учесталост миопатије била је приближно 0,05% за пацијенте. Не-Кинези (н = 7,367) наспрам 0,24% за кинеске пацијенте (н = 5.468). Иако је једина азијска популација процењена у овој клиничкој студији била Кинези, треба бити опрезан при прописивању ГОЛТОР -а азијским пацијентима и нужно се мора користити најнижа доза.
Смањена функционалност транспортних протеина
Смањена функција транспортних протеина ОАТП у јетри може повећати системску изложеност симвастатинској киселини и повећати ризик од миопатије и рабдомиолизе. До оштећења функције може доћи и као резултат инхибиције интеракцијом лекова (нпр. Циклоспорина) и код пацијената носилаца генотипа СЛЦО1Б1 ц. 521Т> Ц.
Пацијенти који носе ген алела СЛЦО1Б1 (ц.521Т> Ц) који кодира мање активан протеин ОАТП1Б1 имају повећану системску изложеност симвастатинској киселини и већи ризик од миопатије. Ризик од миопатије повезан са високом дозом (80 мг) симвастатина је генерално приближно 1%, без генетског тестирања. На основу резултата СЕАРЦХ студије, хомозиготни носачи Ц (који се називају и ЦЦ) лечени са 80 мг имају 15% ризика од миопатије у току једне године, док је ризик код хетерозиготних носилаца хетерозиготног алела Ц (ЦТ) 1,5%. Релативни ризик је 0,3% код пацијената који имају најчешћи генотип (ТТ) (видети одељак 5.2). Ако је доступно, генотипизацију присуства алела Ц треба размотрити као део процене користи и ризика пре прописивања симвастатина у дози од 80 мг појединим пацијентима, а високе дозе, код оних са ЦЦ генотипом, треба избећи. Међутим, одсуство овај ген у генотипизацији не искључује могућност развоја миопатије.
Мерење нивоа креатин киназе
Ниво ЦК не треба мерити након напорних вежби или у присуству било ког другог узрока повећања ЦК јер то може отежати тумачење података. Ако су нивои ЦК значајно повишени на почетку (више од 5 пута од горње границе нормале), треба их поново мерити у року од 5-7 дана да би се резултати потврдили.
Пре третмана
Све пацијенте који започињу терапију ГОЛТОР -ом или повећавају дозу ГОЛТОР -а треба обавестити о ризику од миопатије и упутити их да одмах пријаве сваки необјашњив бол у мишићима, осетљивост и слабост.
Потребан је опрез код пацијената са предиспонирајућим факторима за рабдомиолизу. Да би се установила основна референтна вредност, ниво ЦК треба мерити пре почетка лечења у следећим случајевима:
• старији (старост ≥ 65 година)
• женски пол
• оштећење бубрега
• неконтролисани хипотироидизам
• лична или породична историја наследних мишићних поремећаја
• историја претходних епизода мишићне токсичности са статином или фибратом
• злоупотреба алкохола.
У горенаведеним случајевима, ризик који лечење подразумева мора се одмерити према могућој користи, а у случају лечења препоручује се пажљивије праћење пацијента. Ако је пацијент претходно имао мишићне поремећаје током лечења фибратом или статином, лечење било којим производом који садржи статине (као што је ГОЛТОР) треба започети само опрезно. Ако су нивои ЦК значајно повишени на почетку (више од 5 пута од горње границе нормале), лечење не треба започињати.
Током лечења
Ако током терапије леком ГОЛТОР пацијент пријави бол у мишићима, слабост или грчеве, треба мерити ниво ЦК. У случају значајно повишеног нивоа ЦК (више од 5 пута од горње границе нормале), у одсуству напорних вежби, терапију треба прекинути. Може се размотрити прекид лечења у случају озбиљних мишићних симптома који изазивају свакодневну нелагоду, чак и ако вредности ЦК остану испод 5 пута горње границе нормале. Лечење треба прекинути ако постоји сумња на миопатију из било ког другог разлога.
Ако се симптоми повуку и нивои ЦК се врате у нормалу, може се размотрити поновно увођење ГОЛТОР -а или другог производа који садржи други статин, у најнижој дози и под пажљивим надзором.
Уочена је већа стопа учесталости миопатије код пацијената са титрацијом на 80 мг симвастатина (видети одељак 5.1). Препоручује се периодично мерење нивоа ЦК јер могу бити корисни у идентификацији субклиничких случајева миопатије. Међутим, нема извесности да такво праћење ће спречити миопатију.
ГОЛТОР терапију треба привремено прекинути неколико дана пре велике изборне операције и ако се развије неко веће медицинско или хируршко стање.
Мере за смањење ризика од миопатије изазване интеракцијама лекова (видети такође одељак 4.5)
Ризик од миопатије и рабдомиолизе значајно се повећава истовременом применом ГОЛТОР -а са снажним инхибиторима ЦИП3А4 (попут итраконазола, кетоконазола, посаконазола, вориконазола, еритромицина, кларитромицина, телитромицина, инхибитора протеазе ХИВ -а (нпр. Нелфирцела, бопрепрена, телфирмата), болида ), као и код циклоспорина, даназола и гемфиброзила. Употреба ових лекова је контраиндикована (видети одељак 4.3).
Због присуства симвастатина у ГОЛТОР-у, ризик од миопатије и рабдомиолизе такође се повећава истовременом употребом других фибрата, ниацина у дозама за снижавање липида (≥ 1 г / дан) или истовременом применом амиодарона, амлодипина, верапамила или дилтиазем са неким дозама ГОЛТОР -а (видети одељке 4.2 и 4.5). Ризик од миопатије, укључујући рабдомиолизу, може се повећати при истовременој примени лека ГОЛТОР са фусидатном киселином (видети одељак 4.5).
Сходно томе, што се тиче инхибитора ЦИП3А4, истовремена употреба ГОЛТОР -а са итраконазолом, кетоконазолом, посаконазолом, вориконазолом, инхибиторима ХИВ протеазе (нпр. Нелфинавир), боцепревир, телапревир, еритромицин, кларитромицин, контра телфитромицин (видети одељке 4.3 и 4.5). Ако се не може избећи терапија снажним инхибиторима ЦИП3А4 (агенси који повећавају АУЦ приближно 5 или више пута), лечење ГОЛТОР-ом треба прекинути (и размотрити употребу другог статина) током неки други мање моћни инхибитори ЦИП3А4: флуконазол, верапамил, дилтиазем (видети одељке 4.2 и 4.5). Треба избегавати истовремени унос сока грејпа и ГОЛТОР -а.
Симвастатин се не сме примењивати заједно са фусидатном киселином. Било је извештаја о рабдомиолизи (укључујући неке смртне случајеве) код пацијената који су примали ову комбинацију (видети одељак 4.5). Код пацијената код којих се сматра да је употреба системске фусидатне киселине неопходна, лечење статинима треба прекинути за време трајања терапије фусидатном киселином.Пацијенте треба саветовати да одмах потраже медицинску помоћ ако се појаве симптоми: слабост мишића, бол или осетљивост.
Терапија статином може се поново увести седам дана након последње дозе фусидатне киселине. У изузетним околностима где је потребна продужена системска употреба фусидатне киселине, на пример за лечење тешких инфекција, треба само проценити потребу за истовременом применом ГОЛТОР -а и фусидатне киселине од случаја до случаја под строгим медицинским надзором.
Треба избегавати истовремену примену ГОЛТОР-а у дозама изнад 10 мг / 20 мг дневно и ниацина у дозама за снижавање липида (≥ 1 г / дан) осим ако је вероватноћа да ће клиничка корист надмашити повећани ризик од миопатије (видети одељке 4.2 и 4.5). ).
Ретки случајеви миопатије / рабдомиолизе повезани су са истовременом применом инхибитора ХМГ-ЦоА редуктазе и дозама ниацина (никотинска киселина) које модификују липиде (≥ 1 г / дан), а оба могу изазвати миопатију када се дају сами.
У клиничкој студији (медијан праћења 3,9 година) који је укључивао пацијенте са високим ризиком од кардиоваскуларних болести и са добро контролисаним нивоом ЛДЛ-Ц на симвастатину 40 мг / дан са или без езетимиба 10 мг, није било додатне користи кардиоваскуларни исходи уз додавање доза ниацина (никотинске киселине) које модификују липиде (≥1 г / дан). Стога лекари разматрају комбиновану терапију са симвастатином и дозирају ниацин који модификује липиде (никотинска киселина) (≥ 1 г / дан) или производи који садрже ниацин треба пажљиво да одмере потенцијалне користи и ризике и да пажљиво прате пацијенте ради откривања било каквих знакова или симптома болова у мишићима, осетљивости или слабости, посебно током првих месеци терапије и када се повећавају дозе једног или другог лека .
Осим тога, у овој студији учесталост миопатије била је приближно 0,24% за кинеске пацијенте који су лечени симвастатином од 40 мг или езетимибом / симвастатином 10/40 мг у поређењу са 1,24% за кинеске пацијенте лечене симвастатином. 40 мг или езетимиб / симвастатин 10 / 40 мг заједно са никотинском киселином / ларопипрантом 2.000 мг / 40 мг са модификованим ослобађањем. Иако је једина азијска популација вреднована у овој клиничкој студији била кинеска, будући да је учесталост миопатије већа код кинеских пацијената него код пацијената који нису кинески, истовремена примена ГОЛТОР-а са дозама ниацина (никотинска киселина) може променити профил липида ( ≥ 1 г / дан) не препоручује се азијским пацијентима.
Аципимокс је структурно повезан са ниацином. Иако аципимокс није проучаван, ризик од токсичних ефеката на мишиће може бити сличан оном код ниацина.
Треба избегавати истовремену примену ГОЛТОР -а у дозама изнад 10 мг / 20 мг дневно и амиодарона, амлодипина, верапамила или дилтиазема (видети одељке 4.2 и 4.5).
Пацијенти који узимају друге лекове за које је познато да имају умерен инхибиторни ефекат на ЦИП3А4 у терапијским дозама када се користе истовремено са ГОЛТОР -ом, посебно са већим дозама ГОЛТОР -а, могу имати повећан ризик од миопатије. Ако се ГОЛТОР примењује истовремено са умереним инхибитором ЦИП3А4 (агенси који повећавају АУЦ приближно 2-5 пута), можда ће бити потребно прилагођавање дозе. За неке умерене инхибиторе ЦИП3А4, на пример дилтиазем, препоручује се максимална доза од 10/20 мг ГОЛТОР -а (видети одељак 4.2).
Безбедност и ефикасност ГОЛТОР -а који се примењује са фибратима нису проучавани. Постоји повећан ризик од миопатије када се користи истовремена употреба симвастатина и фибрата (посебно гемфиброзила). Због тога је истовремена употреба ГОЛТОР -а и гемфиброзила контраиндикована (видети одељак 4.3) и не препоручује се истовремена употреба са другим фибратима (видети одељак 4.5).
Ензими јетре
У контролисаним студијама дозирања комбиноване терапије у којима су пацијенти лечени езетимибом и симвастатином, примећено је узастопно повишење трансаминаза (≥3 пута горња граница нормале [ГГН]) (видети одељак 4.8).
У контролисаном клиничком испитивању у коме је више од 9.000 пацијената са хроничном бубрежном болешћу рандомизовано да примају ГОЛТОР 10/20 мг дневно (н = 4.650) или плацебо (н = 4.620) (средњи период праћења од 4.9 година), учесталост узастопно повећање трансаминаза (> 3 пута ГГН) било је 0,7% за ГОЛТОР и 0,6% за плацебо (видети одељак 4.8).
Препоручује се да се пре почетка терапије леком ГОЛТОР спроведу тестови функције јетре, а затим када је клинички индиковано. Пацијенти са титрацијом на дозу од 10 мг / 80 мг треба да се подвргну додатном тесту пре титрације, 3 месеца након титрације до дозе од 10 мг / 80 мг, и периодично након тога (нпр. Сваких шест месеци) током прве године лечења. Посебну пажњу треба обратити на пацијенте код којих се развије повишена концентрација трансаминаза у серуму, а код ових пацијената треба одмах поновити крвне претраге и након тога их обављати чешће. Ако нивои трансаминаза показују доказе прогресије, нарочито ако се повећају до 3 пута изнад горње границе горње границе и упорни су, лечење лековима треба прекинути. Имајте на уму да АЛТ може настати из мишића, стога повећање АЛТ и ЦК може указивати на миопатију (види горе) Миопатија / рабдомиолиза).
Било је ретких постмаркетиншких извештаја о фаталној и нефаталној инсуфицијенцији јетре код пацијената који су узимали статине, укључујући симвастатин. Ако се током лечења леком ГОЛТОР појави озбиљна повреда јетре са клиничким симптомима и / или хипербилирубинемијом или жутицом, одмах прекините терапију. Ако се не пронађе алтернативна етиологија, немојте поново започињати терапију леком ГОЛТОР.
ГОЛТОР треба опрезно користити код пацијената који конзумирају значајне количине алкохола.
Хепатична инсуфицијенција
Због непознатих ефеката повећане изложености езетимибу код пацијената са умереним или тешким оштећењем јетре, ГОЛТОР се не препоручује (видети одељак 5.2).
Шећерна болест
Неки докази указују на то да статини, као класни ефекат, повећавају глукозу у крви, а код неких пацијената, са високим ризиком од развоја дијабетеса, могу изазвати ниво хипергликемије тако да је антидијабетичка терапија одговарајућа.
Овај ризик, међутим, надмашује смањење васкуларног ризика уз употребу статина и стога не би требао бити разлог за прекид лијечења статинима.
Пацијенте у ризику (глукоза наташте 5,6 до 6,9 ммол / Л, БМИ> 30 кг / м2, повишени ниво триглицерида, хипертензија) треба пратити и клинички и биохемијски у складу са националним смерницама.
Педијатријски пацијенти (од 10 до 17 година)
Безбедност и ефикасност езетимиба истовремено примењеног са симвастатином код пацијената од 10 до 17 година са хетерозиготном породичном хиперхолестеролемијом процењени су у контролисаној клиничкој студији код адолесцената (Таннер ИИ или више стадијума) и код девојчица у постменархији током најмање годину дана.
У овој ограниченој контролираној студији опћенито није било учинка на сексуални раст или сазријевање дјечака или дјевојчица у адолесценцији, нити било каквог утјецаја на трајање менструалног циклуса код дјевојчица. Међутим, ефекти езетимиба током периода лечења> 33 недеље на полни раст и сазревање нису проучавани (видети одељке 4.2 и 4.8).
Безбедност и ефикасност езетимиба истовремено примењеног са дозама симвастатина већим од 40 мг дневно нису проучаване код педијатријских пацијената старих од 10 до 17 година.
Езетимиб није испитиван код пацијената млађих од 10 година или код девојчица пре менархе (видети одељке 4.2 и 4.8).
Дуготрајна ефикасност терапије езетимибом код пацијената млађих од 17 година за смањење морбидитета и морталитета код одраслих није проучавана.
Пакети
Сигурност и ефикасност езетимиба примењеног са фибратима нису утврђене (видети горе и одељке 4.3 и 4.5).
Антикоагуланти
Ако се ГОЛТОР додаје варфарину, другом кумаринском антикоагулансу или флуиндиону, потребно је адекватно пратити међународни нормализовани однос (видети одељак 4.5).
Интерстицијска болест плућа
Забележени су случајеви интерстицијалне плућне болести код неких статина, укључујући симвастатин, нарочито при дуготрајној терапији (видети одељак 4.8). Симптоми могу укључивати диспнеју, непродуктивни кашаљ и погоршање општег здравља (умор, губитак тежине и грозницу). Ако се сумња да је пацијент развио интерстицијалну болест плућа, терапију ГОЛТОР -ом треба прекинути.
Помоћне твари
Пацијенти са ретким наследним проблемима интолеранције на галактозу, недостатком Лапп лактазе или малапсорпцијом глукозе-галактозе не би требало да узимају овај лек.
04.5 Интеракције са другим лековима и други облици интеракција
Фармакодинамичке интеракције
Интеракције са лековима за снижавање липида који могу изазвати миопатију када се дају сами
Ризик од миопатије, укључујући рабдомиолизу, повећава се током истовремене примене симвастатина са фибратима. Осим тога, „фармакокинетичка интеракција симвастатина са гемфиброзилом узрокује повећање нивоа симвастатина у плазми (види доле, Фармакокинетичке интеракције и одељци 4.3 и 4.4). Ретки случајеви миопатије / рабдомиолизе повезани су са истовременом применом симвастатина и доза ниацина који модификују липиде (≥ 1 г / дан) (видети одељак 4.4).
Фибрати могу повећати излучивање холестерола у жучи, што доводи до холелитијазе.У претклиничкој студији на псима, езетимиб је повећао холестерол у жучи жучне кесе (видети одељак 5.3). Иако је релевантност ових претклиничких података за људе непозната, не препоручује се истовремена примена лека ГОЛТОР са фибратима (видети одељак 4.4).
Фармакокинетичке интеракције
Препоруке за прописивање агенаса у интеракцији сажете су у следећој табели (додатни детаљи су укључени у текст; видети такође одељке 4.2, 4.3 и 4.4).
Ефекти других лекова на ГОЛТОР
ГОЛТОР
Ниацин: У студији на 15 здравих одраслих особа, истовремена употреба ГОЛТОР -а (10 мг / 20 мг дневно током 7 дана) довела је до малог повећања средњих вредности АУЦ ниацина (22 %) и никотинуринске киселине (19 %), узимајући у обзир као НИАСПАН таблете са продуженим ослобађањем (1.000 мг током 2 дана и 2.000 мг током 5 дана узетих након доручка са ниским садржајем масти). У истој студији, истовремена употреба НИАСПАН -а довела је до благог повећања средњих вредности АУЦ езетимиба (9%), укупног езетимиба (26%), симвастатина (20%) и симвастатинске киселине (35%). одељци 4.2 и 4.4).
Нису спроведена испитивања интеракција лекова са већим дозама симвастатина.
Езетимибе
Антациди: Истовремена примена антацида смањила је стопу апсорпције езетимиба, али није утицала на биорасположивост езетимиба. Смањење брзине апсорпције не сматра се клинички значајним.
Колестирамин: истовремена примена холестирамина смањила је средњу површину испод криве (АУЦ) укупног езетимиба (езетимиб + езетимиб-глукуронид) за приближно 55%. Даље смањење холестерола липопротеина ниске густине (ЛДЛ-Ц) услед додавања ГОЛТОР-а холестирамину може се смањити овом интеракцијом (видети одељак 4.2).
Циклоспорин: У студији са осам пацијената након трансплантације бубрега са клиренсом креатинина> 50 мл / мин при стабилним дозама циклоспорина, примена појединачне дозе од 10 мг езетимиба резултирала је повећањем 3,4 пута (распон од 2,3-7,9 пута) средња АУЦ за укупни езетимиб у поређењу са здравом контролном популацијом из друге студије која је лечена само езетимибом (н = 17). У другој студији, пацијент са трансплантацијом са тешком бубрежном инсуфицијенцијом лечен циклоспорином и неколико других лекова показао је 12 пута већа "укупна изложеност" езетимибу у поређењу са сродним контролама леченим само езетимибом. У двопериодној унакрсној студији, од дванаест здравих испитаника, дневна примена 20 мг езетимиба током 8 дана са 100 мг једнократне дозе циклоспорина 7. дан просечан пораст АУЦ циклоспорина за 15% (у распону од један Смањење од 10% и повећање од 51%) у поређењу са једном дозом од само 100 мг циклоспорина. Нису спроведене контролисане студије о утицају истовремене примене езетимиба на изложеност циклоспорину код пацијената са трансплантираном бубрегом. Истовремена примена ГОЛТОР -а и циклоспорина је контраиндикована (видети одељак 4.3).
Пакети: Истовремена примена фенофибрата или гемфиброзила повећала је укупне концентрације езетимиба приближно 1,5, односно 1,7 пута. Иако се ово повећање не сматра клинички значајним, истовремена примена лека ГОЛТОР са гемфиброзилом је контраиндикована, а са другим фибратима се не препоручује (видети одељке 4.3 и 4.4).
Симвастатин
Симвастатин је супстрат цитокрома П450 3А4. Снажни инхибитори цитокрома П450 3А4 повећавају ризик од миопатије и рабдомиолизе повећањем концентрације инхибиторне активности ХМГ-ЦоА редуктазе у плазми током терапије симвастатином. Такви инхибитори укључују итраконазол, кетоконазол, посаконазол, вориконазол, еритромицин, кларитромицин, телитромицин, инхибиторе ХИВ протеазе (нпр. Нелфинавир), боцепревир, телапревир и нефазодон. Време изложености симвастатинској киселини (активном метаболиту бета-хидрокси киселине). Телитромицин је узроковао 11 пута повећање изложености симвастатинској киселини.
Комбинација са итраконазолом, кетоконазолом, посаконазолом, вориконазолом, инхибиторима ХИВ протеазе (нпр. Нелфинавир), боцепревиром, телапревиром, еритромицином, кларитромицином, телитромицином и нефазодоном је контраиндикована, као и са гемфиброзилом и циклоспорим 4.3). Ако је лечење моћним инхибиторима ЦИП3А4 (агенси који повећавају АУЦ приближно 5 или више пута) неизбежно, терапију ГОЛТОР-ом треба прекинути (и размотрити употребу другог статина) током лечења Опрез приликом комбиновања ГОЛТОР-а са неким другим мање снажним инхибиторима ЦИП3А4: флуконазолом, верапамилом или дилтиаземом (видети одељке 4.2 и 4.4).
Флуконазол: Пријављени су ретки случајеви рабдомиолизе повезане са истовременом применом симвастатина и флуконазола. (видети одељак 4.4).
Циклоспорин: ризик од миопатије / рабдомиолизе повећава се истовременом применом циклоспорина са ГОЛТОР -ом; стога је употреба са циклоспорином контраиндикована (видети одељке 4.3 и 4.4). Иако механизам није у потпуности разјашњен, показало се да циклоспорин повећава АУЦ инхибитора ХМГ-ЦоА редуктазе. симвастатинске киселине је вероватно делимично последица инхибиције ЦИП3А4 и / или ОАТП1Б1.
Даназол: ризик од миопатије и рабдомиолизе повећава се истовременом применом даназола са ГОЛТОР -ом; стога је употреба са даназолом контраиндикована (видети одељке 4.3 и 4.4).
Гемфиброзил: гемфиброзил повећава АУЦ киселог метаболита симвастатина за 1,9 пута, вероватно због инхибиције глукуронидације и / или ОАТП1Б1 (видети одељке 4.3 и 4.4). Истовремена примена са гемфиброзилом је контраиндикована.
Фусидатна киселина
Ризик од миопатије, укључујући рабдомиолизу, може се повећати истовременом применом системске фусидатне киселине са статинима. Истовремена примена ове комбинације може изазвати повећање концентрације оба лека у плазми. Механизам ове интеракције (било фармакодинамички или фармакокинетички, или обоје) је још увек непознат. Било је извештаја о рабдомиолизи (укључујући неке смртне случајеве) код пацијената који су примали ову комбинацију. Ако је потребно лечење фусидатном киселином, лечење ГОЛТОР -ом треба прекинути за време трајања терапије фусидатном киселином (видети одељак 4.4).
Амиодарон: ризик од миопатије и рабдомиолизе повећава се истовременом применом амиодарона са симвастатином (видети одељак 4.4). У клиничкој студији, миопатија је пријављена код 6% пацијената лечених симвастатином у дози од 80 мг и амиодароном. Због тога, доза ГОЛТОР -а не би требало да прелази 10 мг / 20 мг дневно код пацијената који примају истовремену терапију амиодароном.
Блокатори калцијумових канала
• Верапамил: Ризик од миопатије и рабдомиолизе повећава се истовременом применом верапамила са симвастатином у дози од 40 мг или 80 мг (видети одељак 4.4).
У фармакокинетичкој студији, истовремена примена симвастатина са верапамилом довела је до 2,3 пута повећања изложености симвастатинској киселини, вероватно делимично због инхибиције ЦИП3А4. Доза ГОЛТОР -а стога не би требало да прелази 10 мг / 20 мг дневно код пацијената који примају истовремену терапију верапамилом.
• Дилтиазем: Ризик од миопатије и рабдомиолизе повећава се истовременом применом дилтиазема са симвастатином у дози од 80 мг (видети одељак 4.4). У фармакокинетичкој студији, истовремена примена дилтиазема и симвастатина изазвала је 2,7 пута повећање изложености симвастатинској киселини, вероватно због инхибиције ЦИП3А4. Доза ГОЛТОР -а стога не би требало да прелази 10 мг / 20 мг дневно код пацијената који примају истовремену терапију са дилтиаземом.
• Амлодипин
Пацијенти на истовременој терапији амлодипином и симвастатином имају повећан ризик од миопатије. У фармакокинетичкој студији, истовремена примена амлодипина изазвала је 1,6 пута повећање изложености симвастатинској киселини, па стога доза ГОЛТОР-а не би требало да прелази 10 мг / 20 мг дневно код пацијената који су истовремено примали амлодипин.
Умерени инхибитори ЦИП3А4
Пацијенти који узимају друге лекове за које је познато да имају умерен инхибиторни ефекат на ЦИП3А4 када се користе истовремено са ГОЛТОР -ом, посебно са већим дозама ГОЛТОР -а, могу имати повећан ризик од миопатије (видети одељак 4.4).
Инхибитори транспортног протеина ОАТП1Б1
Симвастатин киселина је супстрат транспортног протеина ОАТП1Б1. Истовремена примена лекова који су инхибитори транспортног протеина ОАТП1Б1 може довести до повећане концентрације симвастатинске киселине у плазми и повећаног ризика од миопатије (видети одељке 4.3 и 4.4).
Сок од грејпфрута: сок грејпа инхибира цитокром П450 3А4. Истовремени унос симвастатина и велике количине (више од једног литра дневно) сока од грејпа довеле су до 7 пута веће изложености симвастатинске киселине. Унос 240 мл сока од грејпфрута ујутру и симвастатина увече такође је резултирао повећањем од 1,9 пута, па је потребно избегавати унос сока грејпа током лечења ГОЛТОР-ом.
Колхицин: Било је извештаја о миопатији и рабдомиолизи уз истовремену примену колхицина и симвастатина, код пацијената са бубрежном инсуфицијенцијом. Саветује се помно клиничко праћење таквих пацијената који узимају ову комбинацију.
Рифампицин: Пошто је рифампицин снажан индуктор ЦИП3А4, пацијенти који се подвргавају дуготрајној терапији рифампицином (нпр. Лечење туберкулозе) могу доживети губитак ефикасности симвастатина. У фармакокинетичкој студији на здравим добровољцима, површина испод криве концентрације у плазми (АУЦ) симвастатинске киселине смањена је за 93% уз истовремену примену рифампицина.
НиацинПримећени су случајеви миопатије / рабдомиолизе при истовременој примени симвастатина са дозама ниацина који модификују липиде (≥ 1 г / дан) (види одељак 4.4).
Ефекти ГОЛТОР -а на фармакокинетику других лекова
Езетимибе
У претклиничким студијама показало се да езетимиб не индукује ензиме цитокрома П450 који су укључени у метаболизам лека. Нису примећене клинички значајне фармакокинетичке интеракције између езетимиба и лекова који подлежу метаболизму помоћу цитокрома П450 1А2, 2Д6. 2Ц8, 2Ц9 и 3А4 или Н- ацетилтрансфераза.
Антикоагуланти: У студији на дванаест здравих одраслих мушкараца, истовремена примена езетимиба (10 мг једном дневно) није имала значајан утицај на биорасположивост варфарина и протромбинско време. Међутим, било је постмаркетиншких извештаја о повећању међународног нормализованог односа код пацијената који су додали езетимиб у варфарин или флуиндион. видети одељак 4.4).
Симвастатин
Симвастатин нема инхибиторни ефекат на цитокром П450 3А4. Због тога се не очекује дејство симвастатина на концентрације супстанци које се метаболишу путем цитокрома П450 3А4 у плазми.
Орални антикоагуланси: у две клиничке студије, једна код нормалних добровољаца, а друга код пацијената са хиперхолестеролемијом, симвастатин 20-40 мг / дан је умерено потенцирао ефекат кумаринских антикоагуланса; протромбинско време пријављено као Међународни нормализовани однос (ИНР) порасло је са почетне вредности од 1,7 на 1,8, а са почетне вредности од 2,6 на 3,4 код добровољаца и испитаника. Пријављени су врло ретки случајеви повишеног ИНР -а. Код пацијената лечених кумаринским антикоагулансима, протромбинско време треба одредити пре започињања лечења ГОЛТОР -ом и довољно често током раних фаза терапије да се осигура да не дође до значајне промене протромбинског времена. Након што се документује стабилно протромбинско време, протромбинско време се може пратити у интервалима који се рутински препоручују пацијентима на кумаринским антикоагулансима. Ако се промени доза ГОЛТОР -а или се примена прекине, исти поступак се мора поновити. Терапија симвастатином није повезана са крварењем или променама протромбинског времена код пацијената који нису на антикоагулантној терапији.
04.6 Трудноћа и дојење
Трудноћа
Атеросклероза је хронични процес и рутински прекид лекова за снижавање липида током трудноће мора имати занемарљив утицај на дугорочни ризик повезан са примарном хиперхолестеролемијом.
ГОЛТОР
ГОЛТОР је контраиндикован током трудноће. Нема доступних клиничких података о употреби лека ГОЛТОР током трудноће Студије на животињама у комбинованој терапији показале су репродуктивну токсичност (видети одељак 5.3).
Симвастатин
Безбедност примене симвастатина код трудница није утврђена. Нису спроведене контролисане клиничке студије са симвастатином код трудница. Било је ретких извештаја о урођеним абнормалностима након интраутерине изложености инхибиторима ХМГ-ЦоА редуктазе. Међутим, у проспективној анализи приближно 200 трудноћа изложених током првог тромесечја примене симвастатина или другог блиско повезаног инхибитора ХМГ-ЦоА редуктазе, учесталост конгениталних аномалија била је упоредива са оном у општој популацији. Овај број трудноћа био је статистички довољан да се искључи пораст конгениталних аномалија од 2,5 пута или већи од основне инциденције.
Иако нема доказа да се учесталост урођених абнормалности код потомака пацијената лечених симвастатином или другим блиско повезаним инхибиторима ХМГ-ЦоА редуктазе разликује од оне која се примећује у општој популацији, лечење мајки са симвастатином може смањити ниво фетуса мевалоната, прекурсор биосинтезе холестерола. Из тог разлога, ГОЛТОР се не сме користити код жена које су трудне, које желе да затрудне или сумњају да су трудне. Лечење ГОЛТОР -ом треба прекинути за време трајања трудноће или док то није утврђено да жена није трудна (видети одељак 4.3).
Езетимибе
Нема података о употреби езетимиба током трудноће.
Време храњења
ГОЛТОР је контраиндикован током лактације.Студије на пацовима су показале да се езетимиб излучује у млеко. Није познато да ли се активне компоненте ГОЛТОР -а излучују у мајчино млеко (видети одељак 4.3).
04.7 Утицај на способност управљања возилима и машинама
Нису спроведене студије о утицају на способност управљања возилима и рада са машинама.
04.8 Нежељени ефекти
Безбедност лека ГОЛТОР (или истовремена примена езетимиба и симвастатина еквивалентног ГОЛТОР-у) процењивана је у приближно 12.000 пацијената у клиничким студијама.
Учесталости нежељених ефеката класификоване су на следећи начин: врло честе (≥ 1/10), честе ≥ 1/100,
Следећи нежељени ефекти примећени су код пацијената лечених ГОЛТОР -ом (Н = 2.404) и са већом учесталошћу од плацеба (Н = 1.340).
Следећи нежељени ефекти забележени су код пацијената лечених ГОЛТОР -ом (Н = 9,595) и са већом учесталошћу од статина једном датих (Н = 8,883).
Педијатријски пацијенти (од 10 до 17 година)
У студији спроведеној на адолесцентним пацијентима (од 10 до 17 година) са хетерозиготном породичном хиперхолестеролемијом (н = 248), повишење АЛТ и / или АСТ (≥ 3 к ГНК, узастопно) је примећено код 3% (4 пацијента) пацијенти у групи езетимиба / симвастатина наспрам 2% (2 пацијента) пацијената у групи са монотерапијом симвастатином; проценти повећања вредности ЦПК (≥ 10 Кс ГГН) били су 2% (2 пацијента), односно 0%. Нису забележени случајеви миопатије.
Ова студија није била погодна за поређење ретких нежељених реакција на лекове.
Пацијенти са хроничном бубрежном болешћу
У Студији заштите срца и бубрега (СХАРП) (видети одељак 5.1), која је обухватила више од 9.000 пацијената лечених ГОЛТОР -ом 10/20 мг дневно (н = 4.650) или плацебом (н = 4.620), безбедносни профили су били упоредиви током средњи период праћења од 4,9 година. У овој студији су забележени само озбиљни нежељени догађаји и прекиди због било ког нежељеног догађаја. Стопе прекида због нежељених догађаја биле су упоредиве (10,4% код пацијената лечених ГОЛТОР-ом, 9,8% код пацијената који су примали плацебо). Учесталост миопатије / рабдомиолизе била је 0,2% код пацијената лечених ГОЛТОР-ом и 0,1% код пацијената лечених плацебом. Узастопно повећање трансаминаза (> 3к ГГН) се догодило код 0,7% пацијената. ГОЛТОР лечен у односу на 0,6% пацијената који су примали плацебо У овој студији није било статистички значајног повећања учесталости унапред наведених нежељених догађаја, укључујући рак (9,4% за ГОЛТОР, 9,5% за плацебо), хепатитис, холецистектомију или компликације жучних каменаца или панкреатитиса.
Дијагностичка испитивања
У студијама комбинованог дозирања, учесталост клинички значајних повишења серумских трансаминаза (АЛТ и / или АСТ ≥ 3 к ГГН, узастопне вредности) била је 1,7% код пацијената лечених ГОЛТОР -ом. Ова повишења су генерално била асимптоматска. Нису била повезана са холестазом, па су се вратила на почетну вредност након прекида терапије или током лечења (видети одељак 4.4).
Клинички значајно повећање ЦК (≥ 10 Кс ГГН) примећено је код 0,2% пацијената лечених ГОЛТОР -ом.
Постмаркетиншко искуство
Следећи додатни нежељени ефекти пријављени су у постмаркетиншкој употреби са ГОЛТОР-ом или у клиничким испитивањима или током пост-маркетиншке употребе са једном од појединачних компоненти.
Поремећаји крви и лимфног система: тромбоцитопенија; анемија
Поремећаји нервног система: периферна неуропатија; оштећење меморије
Поремећаји дисања, грудног коша и медијастинума: кашаљ; диспнеја; интерстицијска болест плућа (видети одељак 4.4)
Гастроинтестинални поремећаји: констипација; панкреатитис; гастритис
Поремећаји коже и поткожног ткива: алопеција; мултиформни еритем; реакције преосетљивости, укључујући осип, уртикарију, анафилаксију, ангиоедем
Поремећаји мишићно -коштаног система и везивног ткива: грчеви у мишићима; миопатија * (укључујући миозитис); рабдомиолиза са или без акутне бубрежне инсуфицијенције (видети одељак 4.4); тендинопатија, понекад компликована руптуром
* У клиничкој студији, миопатија се често јављала код пацијената лечених симвастатином од 80 мг / дан у поређењу са пацијентима који су примали 20 мг / дан (1,0% према 0,02%, респективно) (видети одељке 4.4 и 4.5).
Поремећаји метаболизма и исхране: смањен апетит
Васкуларни поремећаји: налети врућине; хипертензија
Општи поремећаји и услови на месту примене: Бол
Хепатобилиарни поремећаји: хепатитис / жутица; фатална и нефатална инсуфицијенција јетре; холелитијаза; холециститис
Поремећаји репродуктивног система и дојке: еректилна дисфункција
Психијатријски поремећаји: депресија, несаница
Ретко су пријављивани привидни синдром преосетљивости, укључујући неке од следећих: ангиоедем, синдром сличан лупусу, полимијалгија реуматика, дерматомиозитис, васкулитис, тромбоцитопенија, еозинофилија, повећана брзина седиментације еритроцита, артритис и артралгија, уртикарија, фотосензитивност, грозница, налети врућине, пискање и малаксалост.
Испитивања: повишена алкална фосфатаза; абнормални тест функције јетре.
Код статина, укључујући симвастатин, забележено је повећање нивоа ХбА1ц и концентрације глукозе у серуму наташте.
Било је ретких постмаркетиншких извештаја о когнитивним оштећењима (нпр. Губитак памћења, заборав, амнезија, оштећење памћења, конфузија) повезани са употребом статина, укључујући симвастатин. Извештаји су генерално били неозбиљни. И реверзибилни након прекида терапије статинима, са различитим временима за почетак симптома (1 дан до година) и отклањањем симптома (средња 3 недеље).
Следећи додатни нежељени догађаји су забележени код неких статина:
• Поремећаји спавања, укључујући ноћне море
• Сексуална дисфункција
• Дијабетес мелитус: учесталост ће зависити од присуства или одсуства фактора ризика (глукоза у крви наташте ≥ 5,6 ммол / Л, БМИ> 30 кг / м2, повишени ниво триглицерида, историја хипертензије).
04.9 Предозирање
ГОЛТОР
У случају предозирања потребно је примијенити симптоматске и потпорне мјере. Истовремена примена езетимиба (1.000 мг / кг) и симвастатина (1.000 мг / кг) добро се подносила у студијама акутне оралне токсичности на мишевима и пацовима. Код ових животиња нису примећени клинички знаци токсичности. Орална процјена ЛД50 за обје врсте била је езетимиб ≥ 1.000 мг / кг / симвастатин ≥ 1.000 мг / кг.
Езетимибе
У клиничким студијама, примена езетимиба, 50 мг / дан, на 15 здравих испитаника до 14 дана, или 40 мг / дан на 18 пацијената са примарном хиперхолестеролемијом до 56 дана, генерално се добро подносила. Пријављено је неколико случајева предозирања; већина њих није била повезана са нежељеним ефектима. Пријављени нежељени ефекти нису били озбиљни. Код животиња, није примећена токсичност након једнократних оралних доза од 5.000 мг / кг езетимиба код пацова и мишева и 3.000 мг / кг код паса.
Симвастатин
Пријављено је неколико случајева предозирања; максимална узета доза је 3,6 г. Сви пацијенти су се опоравили без последица.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: инхибитори ХМГ-ЦоА редуктазе у комбинацији са другим фармаколошким средствима која модификују профил липида.
АТЦ ознака: Ц10БА02.
ГОЛТОР (езетимиб / симвастатин) је производ за снижавање липида који селективно инхибира цревну апсорпцију холестерола и сродних биљних стерола и инхибира ендогену синтезу холестерола.
Механизам дејства:
ГОЛТОР
Холестерол у плазми потиче из цревне апсорпције и ендогене синтезе.ГОЛТОР садржи езетимиб и симвастатин, два једињења за снижавање липида са комплементарним механизмима деловања. ГОЛТОР смањује повишене нивое укупног холестерола (укупног-Ц), ЛДЛ-Ц, аполипопротеина Б (Апо Б), триглицерида (ТГ), липопротеина липопротеина високе густине (Ц-нон-ХДЛ) и повећава холестерол високог холестерола липопротеина густине (ХДЛ-Ц) кроз двоструку инхибицију апсорпције и синтезе холестерола.
Езетимибе
Езетимиб инхибира цревну апсорпцију холестерола. Езетимиб је орално активан и има механизам деловања који се разликује од механизама деловања других класа супстанци за снижавање холестерола (нпр. Статини, секвестранти жучних киселина [смоле], деривати влакнасте киселине и биљни станоли). Молекуларна мета езетимиба је транспортер стерола , Ниеманн-Пицк Ц1-Лике 1 (НПЦ1Л1), одговоран за апсорпцију холестерола и фитостерола у цревима.
Езетимиб је локализован на нивоу ивице четкице танког црева и инхибира апсорпцију холестерола, узрокујући смањење проласка цревног холестерола у јетру; статини смањују синтезу холестерола у јетри и ова два различита механизма производе комплементарно смањење холестерола. У двонедељној клиничкој студији на 18 пацијената са хиперхолестеролемијом, езетимиб је инхибирао интестиналну апсорпцију холестерола за 54% у поређењу са плацебом.
Спроведен је низ претклиничких студија како би се утврдила селективност езетимиба у инхибирању апсорпције холестерола.Езетимиб је инхибирао апсорпцију [14Ц] -холестерола без утицаја на апсорпцију триглицерида, масних киселина, жучних киселина, прогестерона, етинил естрадиола, или витамине А и Д. растворљиве у мастима.
Симвастатин
Након оралног узимања, симвастатин, који је неактиван лактон, хидролизује се у јетри у одговарајући облик активне бета-хидрокси киселине која има снажно инхибиторно деловање на ХМГ-ЦоА редуктазу (3-хидрокси-3-метилглутарил ЦоА редуктазу). Овај ензим катализује конверзију ХМГ-ЦоА у мевалонат, рани и ограничавајући корак у биосинтези холестерола.
Показало се да симвастатин смањује и нормалне и повишене концентрације ЛДЛ-Ц. ЛДЛ се формира од липопротеина врло ниске густине (ВЛДЛ) и углавном се катаболише помоћу ЛДЛ рецептора високог афинитета. Ц-ВЛДЛ) и индукцијом ЛДЛ рецептора, што доводи до смањења производње и повећања катаболизма ЛДЛ-Ц. Аполипопротеин Б се такође значајно смањује током лечења симвастатином.Симвастатин такође умерено повећава ХДЛ-Ц и смањује ТГ у плазми. Као резултат ових промена, односи између укупног холестерола / ХДЛ-Ц и ЛДЛ-Ц / Ц-ХДЛ су смањени.
КЛИНИЧКА СТУДИЈА
У контролисаним клиничким испитивањима, ГОЛТОР је значајно смањио укупни Ц, ЛДЛ-Ц, Апо Б, ТГ и не-ХДЛ-Ц и повећао ХДЛ-Ц код пацијената са хиперхолестеролемијом.
Примарна хиперхолестеролемија
У осмонедељној, двоструко слепој, плацебом контролисаној студији, 240 пацијената са хиперхолестеролемијом који су већ били на монотерапији симвастатином и који нису успели да постигну циљ ЛДЛ-Ц према Националном програму за образовање о холестеролу (НЦЕП) (од 2, 6 до 4,1 ммол / л [100 до 160 мг / дл у зависности од основних карактеристика) рандомизирани су да примају езетимиб 10 мг или плацебо поред своје већ постојеће терапије симвастатином. нису достигли основни циљ ЛДЛ-Ц (~ 80%), значајно више пацијената рандомизираних на езетимиб који су примали симвастатин постигло је циљ ЛДЛ-Ц на крају студије у поређењу са пацијентима рандомизираним на плацебо који су примали истовремено са симвастатином, 76% и 21,5%, респективно.
Одговарајуће смањење ЛДЛ-Ц за езетимиб или плацебо примењено истовремено са симвастатином било је значајно различито (27% односно 3%).
Штавише, езетимиб, примењен истовремено са терапијом симвастатином, значајно је смањио укупне Ц, Апо Б, ТГ у поређењу са плацебом који се примењивао истовремено са симвастатином.
У 24-недељној двоструко слепој мултицентричној студији, 214 пацијената са дијабетесом меллитусом типа 2 лечено је тиазолидиндионима (росиглитазон и пиоглитазон) најмање 3 месеца и симвастатином 20 мг најмање 6 недеља са просечним ЛДЛ-2,4 ммол / л (93 мг / дл), били су рандомизирани да примају симвастатин 40 мг или истовремену примену активних супстанци еквивалентних ГОЛТОР 10 мг / 20 мг. ГОЛТОР 10 мг / 20 мг био је знатно ефикаснији од удвостручавања дозе симвастатина на 40 мг у даљем смањењу ЛДЛ-Ц (-21% и 0%, респективно), укупног Ц (-14% и -1%, респективно), АпоБ (-14% и -2%, респективно) и Ц-нон-ХДЛ (-20% и -2%, респективно) у односу на смањења примећена код 20 мг симвастатина. Резултати за ХДЛ-Ц и ТГ између два групе третмана нису биле значајно различите и на резултате није утицала врста третмана тиазолидиндионима.
Ефикасност различитих јачина ГОЛТОР-а (10 мг / 10 мг до 10 мг / 80 мг / дан) доказана је у 12-недељној, двоструко слепој, плацебом контролисаној, мултицентричној студији која је укључивала све дозе. све повезане дозе симвастатина.
Када се упореде пацијенти лечени свим дозама ГОЛТОР-а са пацијентима који су лечени свим дозама симвастатина, ГОЛТОР је значајно смањио укупне-Ц, ЛДЛ-Ц и ТГ (видети Табелу 1) и такође Апо Б (-42% и -29%, респективно) , нон-ХДЛ-Ц (-49% и -34%, респективно) и Ц-реактивни протеин (-33% и -9%, респективно). Ефекти ГОЛТОР-а на ХДЛ-Ц били су слични ефектима који су примећени код симвастатина. "Даља анализа показала је да је ГОЛТОР значајно повећао ХДЛ-Ц у поређењу са плацебом.
Табела 1
Одговор на ГОЛТОР код пацијената са примарном хиперхолестеролемијом
(средња променаа% од почетне вредности у одсуству третманаб)
а За триглицериде, медијан% одступања од почетне вредности
б Базално - не у лечењу лековима за снижавање липида
ц Комбиноване дозе ГОЛТОР-а (10 / 10-10 / 80) значајно су смањиле укупни Ц, ЛДЛ-Ц и ТГ, у поређењу са симвастатином, и значајно повећале ХДЛ-Ц у поређењу са плацебом.
У слично дизајнираној студији, резултати за све параметре липида били су генерално конзистентни. У комбинованој анализи ове две студије, липидни одговор на ГОЛТОР био је сличан код пацијената са нивоима ТГ већим или мањим од 200 мг / дЛ.
У мултицентричном, двоструко слепом, контролисаном клиничком испитивању (ЕНХАНЦЕ), 720 пацијената са хетерозиготном породичном хиперхолестеролемијом било је рандомизовано да примају 10 мг езетимиба у комбинацији са 80 мг симвастатина (н = 357) или 80 мг симвастатина (н = 363) током 2 године. Примарни циљ студије био је испитати ефекат комбиноване терапије езетимиб / симвастатин на дебљину тунике интиме и медија (ИМТ) каротидне артерије у поређењу са самим симвастатином. Утицај овог маркера још није доказан. Сурогат за кардиоваскуларни морбидитет и морталитет.
Примарна крајња тачка, средња промена ИМТ свих шест каротидних сегмената, није се значајно разликовала (п = 0,29) између две групе третмана на основу ултразвучних мерења у Б режиму. Уз езетимиб 10 мг у комбинацији са симвастатином 80 мг или само симвастатином 80 мг, дебљина интиме и медијалних туника се повећала за 0,0111 мм и 0,0058 мм, респективно, током двогодишњег трајања студије (на почетку, средње мерење ИМТ каротида било је 0,68 мм и 0,69 мм).
Езетимиб 10 мг у комбинацији са 80 мг симвастатина смањио је ЛДЛ-Ц, укупни Ц, Апо Б и ТГ значајно више од 80 мг симвастатина.За две групе лечења проценат повећања Ц-ХДЛ био је сличан. Нежељене реакције пријављене са 10 мг езетимиба у комбинацији са 80 мг симвастатина биле су у складу са познатим безбедносним профилом.
ГОЛТОР садржи симвастатин. У два велика плацебом контролисана клиничка испитивања, Скандинавска студија преживљавања симвастатина (20-40 мг н = 4.444 пацијената) е Студија заштите срца (40 мг; Н = 20.536 пацијената), ефекат терапије симвастатином процењиван је код пацијената са високим ризиком од коронарних догађаја услед континуиране коронарне болести срца, дијабетеса, периферне васкуларне болести, историје можданог удара или друге цереброваскуларне болести. Лечење симвастатином има показано је да смањују: ризик од укупног морталитета кроз смањење смртности услед ЦХД; ризик од нефаталног инфаркта миокарда и можданог удара; и потребу за операцијом са коронарном и некоронарном реваскуларизацијом.
Студија ефикасности додатног смањења холестерола и хомоцистеина (СЕАРЦХ) проценила је ефекат лечења симвастатином у дози од 80 мг наспрам 20 мг (медијан праћења од 6,7 година) на велике васкуларне догађаје (МВЕ; дефинисано као фатално исхемично срце болест, нефатални инфаркт миокарда, поступак коронарне реваскуларизације, нефатални или фатални мождани удар или поступак периферне реваскуларизације) код 12.064 пацијената са историјом инфаркта миокарда. Није било значајне разлике у учесталости МВЕ између 2 групе; симвастатин 20 мг (н = 1.553; 25,7%) у односу на 80 мг симвастатина (н = 1.477; 24,5%); РР 0,94, 95%ЦИ: 0,88 до 1, 01. Апсолутна разлика у нивоу ЛДЛ-Ц између две групе током ток студије био је 0,35 ± 0,01 ммол / Л. Безбедносни профили су били слични између две групе лечења, осим „инциденције миопатије која је била приближно 1,0% код пацијената лечених са симвастатин 80 мг у поређењу са 0,02% код пацијената лечених са 20 мг. Отприлике половина ових случајева миопатије догодила се током прве године лечења. Учесталост миопатије током сваке наредне године лечења била је приближно 0,1%.
Показало се да ГОЛТОР смањује велике кардиоваскуларне догађаје код пацијената са хроничном бубрежном болешћу; међутим, повећање користи ГОЛТОР -а за кардиоваскуларни морбидитет и морталитет у поређењу са оним које је показано за симвастатин није дефинитивно утврђено.
Клиничке студије код педијатријских пацијената (старости од 10 до 17 година)
У мултицентричној, двоструко слепој, контролисаној студији, 142 дечака (Таннер ИИ стадијум и више) и 106 постменарцхе девојчица, од 10 до 17 година (просечна старост 14,2 године) са хетерозиготном породичном хиперхолестеролемијом (ИФ хетерозиготна) са почетним нивоом ЛДЛ-Ц вредности између 4,1 и 10,4 ммол / Л рандомизиране су у езетимиб 10 мг истовремено примењен са симвастатином (10, 20 или 40 мг) или симвастатином (10, 20 или 40 мг) самим током 6 недеља, езетимибом и симвастатином у дози од 40 мг заједно -примењиван или симвастатин 40 мг сам у наредних 27 недеља, а затим су се езетимиб и симвастатин (10 мг, 20 мг или 40 мг) примењивали заједно отворене етикете током 20 недеља.
У 6. недељи, езетимиб истовремено примењен са симвастатином (све дозе) значајно је смањио укупни Ц (38% наспрам 26%), ЛДЛ-Ц (49% наспрам 34%), Апо Б (39% наспрам 27%) и не- ХДЛ-Ц (47% наспрам 33%) у односу на сам симвастатин (све дозе). Резултати су били слични између две групе за лечење ТГ и ХДЛ-Ц (-17% наспрам -12% и +7% наспрам +6%, респективно) У 33. недељи, резултати су били у складу са онима у 6. недељи и значајно више пацијената на езетимибу и симвастатину од 40 мг (62%) постигло је „идеалан терапијски циљ према НЦЕП ААП (
Безбедност и ефикасност езетимиба истовремено примењеног са дозама симвастатина већим од 40 мг дневно нису испитиване код педијатријских пацијената старости од 10 до 17 година. Ефикасност није испитивана код пацијената млађих од 17 година. Дуготрајна терапија езетимибом у смањењу морбидитета и морталитета у одраслој доби.
Хомозиготна породична хиперхолестеролемија (Хомозиготна ИФ)
Двонедељна, двоструко слепа, рандомизирана студија изведена је код пацијената са клиничком и / или генотипском дијагнозом хомозиготне ИФ. Анализирани су подаци подгрупе пацијената (н = 14) који су на почетку лечени симвастатином од 40 мг. Повећање дозе симвастатина са 40 на 80 мг (н = 5) резултирало је смањењем ЛДЛ-Ц за 13% у односу на почетну вредност у поређењу са 40 мг симвастатина. Истовремена примена езетимиба и симвастатина еквивалентног ГОЛТОР-у (10 мг / 40 мг и 10 мг / 80 мг комбиновано, н = 9) резултирало је смањењем ЛДЛ-Ц за 23% у односу на почетну вредност у поређењу са симвастатином од 40 мг. ), дошло је до смањења ЛДЛ-Ц за 29% у односу на почетну вредност у поређењу са симвастатином од 40 мг.
Превенција великих васкуларних догађаја код хроничне бубрежне болести (ЦКД)
Студија заштите срца и бубрега (СХАРП) била је мултинационална, рандомизована, плацебо контролисана, двоструко слепа студија на 9.438 пацијената са хроничном бубрежном болешћу, од којих је једна трећина на почетку била на дијализи. Укупно 4.650 пацијената је распоређено на ГОЛТОР 10/20, а 4.620 на плацебо, а праћено је просечно 4,9 година. Пацијенти су имали просечну старост од 62 године и 63% су били мушкарци, 72% белци, 23% дијабетичари, а за оне који нису на дијализи, просечна процењена брзина гломеруларне филтрације (еГФР) била је 26,5 мл / мин. / 1,73 м2. нема критеријума за укључивање у испитивање засновано на липидима. Просечна основна вредност ЛДЛ-Ц била је 108 мг / дЛ. Након годину дана, укључујући пацијенте који више нису узимали испитивани лек, ЛДЛ-Ц је смањен за 26% у поређењу са плацебом само са 20 мг симвастатина и за 38 % од ГОЛТОР 10/20 мг.
Примарно поређење специфицирано у СХАРП протоколу била је „анализа намере лечења„ великих васкуларних догађаја “(МВЕ; дефинисана као нефатални инфаркт миокарда или срчана смрт, мождани удар или било који поступак реваскуларизације) само код оних пацијената који су у почетку били рандомизовани на ГОЛТОР (н = 4,193) или плацебо (н = 4,191) групе. Секундарне анализе су укључивале исти композит анализиран за целу рандомизовану кохорту (основна студија или 1 година) на ГОЛТОР (н = 4,650) или плацебо (н = 4,620) као као и компоненте овог композита.
Анализа примарне крајње тачке показала је да је ГОЛТОР значајно смањио ризик од великих васкуларних догађаја (749 пацијената са плацебом у односу на 639 у групи ГОЛТОР) са релативним смањењем ризика за 16% (п = 0,001).
Међутим, дизајн ове студије није дозволио засебан допринос монокомпонентног езетимиба ефикасности како би се значајно смањио ризик од великих васкуларних догађаја код пацијената са КББ.
Појединачне компоненте МВЕ код свих рандомизованих пацијената приказане су у Табели 2. ГОЛТОР је значајно смањио ризик од можданог удара и било које реваскуларизације, без значајних нумеричких разлика у корист ГОЛТОР-а за нефатални инфаркт миокарда и срчану смрт.
Табела 2
Велики васкуларни догађаји према групи лечења код свих рандомизованих пацијената у СХАРПа -и
Анализа с намером да се лечи на свим СХАРП пацијентима рандомизованим на ГОЛТОР или плацебо на почетку или након 1 године
б МАЕ; дефинисан као композит нефаталног инфаркта миокарда, коронарне смрти, нехеморагијског можданог удара или било које реваскуларизације
Апсолутно смањење ЛДЛ холестерола постигнуто са ГОЛТОР-ом било је ниже код пацијената са нижим основним ЛДЛ-Ц (
Аортна стеноза
Симвастатин и Езетимиб за лечење стенозе аорте (СЕАС) били су мултицентрична, двоструко слепа, плацебом контролисана студија са просечним трајањем од 4,4 године код 1,873 пацијената са асимптоматском аортном стенозом (АС), документована брзином вршног протока аорте мереном Доплер између 2,5 и 4,0 м / с. Уписани су само пацијенти за које се сматрало да лечење статинима није потребно ради смањења ризика од атеросклеротичне кардиоваскуларне болести. Пацијенти су рандомизирани у омјеру 1: 1 за истовремену примјену плацеба или езетимиба 10 мг и симвастатина 40 мг дневно.
Примарни крајњи циљ био је скуп великих кардиоваскуларних догађаја (МЦЕ) који се састојао од кардиоваскуларне смрти, хируршке замене аортног вентила (АВР), конгестивне срчане инсуфицијенције (ЦХФ) која је резултат прогресије АС, нефаталног инфаркта миокарда, премоснице коронарне артерије (ЦАБГ) )), перкутана коронарна интервенција (ПЦИ), хоспитализација због нестабилне ангине пекторис и нехеморагичног можданог удара Кључне секундарне крајње тачке биле су сложени подскупови категорија догађаја примарне крајње тачке.
У поређењу са плацебом, езетимиб / симвастатин 10/40 мг није значајно смањио ризик од МЦЕ. Примарни исход догодио се код 333 пацијената (35,3%) у групи која је примала езетимиб / симвастатин и код 355 пацијената (38,2%) у групи која је примала плацебо (однос опасности у групи езетимиб / симвастатин, 0,96; интервал поверења 95%, 0,83 до 1,12; п = 0,59) Замена аортног вентила изведена је код 267 пацијената (28,3%) у групи која је примала езетимиб / симвастатин и код 278 пацијената (29,9%) у плацебо групи (однос ризика, 1,00; 95%ЦИ, 0,84 до 1,18; п = 0,97) Мање пацијената је имало исхемијске кардиоваскуларне догађаје у групи која је примала езетимиб / симвастатин (н = 148) у поређењу са плацебо групом (н = 187) (однос ризика, 0,78; 95% ЦИ, 0,63 до 0,97; п = 0,02), углавном због мањем броју пацијената који су подвргнути премосници коронарне артерије.
Рак се чешће јављао у групи езетимиба / симвастатина (105 наспрам 70, п = 0,01). Клиничка важност овог запажања је неизвесна јер у већој студији СХАРП укупан број пацијената са било којом врстом инциденцијалног карцинома (438 у групи езетимиба / симвастатина наспрам 439 у групи која је примала плацебо) није био другачији па самим тим ни исход СЕАС -а студија није могла потврдити СХАРП.
05.2 Фармакокинетичка својства
Нису примећене значајне фармакокинетичке интеракције током истовремене примене езетимиба и симвастатина.
Апсорпција :
ГОЛТОР
ГОЛТОР је биоеквивалент за истовремену примену езетимиба и симвастатина.
Езетимибе
Након оралне примене, езетимиб се брзо и опсежно апсорбује коњугиран са фармаколошки активним фенолним глукуронидом (езетимиб-глукуронид). Средње вршне концентрације у плазми (Цмак) се примећују у року од 1-2 сата за езетимиб-глукуронид и 4 -12 сати за езетимиб. апсолутна биорасположивост езетимиба не може се одредити јер је једињење практично нерастворљиво у воденом медијуму погодном за ињекције.
Истовремена употреба хране (оброци са високим или немасним садржајем масти) није утицала на оралну биорасположивост езетимиба у таблетама од 10 мг.
Симвастатин
Утврђено је да је доступност активног а -хидрокси киселине у системској циркулацији након оралне дозе симвастатина мања од 5% дозе, што је у складу са опсежном екстракцијом јетре првим проласком. Главни метаболити симвастатина присутни у људској плазми су? -хидрокси киселина и четири друга активна метаболита.
Профили укупних и активних инхибитора у плазми нису се променили применом симвастатина непосредно пре стандардног оброка у поређењу са постом.
Дистрибуција :
Езетимибе
Езетимиб и езетимиб-глукуронид везују се 99,7%, односно 88-92% за протеине хумане плазме.
Симвастатин
Симвастатин и П -хидрокси киселина везани су за протеине хумане плазме (95%).
Фармакокинетика симвастатина у једној и више доза није показала накупљање лека након више доза. У свим горе наведеним фармакокинетичким студијама, максимална концентрација инхибитора била је 1,3 до 2,4 сата након дозе.
Биотрансформација :
Езетимибе
Езетимиб се метаболише првенствено у танком цреву и јетри путем коњугације глукуронида (реакција фазе ИИ) са накнадним излучивањем путем жучи. Минимални оксидативни метаболизам (реакција фазе И) примећен је код свих процењених врста. Езетимиб и езетимиб глукуронид су главна једињења изведена из лекова која се налазе у плазми и чине приближно 10-20% односно 80-90% укупног лека присутног у плазми. И езетимиб и езетимиб-глукуронид се полако елиминишу из плазме са доказима значајног ентерохепатичног циклуса Полувреме езетимиба и езетимиб-глукуронида је приближно 22 сата.
Симвастатин
Симвастатин је неактиван лактон који се брзо хидролизује ин виво у одговарајућој а -хидроксикиселини, снажном инхибитору ХМГ -ЦоА редуктазе, хидролиза се јавља углавном у јетри; брзина хидролизе у људској плазми је веома спора.
Код људи, симвастатин се добро апсорбује и пролази кроз хитну екстракцију првог пролаза у јетри.Екстракција у јетри зависи од протока крви у јетри. Јетра је његово примарно место деловања, са накнадним излучивањем еквивалентних супстанци у жучи. Доступност активног лека у системској циркулацији је стога ниска.
Након интравенозне примене метаболита а -хидроксикиселине, његов средњи полуживот је био 1,9 сати.
Елиминација :
Езетимибе
Након оралне примене 14Ц езетимиба (20 мг) код људи, укупни езетимиб је чинио приближно 93% укупне радиоактивности у плазми. Отприлике 78% и 11% примијењене радиоактивности пронађено је у фецесу и урину, током периода од 10 дана прикупљања узорака. Након 48 сати није било мјерљивих нивоа радиоактивности у плазми.
Симвастатин
Симвастатин киселина се активно транспортује до хепатоцита преко носача ОАТП1Б1.
Након оралне дозе симвастатина код људи, 13% радиоактивности се излучило урином, а 60% изметом у року од 96 сати. Након интравенозне примене метаболита а -хидроксикиселине, само просечно 0,3% интравенозне дозе се излучило урином као инхибитори.
Посебне популације:
Педијатријски пацијенти
Апсорпција и метаболизам езетимиба слични су код деце и адолесцената (од 10 до 18 година) и одраслих. На основу укупног езетимиба нема фармакокинетичких разлика између адолесцената и одраслих.Фармакокинетички подаци у ситостеролемији педијатријске популације (видети одељак 4.2).
Геријатријски пацијенти
Концентрација укупног езетимиба у плазми приближно је двоструко већа код старијих особа (≥ 65 година) него код младих (18-45 година). Смањење ЛДЛ-Ц и безбедносни профил упоредиви су код старијих и млађих појединаца који су лечени езетимибом (видети одељак 4.2 ).
Хепатична инсуфицијенција
Након примене појединачне дозе езетимиба од 10 мг, средња површина испод криве (АУЦ) укупног езетимиба повећала се приближно 1,7 пута код пацијената са благим оштећењем јетре (Цхилд Пугх скор 5 или 6), у поређењу са здравим субјектима. У 14-дневној студији са више доза (10 мг / дан) код пацијената са умереним оштећењем јетре (Цхилд Пугх скор 7 до 9), средња АУЦ за укупни езетимиб повећала се приближно 4 пута дневно 1 и 14. дана у поређењу са здравим субјектима. Није потребно прилагођавање дозе код пацијената са благим оштећењем јетре. Због непознатих ефеката повећане изложености езетимибу код пацијената са умереним или тешким оштећењем јетре (Цхилд Пугх скор> 9), езетимиб се не препоручује код ових пацијената (видети одељке 4.2. И 4.4).
Инсуфицијенција бубрега
Езетимибе
Након једне дозе езетимиба од 10 мг код пацијената са тешком бубрежном болешћу (н = 8; средња вредност ЦрЦл ≤30 мл / мин), средња АУЦ за укупни езетимиб повећала се приближно 1,5 пута у поређењу са здравим субјектима. (Н = 9), (видети одељак 4.2).
Додатни пацијент у овој студији (након трансплантације бубрега и лечен вишеструком терапијом лековима, укључујући циклоспорин) имао је 12 пута "изложеност" укупном езетимибу.
Симвастатин
У студији са пацијентима са тешким оштећењем бубрега (клиренс креатинина
Сек
Концентрације укупног езетимиба у плазми су нешто веће (приближно 20%) код жена него код мушкараца.Снижење ЛДЛ-Ц и безбедносни профил упоредиви су међу мушкарцима и женама леченим езетимибом.
СЛЦО1Б1 полиморфизам
Носиоци алела ц.521Т> Ц гена СЛЦО1Б1 су смањили активност ОАТП1Б1. Средња изложеност (АУЦ) главном активном метаболиту, симвастатинској киселини, износи 120% у хетерозиготним носачима алела Ц (ЦТ) и 221% у хомозиготни носачи (ЦЦ) у поређењу са пацијентима који имају најчешћи генотип (ТТ) .Алел Ц има учесталост 18% у европској популацији. Постоји ризик од повећане изложености симвастатинској киселини код пацијената са полиморфизмом СЛЦО1Б1, што може довести до повећаног ризика од рабдомиолизе (видети одељак 4.4).
05.3 Предклинички подаци о безбедности
ГОЛТОР
У студијама истовремене примене са езетимибом и симвастатином уочени су токсични ефекти у суштини они који су типично повезани са статинима. Неки од токсичних ефеката били су израженији од оних који су примећени само уз примену статина. Ово се приписује фармакокинетичким и / или фармакодинамичким интеракцијама у истовременој примени. До оваквих интеракција није дошло у клиничким испитивањима. Епизоде миопатије догодиле су се код пацова тек након излагања дозама неколико пута већим од терапијске дозе код људи (приближно 20 пута ниво АУЦ за симвастатин и 1800 пута ниво АУЦ за активни метаболит). Није било доказа да истовремена примена езетимиба има утицаја на миотоксични потенцијал симвастатина.
Код паса истовремено примењених са езетимибом и статинима, при ниској изложености (хиперплазија жучних канала, накупљање пигмента, инфилтрација мононуклеарних ћелија и мали хепатоцити). Ове промене нису настале са излагањем продуженим дозама до 14 месеци. Општи опоравак резултата теста јетре примећен је након престанка излагања. Ови подаци су у складу са онима описаним са инхибиторима ХМГ-ЦоА или се приписују веома ниским нивоима холестерола постигнутим код паса који се проучавају.
Истовремена примена езетимиба и симвастатина није била тератогена код пацова. Ограничен број скелетних деформитета (фузија каудалних пршљенова, смањен број каудалних пршљенова) примећен је код трудних женки зечева.
У низу есеја ин виво И ин витро Езетимиб, примењен сам или симултано са симвастатином, није показао генотоксични потенцијал.
Езетимибе
Студије хроничне токсичности на животињама са езетимибом нису идентификовале циљне органе за токсичне ефекте.Код паса који су 4 недеље лечени езетимибом (≥ 0,03 мг / кг / дан) концентрација холестерола у жучи порасла је за 2,5 до 3,5 пута. Међутим, у једногодишњој студији на псима која је третирана дозама до 300 мг / кг / дан није примећена повећана инциденција холелитијазе или других хепатобилиарних ефеката. Клиничка вредност ових података за људе није позната. Не може се искључити ризик од литогенезе повезан са терапијском употребом езетимиба.
Дуготрајни тестови карциногености на езетимибу били су негативни.
Езетимиб није имао утицаја на плодност ни у једном полу код пацова, није откривена тератогеност код пацова или зечева, нити је пре- или постнатални развој измењен. кг / дан.
Симвастатин
На основу конвенционалних фармакодинамичких студија на животињама, токсичности при поновљеним дозама, генотоксичности и карциногенезе, нема других ризика за пацијента осим оних који се очекују на основу фармаколошког механизма. У максимално толерисаним дозама код пацова и зечева, симвастатин није резултирао малформацијама фетуса и није имао ефекта на плодност, репродуктивну функцију или неонатални развој.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Бутилхидроксианизол
Монохидрат лимунске киселине
Натријум кроскармелоза
Хипромелоза
Лактоза монохидрат
Магнезијум стеарат
Микрокристална целулоза
Пропил галат
06.2 Некомпатибилност
Није битно.
06.3 Период важења
2 године.
06.4 Посебне мере предострожности при складиштењу
Не чувати на температури изнад 30 ° Ц.
Блистер: Чувати у оригиналном паковању ради заштите лека од светлости и влаге.
Боце: Држите бочицу добро затворену да бисте заштитили лек од светлости и влаге.
06.5 Природа непосредног паковања и садржај паковања
ГОЛТОР 10 мг / 10 мг, 10 мг / 20 мг и 10 мг / 40 мг
Бела боца од полиетилена високе густине (ХДПЕ) са затварачем од полипропилена отпорног на децу и силикатним гелом за сушење, запечаћена посебним језичком, који садржи 100 таблета.
ГОЛТОР 10 мг / 10 мг
ПВЦ / алуминијум полиамидни блистер заварен на алуминијумску фолију помоћу винилне смоле. Таблете се могу извадити притиском на пластични џеп.
Једнослојни блистер од ПВЦ / алуминијум полиамида заварен на алуминијумску фолију помоћу винилне смоле. Таблете се могу извадити притиском на пластични џеп, паковања од 30, 50, 100 или 300 таблета.
ГОЛТОР 10 мг / 20 мг, 10 мг / 40 мг
Непрозирни блистер од полихлоротрифлуороетилена / ПВЦ -а запечаћен на алуминијумску фолију помоћу винилне смоле. Таблете се могу извадити притиском на пластични џеп, паковање од 90 таблета.
ГОЛТОР 10 мг / 20 мг, 10 мг / 40 мг и 10 мг / 80 мг
Непрозирни блистер од полихлоротрифлуороетилена / ПВЦ -а запечаћен на алуминијумску фолију помоћу винилне смоле. Таблете се могу извадити притиском на пластични џеп, паковања од 7, 10, 14, 28, 30, 50, 56, 84, 98, 100 или 300 таблета.
Једнодозни блистер од полихлоротрифлуороетилена / ПВЦ-а запечаћен на алуминијумску фолију помоћу винилне смоле. Таблете се могу извадити притиском на пластични џеп, паковања од 30, 50, 100 или 300 таблета.
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Нема посебних упутстава.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
ДОДАЈТЕ ПХАРМА Срл
Виале Схакеспеаре, 47
00144 Рим
Продавац на продају:
СИГМА-ТАУ Индустрие Фармацеутицхе Риуните С.п.А.
Виа Понтина км 30,400
00040 Помезиа (РМ)
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
100 таблета у бочици од 10 мг / 10 мг АИЦ н. 036678011
7 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678023
10 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678035
14 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678047
28 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678050
30 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678100
50 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678062
56 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678074
98 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678086
2 к 49 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678643
100 таблета у блистерима од 10 мг / 10 мг АИЦ н. 036678098
300 таблета у блистер паковањима од 10 мг / 10 мг АИЦ н. 036678112
30 таблета у блистерима са једном дозом од 10 мг / 10 мг АИЦ н. 036678124
50 таблета у блистерима са једном дозом од 10 мг / 10 мг АИЦ н. 036678136
100 таблета у блистерима са једном дозом од 10 мг / 10 мг АИЦ н. 036678148
300 таблета у блистерима са једном дозом од 10 мг / 10 мг АИЦ н. 036678163
100 таблета у бочици од 10 мг / 20 мг АИЦ н. 036678151
7 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678175
10 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678187
14 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678199
28 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678201
30 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678213
50 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678225
56 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678237
98 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678249
100 таблета у блистерима од 10 мг / 20 мг АИЦ н. 036678252
300 таблета у блистер паковањима од 10 мг / 20 мг АИЦ н. 036678264
30 таблета у блистерима са једном дозом од 10 мг / 20 мг АИЦ н. 036678276
50 таблета у блистерима са једном дозом од 10 мг / 20 мг АИЦ н. 036678288
100 таблета у блистерима са једном дозом од 10 мг / 20 мг АИЦ н. 036678290
300 таблета у блистерима са једном дозом од 10 мг / 20 мг АИЦ н. 036678302
100 таблета у бочици од 10 мг / 40 мг АИЦ н. 036678314
7 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678326
10 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678338
14 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678340
28 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678353
30 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678365
50 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678377
56 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678389
98 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678391
100 таблета у блистерима од 10 мг / 40 мг АИЦ н. 036678403
300 таблета у блистер паковањима од 10 мг / 40 мг АИЦ н. 036678415
30 таблета у блистерима са једном дозом од 10 мг / 40 мг АИЦ н. 036678427
50 таблета у блистерима са једном дозом од 10 мг / 40 мг АИЦ н. 036678439
100 таблета у блистерима од 10 мг / 40 мг са једном дозом АИЦ н. 036678441
300 таблета у блистерима са једном дозом од 10 мг / 40 мг АИЦ н. 036678454
7 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678466
10 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678478
14 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678480
28 таблета у блистерима од 10 мг / 80 мг АИЦ н. 036678492
30 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678504
50 таблета у блистерима од 10 мг / 80 мг АИЦ н. 036678516
56 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678528
98 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678530
100 таблета у блистер паковањима од 10 мг / 80 мг АИЦ н. 036678542
300 таблета у блистерима од 10 мг / 80 мг АИЦ н. 036678555
30 таблета у блистерима са једном дозом од 10 мг / 80 мг АИЦ н. 036678567
50 таблета у блистерима са једном дозом од 10 мг / 80 мг АИЦ н. 036678579
100 таблета у блистерима са једном дозом од 10 мг / 80 мг АИЦ н. 036678581
300 таблета у блистерима са једном дозом од 10 мг / 80 мг АИЦ н. 036678593
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: август 2005
Последњи датум обнове: фебруар 2010
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
Марта 2015