Активни састојци: Есомепразол
ЛУЦЕН 20 мг гастрорезистентне таблете
ЛУЦЕН 40 мг гастрорезистентне таблете
Луцен уметци за паковање су доступни за величине паковања: - ЛУЦЕН 20 мг гастрорезистентне таблете, ЛУЦЕН 40 мг гастрорезистентне таблете
- ЛУЦЕН 10 мг гастрорезистентне грануле за оралну суспензију, у кесицама
- ЛУЦЕН 40 мг прашак за раствор за ињекцију / инфузију
Индикације Зашто се Луцен користи? За шта је то?
ЛУЦЕН садржи лек који се зове есомепразол. Припада групи лекова који се зову „инхибитори протонске пумпе“, који делују тако што смањују количину киселине коју производи желудац.
ЛУЦЕН се користи за лечење следећих поремећаја:
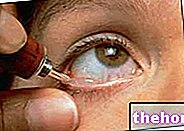
- „Гастроезофагеална рефлуксна болест“ (ГЕРБ). Јавља се када киселина из желуца побегне у једњак (цев која повезује грло са желуцем), узрокујући бол, упалу и печење.
- Чир на желуцу или горњем цреву инфициран бактеријом која се назива „Хелицобацтер пилори". Ако имате ова стања, лекар вам може прописати и антибиотике за лечење инфекције и омогућити чир да зацели.
- Чир на желуцу изазван лековима који се зову НСАИЛ (нестероидни антиинфламаторни лекови). ЛУЦЕН се такође може користити за спречавање стварања чира на желуцу током узимања НСАИЛ.
- Вишак желудачне киселине узрокован тумором у панкреасу (Золлингер-Еллиссонов синдром).
- Продужено лечење поновног крварења чирева, након превенције интравенозном применом Луцена
Контраиндикације Када се Луцен не сме користити
Немојте узимати ЛУЦЕН:
- ако сте алергични (преосетљиви) на есомепразол или неки други састојак овог лека (наведен у одељку: Додатне информације).
- ако сте алергични на друге лекове који спречавају протонску пумпу (нпр. пантопразол, лансопразол, рабепразол, омепразол).
- ако узимате лек који садржи нелфинавир (користи се за лечење ХИВ -а).
Не бисте требали узимати ЛУЦЕН ако падне у било који од горе наведених случајева. Ако сте у недоумици, посаветујте се са лекаром или фармацеутом пре него што узмете ЛУЦЕН.
Предострожности при употреби Шта треба да знате пре него што узмете лек Луцен
Будите посебно пажљиви са ЛУЦЕН -ом
Разговарајте са својим лекаром или фармацеутом пре него што узмете ЛУЦЕН ако:
- Имате озбиљне проблеме са јетром
- Имате озбиљне проблеме са бубрезима.
ЛУЦЕН може прикрити симптоме других болести. Стога, ако вам се нешто догоди од следећег пре него што почнете да узимате или док узимате ЛУЦЕН, одмах обавестите свог лекара:
- Губите пуно килограма без разлога или имате проблема са гутањем
- Појављује се бол у стомаку или лоша пробава
- Почните повраћати храну или крв
- Столице су црне (крваве столице).
Ако вам је прописан ЛУЦЕН према потреби, обратите се свом лекару ако симптоми потрају или промене карактеристике.
Ако узимате инхибитор протонске пумпе као што је ЛУЦЕН, нарочито дуже од годину дана, можда ћете имати мало повећан ризик од прелома кука, ручног зглоба или кичме. Ако имате остеопорозу или узимате кортикостероиде (што може повећати ризик од остеопороза) консултујте свог лекара
Интеракције Који лекови или храна могу променити ефекат Луцена
Обавестите свог лекара или фармацеута ако узимате или сте недавно узимали било које друге лекове, укључујући и лекове који се набављају без рецепта.
Заиста, ЛУЦЕН може утицати на начин на који неки лекови делују, а неки лекови могу утицати на ЛУЦЕН.Не треба да узимате ЛУЦЕН ако узимате лек који садржи нелфинавир (користи се за лечење ХИВ -а).
Обавестите свог лекара или фармацеута ако узимате неки од следећих лекова:
- Атазанавир (користи се за лечење ХИВ -а)
- Клопидогрел (користи се за спречавање крвних угрушака)
- Кетоконазол, итраконазол или вориконазол (користе се за лечење инфекција изазваних гљивицама).
- Ерлотиниб (користи се за лечење рака).
- Циталопрам, имипрамин или кломипрамин (користе се за лечење депресије).
- Диазепам (користи се за лечење анксиозности, за опуштање мишића или код епилепсије).
- Фенитоин (користи се у епилепсији) Ако узимате фенитоин, ваш лекар ће морати да вас прати када започињете или прекидате лечење леком ЛУЦЕН.
- Лекови који се користе за разређивање крви, попут варфарина. Ваш лекар ће вас можда надгледати када започнете или прекинете терапију леком ЛУЦЕН.
- Цилостазол (користи се за лечење повремене клаудикације - бол у ногама при ходању због недовољног снабдевања крвљу).
- Цисаприд (користи се за варење и горушицу).
- Дигоксин (користи се за срчане проблеме).
- Метотрексат (лек за хемотерапију који се користи у високим дозама за лечење рака) - ако узимате високе дозе метотрексата, ваш лекар може привремено прекинути лечење Луценом.
- Такролимус (користи се за трансплантацију органа)
- Рифампицин (користи се за лечење туберкулозе).
- Кантарион (Хиперицум перфоратум) (користи се за лечење депресије).
Ако вам је лекар преписао антибиотике као што су амоксицилин и кларитромицин са ЛУЦЕН -ом за лечење чирева изазваних инфекцијом Хелицобацтер пилори, веома је важно да обавестите лекара о другим лековима.
Упозорења Важно је знати да:
Трудноћа и дојење
Пре него што узмете ЛУЦЕН, обавестите свог лекара ако сте трудни или желите да затрудните. Питајте свог лекара или фармацеута за савет пре него што узмете било који лек. Ваш лекар ће одлучити да ли можете да узмете ЛУЦЕН за то време.
Није познато да ли ЛУЦЕН прелази у мајчино млеко, па не треба да узимате ЛУЦЕН ако дојите.
Узимање ЛУЦЕНА са храном и пићем
Таблете се могу узимати на пун стомак или на празан желудац.
Вожња и управљање машинама
Није вероватно да ће ЛУЦЕН утицати на вашу способност управљања возилима или рада са алатима или машинама.
Важне информације о неким од састојака ЛУЦЕНА
ЛУЦЕН гастрорезистентне таблете садрже сахарозу која је врста шећера. Ако вам је лекар рекао да „не подносите неке шећере, консултујте га пре узимања лека.
Дозирање и начин употребе Како се користи Луцен: Дозирање
Увек узимајте ЛУЦЕН тачно онако како вам је рекао лекар. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
- ЛУЦЕН гастрорезистентне таблете се не препоручују деци млађој од 12 година
- Ако сте дуго узимали овај лек, ваш лекар ће вас пратити (нарочито ако сте узимали овај лек дуже од годину дана)
- Ако вам је лекар рекао да узимате лек по потреби, по потреби, реците свом лекару ако се симптоми промене.
Узимање лека
- Таблете можете узети у било које доба дана.
- Таблете можете узети на пун стомак или на празан стомак.
- Таблете прогутајте целе уз пиће воде. Немојте жвакати или дробити таблете јер садрже обложене грануле које штите лек од желучане киселости, па је важно не оштетити грануле.
Шта учинити ако имате проблема са гутањем таблета
Ако имате проблема са гутањем таблета:
- Ставите таблете у чашу мирне воде. Не смеју се користити друге течности
- Мешајте док се таблете не отопе (смеша неће имати јасан изглед). Попијте одмах или бар у року од 30 минута. Увек их помешајте пре пијења
- Да бисте били сигурни да сте узели сав лек, чашу темељито исперите тако што ћете је до пола напунити водом и напитком. Чврсте честице садрже лек и не смеју се жвакати нити дробити.
Ако апсолутно не можете да прогутате, таблету можете помешати са мало воде, уметнути у шприц и применити кроз цевчицу директно у желудац (желудац).
Колико лекова треба узети
- Ваш лекар ће вас посаветовати о броју таблета које треба узимати и колико дуго. Ово је функција вашег физичког стања, старости и стања јетре.
- Уобичајене дозе дате су испод.
Лечење жгаравице узроковане гастроезофагеалном рефлуксном болешћу (ГЕРБ):
Одрасли и деца од 12 година:
- Ако је ваш лекар утврдио да вам је једњак благо оштећен, уобичајена доза је једна 40 мг ЛУЦЕН гастрорезистентна таблета једном дневно током 4 недеље. Ваш лекар ће вам можда рећи да наставите са узимањем исте дозе још 4 недеље, у случају да једњак није излечио.
- Након зарастања једњака, уобичајена доза је једна ЛУЦЕН гастрорезистентна таблета од 20 мг једном дневно.
- Ако једњак није оштећен, уобичајена доза је једна ЛУЦЕН 20 мг гастрорезистентна таблета сваки дан. Када су симптоми под контролом, лекар ће вас обавестити да можете узети лек по потреби, највише један гастро- отпорне таблете.Луцен 20 мг дневно.
- Ако имате тешке проблеме са јетром, лекар ће вам дати мању дозу.
Лечење чирева изазваних инфекцијом Хелицобацтер пилори и спречавање њиховог поновног појављивања:
- Одрасли од 18 година па надаље: уобичајена доза је једна ЛУЦЕН 20 мг гастрорезистентна таблета два пута дневно током једне недеље.
- Ваш лекар ће вам такође рећи да узимате антибиотике који се зову амоксицилин и кларитромицин.
Лечење чира на желуцу изазваног НСАИЛ (нестероидним антиинфламаторним лековима):
- Одрасли од 18 година па надаље: уобичајена доза је једна ЛУЦЕН 20 мг гастрорезистентна таблета једном дневно током 4 до 8 недеља.
Превенција чира на желуцу ако узимате НСАИЛ (нестероидне антиинфламаторне лекове):
- Одрасли од 18 година па надаље: уобичајена доза је једна ЛУЦЕН 20 мг гастрорезистентна таблета једном дневно.
Лечење вишка желудачне киселине узроковано растом панкреаса (Золлингер-Еллисонов синдром):
- Одрасли од 18 година па надаље: уобичајена доза је једна ЛУЦЕН 40 мг гастрорезистентна таблета два пута дневно.
- Ваш лекар ће прилагодити дозу у складу са вашим потребама и такође ће одлучити колико дуго треба наставити лечење.
Максимална доза је 80 мг два пута дневно.
Продужено лечење поновног крварења чирева, након превенције интравенозном применом Луцена:
Уобичајена доза је једна таблета Луцен од 40 мг једном дневно током 4 недеље.
Предозирање Шта учинити ако сте узели превише Луцена
Ако сте узели више лека ЛУЦЕН него што је требало
Ако сте узели више лека ЛУЦЕН него што вам је прописао лекар, одмах обавестите свог лекара или фармацеута.
Ако сте заборавили да узмете ЛУЦЕН
- Ако сте заборавили да узмете дозу ЛУЦЕНА, узмите је чим се сетите. Ако је скоро време за следећу дозу, прескочите пропуштену.
- Немојте узети двоструку дозу (две дозе истовремено) да бисте надокнадили заборављену дозу.
Нежељени ефекти Који су нежељени ефекти Луцена
Као и сви лекови, ЛУЦЕН може изазвати нежељена дејства, мада се она не морају јавити код свих.
Ако приметите било који од следећих озбиљних нежељених ефеката, престаните са узимањем лека ЛУЦЕН и одмах се обратите лекару:
- Нагло пискање, отицање усана, језика и грла или тела, осип, несвестица или тешкоће при гутању (тешка алергијска реакција).
- Црвенило коже са пликовима или љуштењем. Озбиљни пликови и крварење могу се појавити и на уснама, очима, устима, носу и гениталијама. Ово може бити „Стевенс-Јохнсонов синдром“ или „токсична епидермална некролиза“.
- Жута кожа, тамни урин и умор могу бити симптоми проблема са јетром. Ови ефекти су ретки, погађају мање од 1 на 1000 људи.
Остали нежељени ефекти укључују:
Честе (јављају се у мање од 1 на 10 особа):
- Главобоља.
- Ефекти на желудац или црева: дијареја, бол у стомаку, затвор, надутост.
- Мучнина или повраћање.
Мање често (јављају се у мање од 1 на 100 људи):
- Отицање стопала и глежњева.
- Поремећен сан (несаница).
- Вртоглавица, игле и игле, поспаност.
- Вртоглавица.
- Сува уста
- Промјене у крвним претрагама које провјеравају рад јетре.
- Осип на кожи, осип и свраб.
- Прелом кука, зглоба или кичме (ако се Луцен користи у високим дозама и дуже време).
Ретко (јављају се код мање од 1 на 1.000 људи):
- Проблеми са крвљу, као што је смањени број белих крвних зрнаца и тромбоцита. То може узроковати слабост, модрице или могућност лакшег добијања инфекције.
- Низак ниво натријума у крви. То може изазвати слабост, повраћање и грчеве.
- Осећај узнемирености, збуњености или депресије.
- Промене у укусу.
- Проблеми са видом, као што је замагљен вид.
- Нагло пискање или отежано дисање (бронхоспазам).
- Запаљење унутрашњости уста.
- Инфекција звана "дрозд" која може утицати на црева и изазвана је гљивицама.
- Проблеми с јетром, укључујући жутицу која може узроковати жуту кожу, тамни урин и умор.
- Губитак косе (алопеција).
- Осип на кожи при излагању сунцу.
- Бол у зглобовима (артралгија) или у мишићима (миалгија).
- Општи осећај лошег осећаја и недостатка снаге.
- Повећано знојење.
Веома ретко (јављају се код мање од 1 на 10.000 људи):
- Промене у броју крвних зрнаца, укључујући агранулоцитозу (недостатак белих крвних зрнаца).
- Агресија.
- Видети, осетити или чути ствари којих нема (халуцинације).
- Озбиљни проблеми с јетром који доводе до отказивања јетре и упале мозга.
- Изненадни почетак озбиљног осипа или стварања пликова или љуштења коже. Ово може бити повезано са високом температуром и боловима у зглобовима (мултиформни еритем, Стевенс-Јохнсонов синдром, токсична епидермална некролиза).
- Слабост мишића.
- Озбиљни проблеми са бубрезима.
- Повећање груди код мушкараца.
Није познато (учесталост се не може проценити из доступних података)
- Ако узимате ЛУЦЕН дуже од три месеца, ниво магнезијума у крви може пасти. Низак ниво магнезијума може се манифестовати умором, невољним контракцијама мишића, дезоријентацијом, конвулзијама, вртоглавицом, повећањем откуцаја срца. Ако имате било који од ових симптома, одмах се обратите лекару. Низак ниво магнезијума такође може довести до смањења нивоа калијума или калцијума у крви. Ваш лекар треба да одлучи да ли ће повремено проверавати ниво магнезијума у крви.
- Упала у цревима (доводи до дијареје).
ЛУЦЕН у врло ретким случајевима може утицати на бела крвна зрнца што доводи до имунодефицијенције. Ако имате инфекцију са симптомима као што је грозница са озбиљним погоршањем општег физичког стања или грозница са симптомима локалне инфекције, као што су бол у врату, грлу или устима или отежано мокрење, требало би да посетите лекара што је пре могуће да се недостатак белих крвних зрнаца (агранулоцитоза) може искључити тестом крви. Важно је да дате информације о лековима које узимате. Не брините због горе наведене листе могућих нежељених ефеката. Можда их нећете добити. Ако неко од нежељених дејстава постане озбиљно или ако приметите било које нежељено дејство које није наведено у овом упутству, молимо вас да то кажете свом лекару или фармацеуту.
Истек и задржавање
- Чувати ван домашаја и погледа деце.
- Не чувати на температури изнад 30 ° Ц.
- Чувати у оригиналном паковању (блистер) или држати посуду добро затворену (боца) ради заштите од влаге.
- Немојте користити таблете након истека рока ваљаности (ЕКСП) наведеног на кутији, новчанику или блистеру. Датум истека се односи на последњи дан у месецу.
- Лекове не треба одлагати у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
ОСТАЛЕ ИНФОРМАЦИЈЕ
Шта ЛУЦЕН садржи
Активни састојак је есомепразол. ЛУЦЕН гастрорезистентне таблете присутне су у 2 јачине које садрже 20 или 40 мг есомепразола (у облику магнезијум трихидрата).
Помоћни састојци су: глицерол моностеарат 40-55, хипролоза, хипромелоза, оксид гвожђа (црвено-смеђи, жути) (Е172, само за таблете од 20 мг), магнезијум стеарат, кополимер етил акрилата метакрилне киселине (1: 1) дисперзија на 30 %, микрокристална целулоза, синтетички парафин, макроголи, полисорбат 80, кросповидон, натријум стеарил фумарат, сфере сахарозе (сахароза и кукурузни скроб), талк, титанијум диоксид (Е171), триетил цитрат.
Опис изгледа ЛУЦЕН -а и садржај паковања
- ЛУЦЕН 20 мг гастрорезистентне таблете су светло розе боје са А / ЕХ на једној страни и 20 мг на другој.
- ЛУЦЕН 40 мг гастрорезистентне таблете су розе боје са А / ЕИ на једној страни и 40 мг на другој.
- Таблете су у блистер паковањима, новчаницима и / или бочицама које садрже
- 20 мг, 40 мг: бочица са 2-5-7-14-15-28-30-56-60-100-140 (28к5) таблета.
- 20 мг, 40 мг: блистер или новчаник блистер од 3-7-7к1-14-15-25к1-28-30-50к1- 56-60-90-98-100к1-140 таблета.
Не могу се на тржиште ставити све величине паковања
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ЛУЦЕНТИС 10 МГ / МЛ раствор за убризгавање
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ
Један мл садржи 10 мг ранибизумаба *. Свака бочица садржи 2,3 мг ранибизумаба у 0,23 мл раствора.
* Ранибизумаб је фрагмент хуманизованог моноклоналног антитела произведен у ћелијама Есцхерицхиа цоли технологијом рекомбинантне ДНК.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Раствор за ињекције
Бистри, безбојни до бледо жути водени раствор.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Луцентис је индициран код одраслих за:
• Лечење старосне неоваскуларне (влажне) макуларне дегенерације (АМД)
• Лечење оштећења вида узрокованог дијабетичким едемом макуле (ДМЕ)
• Лечење оштећења вида узрокованог „макуларним едемом који је последица оклузије вене мрежњаче (грана РВО или централни РВО)
• Лечење оштећења вида узроковано хороидалном неоваскуларизацијом (ЦНВ) секундарно патолошкој кратковидости (ПМ)
04.2 Дозирање и начин примене
Луцентис треба да даје квалификовани офталмолог са искуством у интравитреалним ињекцијама.
Дозирање за лечење мокрог АМД
Препоручена доза Луцентиса је 0,5 мг која се даје месечно као једна интравитреална ињекција. Ово одговара убризганој запремини од 0,05 мл.
Третман се примењује месечно и наставља се док се не постигне максимална оштрина вида, тј. Оштрина вида пацијента је стабилна за три узастопне месечне контроле које се раде током лечења ранибизумабом.
Због тога је потребно месечно пратити оштрину вида пацијената.
Третман треба наставити ако праћење укаже на смањење видне оштрине услед влажног АМД -а. Затим би требало применити месечне ињекције док се поново не постигне стабилна оштрина вида за три узастопне месечне контроле (то подразумева најмање две ињекције). Интервал између две дозе не сме бити мањи од месец дана.
Дозирање за лечење оштећења вида узрокованог ДМЕ -ом или макуларним едемом који је последица РВО -а
Препоручена доза Луцентиса је 0,5 мг која се даје месечно као једна интравитреална ињекција. Ово одговара убризганој запремини од 0,05 мл.
Третман се примењује месечно и наставља се док се не постигне максимална оштрина вида, тј. Оштрина вида пацијента је стабилна за три узастопне месечне контроле које се раде током лечења ранибизумабом. Ако нема побољшања видне оштрине током прве три ињекције, не препоручује се наставак лечења.
Због тога је потребно месечно пратити оштрину вида пацијената.
Третман треба наставити када праћење укаже на смањену оштрину вида услед ДМЕ -а или макуларног едема који је последица РВО -а. Затим би требало применити месечне ињекције све док се поново не постигне стабилна оштрина вида за три месечне контроле. Узастопно (ово укључује најмање две ињекције). Интервал између две дозе не би требало да буде мањи од месец дана.
Луцентис и ласерска фотокоагулација у ДМЕ и макуларни едем секундарни према БРВО
Постоји одређено искуство у примени Луцентиса истовремено са ласерском фотокоагулацијом (видети одељак 5.1). Када се даје истог дана, Луцентис треба дати најмање 30 минута након ласерске фотокоагулације. Луцентис се може дати пацијентима који су претходно примили ласерску фотокоагулацију.
Дозирање за лечење оштећења вида узрокованог ЦНВ -ом секундарно у односу на ПМ
Лечење треба започети једном ињекцијом.
Ако се праћењем открију знаци активности болести, као што је смањена оштрина вида и / или знаци повреде, препоручује се даље лечење.
Праћење болести може укључивати клинички преглед, оптичку кохерентну томографију (ОЦТ) или флуоресцеинску ангиографију (ФА).
Док је неким пацијентима можда потребна само једна или две ињекције током прве године лечења, некима ће можда бити потребно чешће лечење (видети одељак 5.1). Због тога се препоручује месечно праћење током прва два месеца, а најмање свака три месеца током прве године лечења. Након прве године, лекар може одредити учесталост праћења.
Интервал између две дозе не сме бити мањи од месец дана.
Луцентис и фотодинамичка терапија са Висудине -ом у ЦНВ секундарно у односу на ПМ
Нема искуства са применом Луцентиса у комбинацији са Висудинеом.
Посебне популације
Хепатична инсуфицијенција
Луцентис није проучаван код пацијената са инсуфицијенцијом јетре. Међутим, за овај став нису потребна посебна разматрања.
Инсуфицијенција бубрега
Није потребно прилагођавање дозе код пацијената са бубрежном инсуфицијенцијом (видети одељак 5.2).
Старији грађани
Код старијих особа није потребно прилагођавање дозе. Постоји „ограничено“ искуство код пацијената са ДМЕ старијим од 75 година.
Педијатријска популација
Безбедност и ефикасност лека Луцентис код деце и адолесцената млађих од 18 година нису утврђени. Нема доступних података.
Начин примене
Бочице за једнократну употребу само за интравитреалну употребу.
Пре примене Луцентиса треба визуелно проверити на присуство честица и промену боје.
Поступак за ињекцију мора се извести под асептичним условима, који укључују дезинфекцију руку као и за било који хируршки захват, стерилне рукавице, стерилну завесу и стерилни блефаростат (или еквивалент) и могућност извођења стерилне парацентезе (ако је потребно анамнезу реакција преосетљивости пацијента треба пажљиво проценити пре интравитреалне процедуре (видети одељак 4.4). У складу са клиничком праксом, пре ињекције треба применити одговарајућу анестезију и локални антимикробни лек широког спектра за дезинфекцију периокуларне, очне и капне површине.
За информације о припреми Луцентиса погледајте одељак 6.6.
Ињекциону иглу убаците 3,5-4,0 мм позади лимбуса, у комору стакластог тела, избегавајући хоризонтални меридијан и усмеравајући иглу према центру очне јабучице. Убризгати ињекциону запремину од 0,05 мл; променити склерално место за наредне ињекције.
04.3 Контраиндикације
Преосетљивост на активну супстанцу или било коју помоћну супстанцу наведену у одељку 6.1.
Пацијенти са тренутним или сумњивим окуларним или периокуларним инфекцијама.
Пацијенти са сталном тешком интраокуларном упалом.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Реакције повезане са интравитреалном ињекцијом
Интравитреалне ињекције, укључујући оне са Луцентисом, биле су повезане са ендофталмитисом, интраокуларном упалом, регматогеним одвајањем мрежњаче, руптуром мрежњаче и јатрогеном трауматском катарактом (видети одељак 4.8). За примену Луцентиса увек треба користити одговарајуће технике асептичког убризгавања. Осим тога, пацијенте треба пратити недељу дана након ињекције како би се омогућило брзо лечење у случају инфекције. Пацијенте треба упутити како да без одлагања пријаве све симптоме који указују на ендофталмитис или било који од горе наведених догађаја.
Повећање очног притиска
У року од 60 минута од ињекције Луцентиса примећено је пролазно повећање очног притиска (ИОП). Такође је примећено продужено повећање интраокуларног притиска (видети одељак 4.8). Интраокуларни притисак и перфузију главе оптичког нерва треба пратити и на одговарајући начин лечити.
Билатерални третман
Ограничени подаци о билатералној употреби Луцентиса (укључујући дозирање истог дана) не указују на повећан ризик од системских нежељених догађаја у поређењу са унилатералним третманом.
Имуногеност
Са Луцентисом постоји потенцијал за имуногеност. С обзиром да постоји могућност повећане системске изложености код испитаника са ДМЕ, не може се искључити повећани ризик од развоја преосетљивости у овој популацији пацијената. Пацијенте такође треба едуковати о томе како пријавити ако се интраокуларна упала погорша јер би то могао бити клинички симптом који се може приписати стварање интраокуларних антитела.
Истовремена употреба са другим анти-ВЕГФ (васкуларни ендотелни фактор раста)
Луцентис се не сме примењивати истовремено са другим анти-ВЕГФ лековима (системским или окуларним).
Луцентис прекид
Не треба давати дозу и не треба наставити лечење пре следећег заказаног третмана у случају:
• смањење најбоље кориговане оштрине вида (БЦВА) ≥30 слова у односу на последњу процену;
• интраокуларни притисак ≥30 ммХг;
• прекид мрежњаче;
• "субретинално крварење које се протеже до центра фовее, или ако је опсег крварења ≥50% укупне површине лезије";
• интраокуларна операција изведена или планирана у претходних или наредних 28 дана.
Пуцање пигментног епитела ретине
Фактори ризика повезани са настанком руптуре пигментног епитела ретине након анти-ВЕГФ терапије за влажни АМД укључују велико и / или високо одвајање пигментног епитела ретине. Приликом започињања терапије Луцентисом, потребан је опрез код пацијената са овим факторима ризика за пуцање ретиналног пигментног епитела.
Регматогено одвајање мрежњаче или макуларне рупе
Лечење треба прекинути код особа са регматогеним одвајањем мрежњаче или макуларним рупама стадија 3 или 4.
Становништво са ограниченим подацима
Постоји само ограничено искуство у лечењу субјеката са ДМЕ секундарним у односу на дијабетес типа И. Луцентис није проучаван код пацијената који су претходно примали интравитреалне ињекције, код пацијената са активним системским инфекцијама, пролиферативном дијабетичком ретинопатијом или код пацијената са истовременим медицинским стањима као што је одвајање мрежњаче или макуларна рупа. Такође нема искуства у лечењу Луцентисом код пацијената са дијабетесом са ХбАлц већим од 12% и неконтролисаном хипертензијом. Лекар треба да узме у обзир недостатак информација при лечењу ових пацијената.
Код пацијената са ПМ, постоје ограничени подаци о ефекту Луцентиса код пацијената који су претходно лечени неуспешном фотодинамичком терапијом вертепорфином (вПДТ). Надаље, иако је констатован ефекат забележен код особа са субфовеалним и јукстафовеалним лезијама, нема довољно података о ефекту Луцентиса код ПМ субјеката са екстрафовеалним лезијама.
Системски ефекти након интравитреалне примене
Системски нежељени догађаји, укључујући неокуларне крварења и артеријске тромбоемболијске догађаје, пријављени су након интравитреалне ињекције инхибитора ВЕГФ.
Постоје ограничени подаци о безбедности лечења ДМЕ -а, макуларног едема узрокованог РВО -ом и ЦНВ -ом секундарно у односу на ПМ код пацијената са историјом можданог удара или пролазних исхемијских напада. Посебан опрез је потребан при лечењу таквих пацијената (видети одељак 4.8).
Претходне епизоде РВО, исхемијске гране и централног РВО
Постоји ограничено искуство у лечењу пацијената са претходним епизодама РВО и пацијената са исхемијском граном РВО (БРВО) и централним РВО (ЦРВО). Код пацијената са РВО који имају губитак видне функције са клиничким знацима иреверзибилне исхемије, лечење је Не препоручује се.
04.5 Интеракције са другим лековима и други облици интеракција
Нису спроведена конвенционална испитивања интеракција.
За комбиновану примену фотодинамичке терапије (ПДТ) са вертепорфином и Луцентисом у влажној АМД и ПМ, видети одељак 5.1.
За комбиновану употребу ласерске фотокоагулације и Луцентиса у лечењу ДМЕ и БРВО, видети одељке 4.2 и 5.1.
04.6 Трудноћа и дојење
Жене у репродуктивном периоду / контрацепција код жена
Жене у репродуктивном периоду треба да користе ефикасну контрацепцију током лечења.
Трудноћа
За ранибизумаб нису доступни клинички подаци о изложености трудноћи. Студије на мајмунима циномолгус нису показале директне или индиректне штетне ефекте на трудноћу или ембрионални / фетални развој (видети одељак 5.3). Системска изложеност ранибизумабу је ниска након очне примене, али због механизма деловања ранибизумаб треба сматрати потенцијално тератогеним и ембрио / фетотоксичним. Због тога се ранибизумаб не сме примењивати током трудноће, осим ако очекиване користи надмашују потенцијални ризик за фетус. Женама које планирају трудноћу и које су лечене ранибизумабом препоручује се да сачекају најмање 3 месеца након последње дозе ранибизумаба пре зачећа бебе.
Трудноћа
Није познато да ли се Луцентис излучује у мајчино млеко. Препоручује се да не дојите док користите Луцентис.
Плодност
Нема доступних података о плодности.
04.7 Утицај на способност управљања возилима и машинама
Поступак лечења Луцентисом може изазвати пролазне сметње вида које могу утицати на способност управљања возилима и рада са машинама (видети одељак 4.8). Пацијенти који имају ове симптоме не би требали возити или управљати машинама док ови пролазни поремећаји вида не престану.
04.8 Нежељени ефекти
Сажетак сигурносног профила
Већина нежељених реакција пријављених након примене Луцентиса повезана је са поступком интравитреалне ињекције.
Најчешће пријављене очне нуспојаве након ињекције Луцентиса су: бол у оку, хиперемија ока, повишен интраокуларни притисак, витреитис, одвајање стакластог ткива, крварење у мрежњачи, сметње вида, пловци (крварење у стакластом тијелу), иритација ока, осјећај страног тијела око, повећано сузење, блефаритис, суво око и сврбеж ока.
Најчешће пријављене неокуларне нежељене реакције су главобоља, назофарингитис и артралгија.
Мање често пријављене, али озбиљније нежељене реакције укључују ендофталмитис, слепило, одвајање мрежњаче, руптуру мрежњаче и јатрогену трауматску катаракту (видети одељак 4.4).
Пацијенте треба обавестити о симптомима ових потенцијалних нежељених реакција и упутити их да обавесте свог лекара ако осете знакове као што су бол у очима или повећана нелагодност, погоршање црвенила ока, замагљен или смањен вид, повећан број стакластих лелујача или " повећана осетљивост на светлост.
Нежељене реакције пријављене након примене Луцентиса у клиничким студијама сажете су у доњој табели.
Табела нежељених реакција #
Нежељене реакције су наведене према органским системима и учесталости према следећој конвенцији: врло честе (≥1 / 10), честе (≥1 / 100,
Инфекције и инфестације
Веома честа Назофарингитис
заједнички Инфекција уринарног тракта *
Поремећаји крви и лимфног система
заједнички Анемија
Поремећаји имунолошког система
заједнички Преосетљивост
Психијатријски поремећаји
заједнички Анксиозност
Поремећаји нервног система
Веома честа Главобоља
Поремећаји ока
Веома честа Витреитис, одвајање стакластог тела, крварење у мрежњачи, сметње вида, бол у очима, флоатери у стакластом тијелу, крварење у коњуктиви, иритација ока, осећај страног тела у оку, повећана лакримација, блефаритис, суво око, очна хиперемија, сврбеж ока.
заједнички Дегенерација мрежњаче, поремећаји мрежњаче, одвајање мрежњаче, кидање мрежњаче, одвајање пигментног епитела ретине, пуцање пигментног епитела ретине, смањена оштрина вида, крварење у стакластом телу, поремећаји стакластог тела, увеитис, иритис, иридоциклитис, катаракта, поткапсуларна катаракта постериорна капсула кератитис, абразија рожњаче, реакција предње коморе, замагљен вид, крварење на месту убризгавања, крварење у очима, коњунктивитис, коњунктивитис
алергијски, очни исцједак, свјетлосни бљескови, фотофобија, очна нелагодност, едем капака, бол у очним капцима, хиперемија коњунктиве.
необичан Слепоћа, ендофталмитис, хипопион, хифема, кератопатија, синехије шаренице, наслаге рожњаче, едем рожњаче, стријеве рожњаче, бол на месту убризгавања, иритација на месту убризгавања, абнормални осећај у оку, иритација капака.
Поремећаји дисања, грудног коша и медијастинума
заједнички Кашаљ
Гастроинтестинални поремећаји
заједнички Мучнина
Поремећаји коже и поткожног ткива
заједнички Алергијске реакције (осип, осип, свраб, еритем)
Поремећаји мишићно -коштаног система и везивног ткива
Веома честа Артралгија
Дијагностички тестови
Веома честа Повећан интраокуларни притисак
# Нежељене реакције су дефинисане као нежељени догађаји (код најмање 0,5 процентних поена пацијената) који су се јавили са већом стопом (најмање 2 процентна поена) код пацијената који су били на терапији Луцентисом 0,5 мг у поређењу са онима који су примали контролни третман (лажни или ПДТ вертепорфин).
* забележено само у популацији са ДМЕ
Нежељене реакције повезане са категоријом лекова
У студијама ИИИ са влажним АМД-ом, укупна учесталост неокуларних крварења, нежељених догађаја потенцијално повезаних са инхибиторима ВЕГФ-а (фактор раста ендотелних судова), била је благо повећана код пацијената лечених ранибизумабом. Међутим, не постоји константан образац између различитих крварења. Постоји теоретски ризик од артеријских тромбоемболијских догађаја, укључујући мождани удар и инфаркт миокарда, који су резултат интравитреалне употребе инхибитора ВЕГФ. Ниска учесталост артеријских тромбоемболијских догађаја примећена је у клиничким испитивањима са Луцентисом код пацијената са АМД, ДМЕ, РВО и ПМ и нису уочене разлике међу групама ранибизумаба у поређењу са контролом.
Пријављивање сумње на нежељене реакције
Извештавање о сумњама на нежељене реакције које се јављају након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика од лека. Здравствени радници се моле да пријаве сваку сумњу на нежељену реакцију преко Италијанске агенције за лекове. , веб страница: хттпс://ввв.аифа.гов.ит/цонтент/сегналазиони-реазиони-авверсе.
04.9 Предозирање
Случајеви случајног предозирања забележени су из клиничких испитивања на мокром АМД-у и постмаркетиншких података. Нежељене реакције које су најчешће биле повезане са овим случајевима биле су повишен очни притисак, пролазно слепило, смањена оштрина вида, едем рожњаче и бол. Ако дође до предозирања, интраокуларни притисак треба пратити и лекар сматрати неопходним.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: Офталмолози, анти-неоваскуларни агенси, АТЦ ознака: С01ЛА04
Ранибизумаб је хуманизовани рекомбинантни фрагмент моноклоналног антитела усмерен против људског васкуларног ендотелног фактора раста А (ВЕГФ-А). Везује се са високим афинитетом за изоформе ВЕГФ-А (нпр. ВЕГФ110, ВЕГФ121 и ВЕГФ165), спречавајући тако везивање ВЕГФ-А за његове рецепторе ВЕГФР-1 и ВЕГФР-2. За његове рецепторе доводи до пролиферације ендотелних ћелија на неоваскуларизацију и повећање васкуларне пропустљивости за које се сматра да доприносе прогресији неоваскуларног облика старосне макуларне дегенерације, патолошке миопије или смањеног вида узрокованог или дијабетичким макуларним едемом или „Макуларним едемом секундарним у односу на РВО.
Третман влажног АМД -а
За влажну АМД, безбедност и клиничка ефикасност Луцентиса процењиване су у три 24-месечне рандомизоване, двоструко слепе, лажне или активно контролисане студије код пацијената са неоваскуларном АМД. Укупно 1.323 пацијената (879 лечених и 444 контроле) било је укључено у ове студије.
У студији ФВФ2598г (МАРИНА), 716 пацијената са минимално класичним или окултним лезијама хороидалне неоваскуларизације (ЦНВ) без класичне компоненте примило је месечне интравитреалне ињекције Луцентиса 0,3 мг (н = 238) или 0,5 мг (н = 240) или лажне ињекције (н = 238).
У студији ФВФ2587г (АНЦХОР), 423 пацијента са претежно класичним ЦНВ -ом примило је један од следећих третмана: 1) месечне интравитреалне ињекције Луцентиса 0,3 мг и лажног ПДТ -а (н = 140); 2) месечне интравитреалне ињекције Луцентиса 0,5 мг и лажног ПДТ -а (н = 140); или 3) интравитреалне лажне ињекције и ПДТ са вертепорфином (н = 143). ПДТ са вертепорфином или лажним је даван заједно са почетном ињекцијом Луцентиса, а затим свака 3 месеца ако је флуорангиографија показала постојаност или наставак васкуларног цурења.
Кључни налази сажети су у табелама 1, 2 и на слици 1.
Табела 1 Резултати у 12. и 24. месецу у студији ФВФ2598г (МАРИНА)
ап
Табела 2 Резултати у 12. и 24. месецу у студији ФВФ2587г (СИДРА)
Сто
Резултати обе студије показали су да би наставак лечења ранибизумабом такође могао бити од користи код пацијената који су изгубили ≥15 слова најбоље кориговане оштрине вида (БЦВА) у првој години лечења.
Студија ФВФ3192г (ПИЕР) је рандомизирана, двоструко слепа, лажно контролисана студија осмишљена да процени безбедност и ефикасност Луцентиса код 184 пацијената са свим облицима неоваскуларне АМД. Пацијенти су примили интравитреалне ињекције Луцентиса 0,3 мг (н = 60) или 0,5 мг (н = 61) или лажне ињекције (н = 63) једном месечно у 3 узастопне дозе, након чега следи једна доза која се даје једном у 3 месеца. Од 14. месеца студије, пацијенти лечени лажном ињекцијом примани су лечење ранибизумабом, а од 19. месеца могли су да се изводе чешћи третмани. Пацијенти лечени Луцентисом у ПИЕР студији примили су у просеку укупно 10 третмана.
Примарна крајња тачка ефикасности била је средња промена видне оштрине након 12 месеци у поређењу са основном вредношћу.Након почетног повећања видне оштрине (након месечне дозе), у просеку се видна оштрина пацијената смањивала са тромесечним дозирањем, враћајући се на почетну вредност у 12. месецу, а овај ефекат је задржан код већине лечених пацијената. Са ранибизумабом (82%) Месец 24. Подаци ограниченог броја испитаника који су преведени на лечење ранибизумабом након више од годину дана лажног лечења сугеришу да рано започињање лечења може бити повезано са бољим задржавањем „видне оштрине“.
И у студијама МАРИНА и у АНЦХОР-у побољшање видне оштрине примећено са Луцентисом од 0,5 мг након 12 месеци било је праћено користима које су пријавили пацијенти мерене резултатом Упитника за визуелне функције Националног института за очи (ВФК-25). Разлике између Луцентиса 0,5 мг и две контролне групе су процењене са вредностима п у распону од 0,009 до
Ефикасност Луцентиса у лечењу влажног АМД-а потврђена је у постмаркетиншким студијама АМД-а. Подаци из две студије (МОНТ БЛАНЦ, БПД952А2308 и ДЕНАЛИ, БПД952А2309) нису показали додатне ефекте комбиноване примене вертепорфина (Висудине ПДТ) и Луцентис у поређењу са самим Луцентисом.
Лечење оштећења вида услед ДМЕ
Безбедност и ефикасност лека Луцентис процењиване су у две рандомизиране, двоструко слепе, лажно контролисане или активне 12-месечне студије код пацијената са смањеним видом због дијабетичког макуларног едема. Укупно су ове студије биле укључене. Од 496 пацијената (336 активних и 160 контрола), већина је имала дијабетес типа ИИ, 28 лечених пацијената имало је дијабетес типа И.
У другој фази студије Д2201 (РЕСОЛВЕ), 151 пацијент је лечен ранибизумабом (6 мг / мл, н = 51, 10 мг / мл, н = 51) или лажним (н = 49) са једном "интравитреалном ињекцијом месечно. док се не испуне унапред дефинисани критеријуми. Почетна доза ранибизумаба (0,3 мг или 0,5 мг) могла се удвостручити у било ком тренутку током студије након прве ињекције. Ласерска фотокоагулација је била дозвољена као спасоносни третман од 3. месеца у обе руке. Студија имао је два дела: истраживачки део (првих 42 пацијената посећено у 6. месецу) и потврдни део (преосталих 109 пацијената посећено у 12. месецу).
Кључни налази из потврдног дела студије (2/3 пацијената) сажети су у Табели 3.
Табела 3 Исходи у 12. месецу у студији Д2201 (РЕШИ) (укупна популација студије)
ап
У студији ИИИ фазе Д2301 (РЕСТОРЕ), 345 пацијената са оштећењем вида због макуларног едема било је рандомизовано да прими или „интравитреалну ињекцију од 0,5 мг ранибизумаба као монотерапију и ласерску лажну фотокоагулацију (н = 116), или комбинацију од 0,5 мг ранибизумаб и ласерска фотокоагулација (н = 118) или „лажна ињекција и ласерска фотокоагулација (н = 111). Лечење ранибизумабом започето је месечним интравитреалним ињекцијама и настављало се док оштрина вида није остала стабилна најмање три узастопне месечне провере. Лечење је настављено када је примећено смањење БЦВА услед прогресије ДМЕ. Ласерска фотокоагулација је примењена на почетку истог дана, најмање 30 минута пре ињекције ранибизумаба, а након тога према потреби на основу критеријума ЕТДРС.
Кључни налази сажети су у табели 4 и на слици 2.
Табела 4 Резултати у 12. месецу у студији Д2301 (ОБНОВИ)
ап
Ефекат је био доследан у већини подгрупа, међутим, субјекти са прилично високим БЦВА на почетку (> 73 слова) са макуларним едемом и централном дебљином мрежњаче
Побољшање видне оштрине у 12. месецу примећено са Луцентисом 0,5 мг било је пропраћено користима главних функција повезаних са видом које је пријавио пацијент, мерено резултатом Упитника за визуелне функције Националног института за очи (ВФК-25). Не постоје разлике због лечења Разлика између Луцентиса 0,5 мг и контролне групе је процењена са п-вредношћу од 0,0137 (ранибизумаб моно) и 0,0041 (ранибизумаб + ласер) за композитни резултат ВФК-25.
У обе студије, визуелно побољшање пратило је континуирано смањење макуларног едема мерено као централна дебљина мрежњаче (ЦРТ).
Третман оштећења вида узрокованог макуларним едемом који је последица РВО
Клиничка безбедност и ефикасност Луцентиса код пацијената са оштећењем вида услед макуларног едема који је последица РВО-а процењивани су у рандомизованим, двоструко слепим, контролисаним испитивањима: БРАВО и ЦРУИСЕ који су регрутовали пацијенте са БРВО (н = 397) и ЦРВО (н = 392) У обе студије, пацијенти су примили или 0,3 мг или 0,5 мг ранибизумаба интравитреално или лажне ињекције. Након 6 месеци, пацијенти у лажној контролној руци премештени су у групу ранибизумаба 0,5 мг. У БРАВО студији, ласерска фотокоагулација као третман за спасавање био дозвољен у свим оружјима од 3. месеца.
Кључни налази из студија БРАВО и ЦРУИСЕ приказани су у Табелама 5 и 6
Табела 5 Резултати у 6. и 12. месецу (БРАВО)
ап
Табела 6 Резултати у 6. и 12. месецу (КРСТАРЕЊЕ)
ап
У обе студије, визуелно побољшање пратило је континуирано и значајно смањење макуларног едема мерено у смислу дебљине централне ретине.
Код пацијената са БРВО -ом (студија БРАВО и продужење студије ХОРИЗОН): Након 2 године, пацијенти који су били лечени лажним ињекцијама у првих 6 месеци, а затим прешли на лечење ранибизумабом, имали су повећање АВ (& симп; 15 слова) упоредиво са тим пацијената који су лечени ранибизумабом од почетка студије (& симп; 16 слова).Међутим, број пацијената који су навршили 2 године био је ограничен и у студији ХОРИЗОН заказане су само тромјесечне посјете. Стога нема довољно доказа који би закључили препорукама о томе када треба започети лијечење ранибизумабом код пацијената са БРВО.
Код пацијената са ЦРВО (студија ЦРУИСЕ и продужење студије ХОРИЗОН): После 2 године, пацијенти који су у првих 6 месеци били лечени лажним ињекцијама, а затим преведени на терапију ранибизумабом, нису показали повећање АВ (& симп; 6 слова) у поређењу са онима пацијената који су лечени ранибизумабом од почетка студије (& симп; 12 слова).
Побољшање видне оштрине примећено током лечења ранибизумабом у 6. и 12. месецу праћено је добробитима које су пријавили пацијенти мерене анкетним упитником за визуелне функције Националног института за очи (НЕИ ВФК-25) за блиске и удаљене активности Разлика између Луцентиса 0,5 мг и утврђено је да се контролна група налази између вредности п између 0,02 и 0,0002.
Лечење оштећења вида услед ЦНВ -а секундарно са ПМ
Безбедност и клиничка ефикасност Луцентиса код пацијената са оштећењем вида услед ЦНВ у ПМ потврђени су на основу 12-месечних података из кључне рандомизоване, двоструко слепе, контролисане студије Ф2301 (РАДИАНЦЕ). Ова студија је имала за циљ да процени два различита режима дозирања. ранибизумаба 0,5 мг примењеног интравитреалном ињекцијом у односу на вертепорфински ПДТ (вПДТ, визудинска фотодинамичка терапија). 277 пацијената је рандомизовано у једну од следећих група:
• Група И (ранибизумаб 0,5 мг, режим лечења одређен критеријумима "стабилности" дефинисаним као нема промене БЦВА у односу на процене у претходна два месеца).
• Група ИИ (ранибизумаб 0,5 мг, режим лечења одређен према критеријуму "активности болести" дефинисан као оштећење вида приписује се интра- или субретиналној течности или активном истицању изазваном лезијама ЦНВ-а, што доказују ОЦТ и / или АФ).
• Група ИИИ (пацијенти лечени вПДТ - са могућношћу лечења ранибизумабом почевши од 3. месеца).
Током 12 месеци студије, пацијенти су примили у просеку 4,6 ињекција (опсег 1-11) у Групи И и 3,5 ињекције (опсег 1-12) у Групи ИИ. Међу пацијентима који припадају групи ИИ, која одражава препоручену дозу (видети одељак 4.2), 50,9% пацијената је прошло терапију са 1 до 2 ињекције, 34,5% 3 до 5 ињекција и 14,7% је дало 6 до 12 ињекција током 12-месечне студије . 62,9% пацијената ИИ групе није захтевало ињекције током других 6 месеци студије.
Кључни налази РАДИАНЦЕ -а сажети су у табели 7 и на слици 5.
Табела 7 Резултати у 3. и 12. месецу (РАДИАНЦЕ)
ап
б Упоредна контрола до 3. месеца Пацијенти рандомизовани да приме вПДТ били су подобни за лечење ранибизумабом 3. месеца (у ИИИ групи, 38 пацијената је добило ранибизумаб 3. месеца)
Побољшање вида било је праћено смањењем дебљине централне ретине.
У поређењу са групом која је примала вПДТ, пацијенти у групама леченим ранибизумабом пријавили су корист (п-вредност
Педијатријска популација
Безбедност и ефикасност ранибизумаба код деце још нису утврђени.
Европска агенција за лекове одустала је од обавезе достављања резултата студија са Луцентисом у свим подскупинама педијатријске популације за неоваскуларну АМД, оштећење вида услед ДМЕ, оштећење вида услед секундарног макуларног едема због РВО и оштећење вида услед секундарног ЦНВ ПМ (видети одељак 4.2 за информације о педијатријској употреби).
05.2 Фармакокинетичка својства
Након месечне интравитреалне примене Луцентиса код пацијената са неоваскуларном АМД, серумске концентрације ранибизумаба су генерално биле ниске, са максималним нивоима (Цмак) генерално испод концентрације ранибизумаба потребне за инхибирање биолошке активности ВЕГФ-а за 50% (11-27 нг / мЛ) , оцењено на тесту ин витро пролиферација ћелија). Цмак је била пропорционална дози у целом распону доза од 0,05 до 1,0 мг / око. Код ограниченог броја пацијената са ДМЕ -ом, откривене концентрације у серуму указују на то да се не може искључити нешто већа системска изложеност онима које су примећене код пацијената са неоваскуларном АМД. Серумске концентрације ранибизумаба код пацијената са РВО биле су сличне или незнатно веће од оних које су примећене код пацијената са неоваскуларном АМД.
На основу популационе фармакокинетичке анализе и серумског клиренса ранибизумаба за неоваскуларне АМД пацијенте лечене дозом од 0,5 мг, средњи полувреме елиминације ранибизумаба у стакластом тијелу је приближно 9 дана. У време месечне интравитреалне примене Луцентиса 0,5 мг / око, очекује се да ће серумски Ц ранибизумаба, достигнут приближно 1 дан након дозе, генерално кретати између 0,79 и 2,90 нг / мл, док се очекује да Цмин генерално варира између 0,07 и 0,49 нг / мл. Процењује се да су концентрације ранибизумаба у серуму приближно 90.000 пута ниже од концентрација у стакластом телу.
Пацијенти са бубрежном инсуфицијенцијом: Нису спроведене конвенционалне студије за испитивање фармакокинетике Луцентиса код пацијената са бубрежном инсуфицијенцијом. У „фармакокинетичкој анализи у популацији пацијената са неоваскуларном АМД, 68% (136 од 200) пацијената имало је„ бубрежну инсуфицијенцију (46,5% блага [50-80 мЛ / мин], 20% умерена [30 -50 мЛ / мин] и 15% озбиљан [системски клиренс је био нешто нижи, али то није било клинички значајно.
Пацијенти са инсуфицијенцијом јетре: Нису спроведене конвенционалне студије које би испитивале фармакокинетику Луцентиса код пацијената са инсуфицијенцијом јетре.
05.3 Предклинички подаци о безбедности
Билатерална интравитреална примена ранибизумаба мајмунима циномолгус у дозама између 0,25 мг / око и 2,0 мг / око једном у 2 недеље до 26 недеља довела је до очних ефеката зависних од дозе.
Интраокуларно, повећање брзине и ћелија зависило је од дозе у предњој комори, а врхунац је достигао 2 дана након ињекције. Озбиљност упалног одговора опћенито се смањује с накнадним ињекцијама или током периода опоравка.Дошло је до ћелијске инфилтрације и стакластог плутања у задњем сегменту, који је такође имао тенденцију да зависи од дозе и опћенито је постојао до краја периода лијечења. У студији од 26 недеља, озбиљност упале стакластог тела се повећавала са бројем ињекција. Међутим, реверзибилност је примећена након периода опоравка. Природа и трајање упале задњег сегмента указују на одговор антитела. што може бити клинички неважно. Формирање катаракте је примећено код неких животиња након релативно дугог периода интензивне упале, што сугерише да су промене сочива биле секундарне због тешке упале. Након интравитреалних ињекција, примећено је пролазно повећање очног притиска након примене, без обзира на дозу.
Микроскопске очне промене биле су повезане са упалом и нису указивале на дегенеративне процесе.Упале грануломатозне промене забележене су на оптичком диску неких очију. Ове промене задњег сегмента су се смањиле, а у неким случајевима и решиле, током периода опоравка.
Није било знакова системске токсичности након интравитреалне примене. Серумска и стакласта антитела на ранибизумаб нађена су у подскупу третираних животиња.
Нису доступни подаци о канцерогености или мутагености.
Код трудних мајмуна, интравитреална ињекција ранибизумаба резултирала је максималном системском изложеношћу 0,9-7 пута најгоре клиничке изложености није узроковала развојну токсичност или тератогеност, те није имала утјецаја на тежину или структуру тијела. тератоген и ембрио / фетотоксичан на основу фармаколошког дејства.
Одсуство посредованих ефеката ранибизумаба на развој ембриона / фетуса је вероватно повезано углавном са немогућношћу фрагмента Фаб да пређе плаценту. Међутим, описан је случај са високим нивоом ранибизумаба у мајчином серуму и присуством ранибизумаба у феталном серуму, што сугерише да је антитело против ранибизумаба деловало као протеин (који садржи ФЦ регију) који транспортује ранибизумаб, чиме се смањује његово уклањање из мајчиног серума и дозвољавајући његово преношење у плаценту. Будући да су тестови на развој ембрија / фетуса проведени на здравим трудним животињама и да неке болести (попут дијабетеса) могу промијенити плацентну пропусност за Фаб фрагмент, студију је потребно тумачити с опрезом.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
α, α-трехалоза дихидрат
Хистидин хидрохлорид, монохидрат
Хистидин
Полисорбат 20
Вода за ињекције
06.2 Некомпатибилност
У недостатку студија компатибилности, овај лек се не сме мешати са другим лековима.
06.3 Период важења
3 године
06.4 Посебне мере предострожности при складиштењу
Чувати у фрижидеру (2 ° Ц - 8 ° Ц).
Немојте замрзавати.
Бочицу чувајте у спољном паковању ради заштите лека од светлости.
06.5 Природа непосредног паковања и садржај паковања
0,23 мл стерилног раствора у бочици (стакло типа И) са чепом (хлоробутил гума), 1 тупом иглом за филтрирање (18Г к 1½ ", 1,2 мм к 40 мм, 5 мцм), 1 иглом за ињекцију (30Г к ½", 0,3 мм к 13 мм) и 1 шприц (полипропилен) (1 мл). Паковање садржи 1 бочицу.
06.6 Упутства за употребу и руковање
Бочица, игла за ињекцију, игла за филтер и шприц су само за једнократну употребу. Поновна употреба може изазвати инфекцију или другу болест / повреду. Све компоненте су стерилне. Не смије се користити било која компонента на чијем паковању постоје знаци оштећења или неовлаштеног рада. Не може се гарантовати стерилност ако печат на амбалажи компоненте није нетакнут.
Да бисте припремили Луцентис за интравитреалну ињекцију, следите доле наведена упутства:
1. Пре сакупљања дезинфикујте спољни део гуменог чепа бочице.
2. Асептично причврстите иглу филтера од 5 мцм (18Г к 1½ ", 1,2 мм к 40 мм, испоручено) на шприц од 1 мл (испоручено). Уметните тупу иглу филтера у средину поклопца док не додирне дно бочице.
3. Извуците сву течност из бочице држећи је у усправном положају, благо нагнутом да бисте олакшали потпуно повлачење.
4. Уверите се да је клип шприца повучен довољно уназад приликом пражњења бочице да бисте потпуно испразнили иглу филтера.
5. Оставите иглу филтера тупу у бочици и извадите шприц из ње. Одбаците иглу филтера након што извучете садржај бочице и немојте је користити за интравитреалну ињекцију.
6. Чврсто и асептично причврстите ињекциону иглу (30Г к ½ ", 0,3 мм к 13 мм, испоручено) на шприц.
7. Пажљиво уклоните поклопац са ињекционе игле без одвајања ињекционе игле са шприца.
Напомена: Држите жуту подлогу ињекционе игле док уклањате поклопац.
8. Пажљиво избаците ваздух из шприца и подесите дозу на 0,05 мл означену на шприцу Шприца је спремна за ињекцију.
Напомена: Не чистите ињекциону иглу и не повлачите клип уназад.
Након ињекције, немојте покривати иглу нити је одвајати од шприца. Одложите употребљени шприц заједно са иглом у одговарајући контејнер или у складу са локалним захтевима.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Новартис Еуропхарм Лимитед
Вимблехурст Роад
Хорсхам
Западни Сасекс, РХ12 5АБ
УК
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
ЕУ/1/06/374/001
037608027
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 22. јануар 2007
Датум последњег обнављања: 24. јануар 2012
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
05/2014