Гликоген је макромолекула (молекулска маса од око 400 милиона далтона) α-глукозе у којој углавном постоје α-1,4 гликозидне везе и гранања у омјеру 1:10, због α-1,6 гликозидних веза.
Гликоген чини резервни материјал и стално се разграђује и реконституише; у целој телесној ћелијској маси има око 100 г гликогена: већина се налази у јетри где је покретна и стога се може користити као резерва за друге органе (гликоген у мишићима није покретан).
Сви ензими који катализују разградњу и синтезу гликогена налазе се у цитоплазми, стога је потребан систем регулације који чини један пут неактивним када је други активан: ако постоји доступна глукоза, она се претвара у гликоген (анаболизам), што је резерва, обрнуто, ако је за глукозу потребан ц ", тада се гликоген разграђује (катаболизам).

Ензим који је углавном укључен у разградњу гликогена је гликоген фосфорилаза; овај ензим је у стању да цепи гликозидну везу α-1,4 користећи аноргански ортофосфат као литичко средство: цепање се одвија фосфоролитичким путем и добија се 1-фосфат глукозе.
На пет или шест јединица од тачке гранања, ензим гликоген фосфорилаза више није у стању да делује, па се одваја од гликогена и замењује га ензим за дерамификацију који је трансфераза: на каталитичком месту овог ензима ц "је" хистидин који омогућава пренос три сахаридне јединице у најближи гликозидни ланац (хистидин напада први угљеник молекула глукозе). Управо поменути ензим је гликозилтрансфераза; на крају дејства овог ензима, само једна јединица глукозе остаје на бочном ланцу са првим угљеником везаним за шести угљеник глукозе у главном ланцу.Последња јединица глукозе у бочном ланцу ослобађа се дејством "ензим α-1,6 гликозидаза (овај ензим чини други део ензима за дерамификацију); с обзиром на то да су гране у гликогену у односу 1:10, потпуном разградњом макромолекуле добијамо око 90% глукозе 1-фосфата и око 10% глукоза.
Деловање горе наведених ензима омогућава елиминацију бочног ланца из молекула гликогена; активност ових ензима се може понављати све док не дође до потпуне деградације ланца.
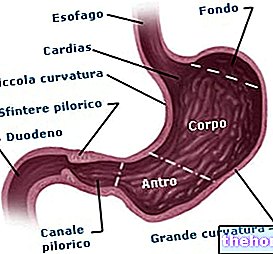
Хајде да размотримо хепатоцит; глукоза (која се асимилује исхраном), када уђе у ћелију, претвара се у глукозу 6-фосфат и тако се активира. Глукоза 6-фосфат, дејством фосфоглукомутаза, се трансформише у глукозу 1-фосфат: потоњи је непосредни прекурсор биосинтезе; у биосинтези се користи активирани облик шећера који је представљен шећером везаним за дифосфат: обично уридилдифосфат (УДП). Глукоза 1-фосфат је затим се претвара у УДП-глукозу, овај метаболит под дејством гликоген синтаза који је у стању да веже УДП-глукозу за несредујући крај растућег гликогена: добија се продужени гликоген глукозидне јединице и УДП.УДП се претвара помоћу ензима нуклеозидне дифосфокиназе у УТП који се враћа у циркулацију.
До разградње гликогена долази дејством гликоген фосфорилаза који ослобађа молекул глукозе и претвара га у глукозу 1-фосфат. Након тога, фосфоглукомутаза претвара глукозу 1-фосфат у глукозу 6-фосфат.
Гликоген се синтетише, пре свега, у јетри и мишићима: у организму постоји 1-1,2 хектограма гликогена распоређених по мишићној маси.
Гликоген миоцита представља резерву енергије само за ову ћелију, док је гликоген који се налази у јетри такође резерва за друга ткива, односно може се, као глукоза, послати у друге ћелије.
Глукоза-6-фосфат добијен у мишићима разградњом гликогена затим се шаље, у случају потребе за енергијом, на гликолизу; у јетри се глукоза 6-фосфат претвара у глукозу дејством глукоза 6-фосфат фосфатаза (карактеристичан ензим хепатоцита) и преноси се у крвоток.
Гликоген синтаза и гликоген фосфорилаза делују на нередуцирајуће јединице гликогена, па мора постојати хормонски сигнал који наређује активирање једног пута и блокирање другог (или обрнуто).
У лабораторији је било могуће продужити гликогенски ланац експлоатацијом гликоген фосфорилазе и употребом глукоза 1-фосфата у врло високој концентрацији.
У ћелијама гликоген фосфорилаза само катализује реакцију разградње јер су концентрације метаболита такве да померају равнотежу следеће реакције удесно (тј. Ка разградњи гликогена):

Погледајмо механизам деловања гликоген фосфорилазе: ацетални кисеоник (који делује као мост између јединица глукозе) везује се за водоник фосфорила: реакциони међупродукт настаје карбокацијом (на глукози која је све " екстремитети) за које се фосфорил (Пи) везује врло брзо.
Гликоген фосфорилаза захтева кофактор који је пиридоксал фосфат (овај молекул је такође кофактор за трансаминазе): има делимично протонирани фосфорил (пиридоксал фосфат је окружен хидрофобном средином која оправдава присуство протона везаних за њега). Фосфорил (Пи) је у стању да пренесе протон у гликоген јер овај фосфорил затим поново преузима протон из делимично протонираног фосфорила пиридоксал фосфата. Вероватноћа да при физиолошком пХ фосфорил изгуби свој протон и остане потпуно депротониран је веома мала.
Хајде сада да видимо како фосфоглукомутаза делује. Овај ензим представља, на каталитичком месту, остатак фосфорилисаног серина; серин даје фосфорил у глукозу 1-фосфат (на позицији шест): глукоза 1,6-бисфосфат се формира кратко време, затим се серин рефосфорилише узимајући фосфорил у позицију један. Фосфоглуко мутаза може деловати у оба смера, односно претварати глукозу 1-фосфат у глукозу 6-фосфат или обрнуто; ако се произведе глукоза-6-фосфат, он се може послати директно на гликолизу, у мишићима, или трансформисати у глукозу у јетри.
Ензим уридил фосфоглуко трансфераза (или УДП глукоза пирофосфорилаза) катализује реакцију преноса глукозе 1-фосфата на УТП везивањем за фосфорил а.
Ензим који је управо описан је пирофосфорилаза: ово име је због чињенице да је супротна реакција на ону која је управо описана пирофосфорилација.
УДП глукоза, добијена на описани начин, може продужити ланац гликогена, помоћу моносахаридне јединице.
Могуће је да се реакција развије ка стварању УДП глукозе уклањањем производа који је пирофосфат; ензим пирофосфатаза претвара пирофосфат у два молекула ортофосфата (хидролиза анхидрида) и на тај начин одржава концентрацију пирофосфата тако ниском да чини процес формирања УДП глукозе термодинамички повољним.
Као што је поменуто, УДП глукоза, захваљујући дејству гликоген синтазе, може да продужи ланац гликогена.
Развејаности (у односу 1:10) су последица чињенице да, када се ланац гликогена састоји од 20-25 јединица, интервенише разгранати ензим (који има "хистидин на свом каталитичком месту), способан да пренесе низ 7 -8 гликозидних јединица даље низводно од 5-6 јединица: тако се ствара ново гранање.
Због нервног порекла или ако је потребна енергија због физичког напора, адреналин се лучи из надбубрежних жлезда.
Циљне ћелије адреналина (и норадреналина) су ћелије јетре, мишића и масног ткива (у потоњем долази до разградње триглицерида и циркулације масних киселина: због тога се глукоза производи у митохондријском 6 -фосфату, послат на гликолизу, док се у адипоцитима глукоза 6-фосфат дејством ензима глукоза 6-фосфат фосфатаза претвара у глукозу и извози у ткива).
Да видимо, сада модалитети деловања адреналина. Адреналин се везује за рецептор који се налази на ћелијској мембрани (од миоцита и хепатоцита) и то одређује превођење сигнала споља ка унутрашњости ћелије.Активира се протеинска киназа која истовремено делује на системе који регулишу синтезу и разградњу гликогена:
Гликоген синтаза постоји у два облика: дефосфорилирани (активни) облик и фосфорилисани (неактиван) облик; протеин киназа фосфорилише гликоген синтазу и блокира њено деловање.
Гликоген фосфорилаза може постојати у два облика: активни облик у којем је присутан фосфорилисани серин и неактиван облик у којем је серин дефосфорилиран. Ензим може активирати гликоген фосфорилазу гликоген фосфорилаза киназа. Гликоген фосфорилаза киназа је активна ако је фосфорилисана и неактивна ако је дефосфорилирана; протеинска киназа има као супстрат гликоген фосфорилаза киназу, односно способна је да фосфорилише (и, стога, активира) ову другу, која заузврат активира гликоген фосфорилазу.
Када се сигнал адреналина заврши, ефекат који има на ћелију такође мора престати: ензими фосфатазе затим интервенишу на врсту протеина.